
【题目】设NA表示阿伏加德罗常数的值,下列说法中正确的是
A. 常温常压下,56g丙烯与环丁烷的混合气体中含有4NA个碳原子
B. 25℃,pH=1的H2SO4溶液中,H+的数目为0.2NA
C. 标准状况下,0.1molCl2溶于水,转移的电子数目为0.1NA
D. 1mol的P4O6中含有6 NA个P-O键(P4O6的结构如图: ![]() )
)
 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:
【题目】掌握仪器名称、组装及使用方法是中学化学实验的基础,如图为两套实验装置。
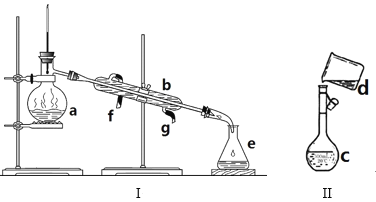
(1)写出下列仪器的名称:a、_____b、 _____
(2)若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器是____,将仪器补充完整后进行实验,温度计水银球的位置在____处。冷凝水由____(填f或g)口通入,___口流出。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过海水晾晒可以得到粗盐,粗盐除还有NaCl外,还含有MgCl2、 CaCl2、 Na2SO4以及泥沙等杂质。以下是某兴趣小组制备精盐的实验方案,各步操作流程如下。下列说法正确的是

A. 实验过程中①、⑤步骤的操作分别是溶解、过滤
B. 实验过程中步骤④的目的是仅除去溶液中的Ca2+
C. 实验过程中步骤⑦中的蒸发所用到的仪器是酒精灯、玻璃棒、烧杯、铁架台(带铁圈)
D. 实验过程中②、④步骤互换,对实验结果不影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下 ①6.72L CH4 ②3.01×1023个HCl分子 ③13.6g H2S ④0.2 mol NH3,这四种气体的关系表达正确的是( )
a.体积②>③>①>④ b.密度②>③>④>①
c.质量②>③>①>④ d.氢原子个数①>③>④>②
A.abcB.bcdC.abdD.abcd
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上将苯的蒸汽通过赤热的铁合成一种可作传热载体的化合物,该化合物分子中苯环上的一氯化物有3种,1mol该化合物催化加氢时最多消耗6mol氢气,判断这种化合物可能是(提示:在一定条件下,醛基也可以与H2发生加成反应)( )
A. ![]() B.
B. ![]()
C. ![]() D.
D. 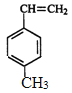
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】曾在南充求学和工作过的青年学者孙旭平及其领衔团队,近日成功利用Mo2N纳米催化剂在0.1mol·L1盐酸溶液中进行电催化固氮,装置如图所示,在一定电压下具有较高的产氨速率。下列判断错误的是

A. Mo2N/GCE电极为阴极
B. 溶液中H+通过隔膜向MoN/GCE电极区迁移
C. Mo2N/GCE电极区反应式为N2+6H++6e====2NH3
D. 为提高溶液的导电性,可在石墨电极区加入适量的盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化硫的催化氧化是工业上生产硫酸的主要反应,反应如下:2SO2(g)+O2(g)![]() 2SO3(g) △H1=-197.7kJ·mol-1 K1(浓度平衡常数)
2SO3(g) △H1=-197.7kJ·mol-1 K1(浓度平衡常数)
为研究该反应,某同学设计了以下三种已装固体V2O3催化剂的密闭容器装置

(1)在初始体积与温度相同的条件下,甲、乙、丙中均按2 mol SO2、1molO2投料,达平衡时,三个容器中SO2的转化率从大到小的顺序为___________________(用“甲、乙、丙”表示)。
(2)在容器丙中,0.1MPa条件下,在不同温度或不同投料方式下研究上述反应得到数据如下表:
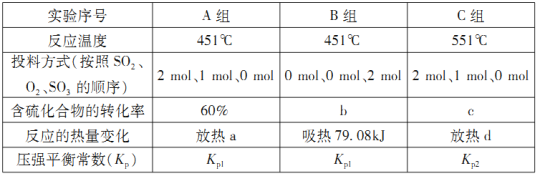
①表中:a=___________;b=___________。
②已知用平衡分压(分压=总压×物质的量分数)代替平衡浓度计算,得到的平衡常数即为压强平衡常数,则Kp1___________Kp2(填“>”、“<”或“=”)。
③451℃,若按0.4 mol SO2、0.4molO2、0.4 mol SO3进行投料,则反应开始时v正(SO2)_______v逆(SO2)(填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯酸钾是常见的氧化剂,用于制造火药、烟火。工业上用石灰乳氯化法制备氯酸钾的流程如图所示:
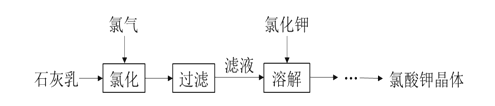
已知:氯化过程主要发生反应:![]()
完成下列填空:
(1)工业生产氯气的方法是________(请用文字表述)。
(2)氯化过程需要控制较高温度,其目的有:①_______;②减少Cl2与Ca(OH)2之间的副反应。
(3)向热的滤液中加入稍过量的氯化钾,待溶解完全后进行冷却,有大量氯酸钾晶体析出,写出相关反应的化学方程式:______。得到的氯酸钾晶体中可能会含有少量氯化钾,进一步提纯的方法是_______。
(4)为测定所得晶体中氯酸钾的纯度,将a g样品与b g二氧化锰混合,加热该混合物一段时间后(杂质不参加反应)冷却,称量剩余固体质量,重复加热、冷却、称量操作,记录数据如下表:
加热次数 | 第一次 | 第二次 | 第三次 | 第四次 |
剩余固体质量(g) | c | d | e | e |
(i)进行加热操作时,应将固体置于________(填仪器名称)中。
(ii)该实验不必进行第五次加热的原因是_______。
(iii)若某次测定结果的相对误差为-2.98%,写出导致这一结果的一种可能情况。______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com