
ʵ�飺��0.1 mol·L��1MgCl2��Һ��0.2 mol·L��1NaOH��Һ�������ϵõ���Һa��ȡ������Һa���˵õ���Һb�Ͱ�ɫ����c��������Һa�еμ�0.1 mol·L��1FeCl3��Һ�����ֺ��ɫ���������з�������ȷ����(����)
A��Һb��pH��7
B��������ɫ�仯˵��Mg(OH)2ת��ΪFe(OH)3
C��ʵ�����֤��Fe(OH)3���ܽ�ȱ�Mg(OH)2��С
D����Һa�д��ڳ����ܽ�ƽ�⣺Mg(OH)2(s)??
Mg2��(aq)��2OH��(aq)
 �������¿��ÿ�ʱ��ҵϵ�д�
�������¿��ÿ�ʱ��ҵϵ�д� Ӣ�żƻ�ͬ����ʱ��Чѵ��ϵ�д�
Ӣ�żƻ�ͬ����ʱ��Чѵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ�������£���E(g)��F(g)������������2 L�ܱ������У�����������Ӧ������5 minĩ�ﵽƽ�⣺2E(g)��F(g)2G(g)���й��������£�
| E(g) | F(g) | G(g) | |
| ��ʼŨ��/mol��L��1 | 2.0 | 1.0 | 0 |
| ƽ��Ũ��/mol��L��1 | c1 | c2 | 0.4 |
�����ж���ȷ����(����)
A����Ӧ��ǰ5 min�ڣ�v(E)��0.04 mol��L��1��min��1
B�������������䣬������E��Ũ�ȣ����ƽ��ʱE��ת���ʻ�����
C�������������䣬�����¶ȣ�ƽ��ʱn(E)��3.0 mol����Ӧ�Ħ�H��0
D��ƽ�������2.0 mol E��1.0 mol F������ͬ�������ٴ�ƽ��ʱ��c(G)��0.2 mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij���Ͻ�Ӳ�����к���þ��ͭ���裬Ϊ�˲ⶨ�úϽ������ĺ����������������ʵ�飺
��1��ȡ��Ʒa g������ʱʹ�õ���������Ϊ________________________________________________________________________��
��2������Ʒ����������ϡ�����У����ˣ���Һ����Ҫ���С����������� �������к��С������������ܽ⡢����ʱʹ�õ�����Ϊ________________________________________________________________________��
��3������Һ�м������������������Һ�����ˣ�д���ò�������з�Ӧ�Ļ�ѧ����ʽ______________________________________________��
��4���ڵڣ�3��������Һ��ͨ������CO2�����ˣ�������������ˮϴ�����κ�ɲ��������������ټ���Ϊֹ����ȴ�����������Ϊb g��
��5���Ͻ���������������Ϊ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ж�������ȷ�Ļ����̡�������Ļ�������
(1)Ca(OH)2���Ƴɳ���ʯ��ˮ�����Կ�����2.0 mol·L��1��Ca(OH)2��Һ(����)
(2014·�㶫���ۣ�9D)
(2)�ܽ��С�ij��������ܽ�ȸ�С�ij���ת��������ZnS�����еμ�CuSO4��Һ���Եõ�CuS����(����)
(2014·�������ۣ�12D)
(3)��֤Fe(OH)3���ܽ��С��Mg(OH)2���ɽ�FeCl3��Һ����Mg(OH)2����Һ�У����ɹ۲쵽�����ɰ�ɫ��Ϊ���ɫ(����)
(2014·�Ĵ����ۣ�4D)
(4)25 ��ʱCu(OH)2��ˮ�е��ܽ�ȴ�������Cu(NO3)2��Һ�е��ܽ��(����)
(2014·�������ۣ�3D)
(5)AgCl������ת��ΪAgI������K(AgX)��c(Ag��)·c(X��)����K(AgI)��K(AgCl)(����)
(2013·�������ۣ�2D)
(6)CaCO3������ϡ���ᣬҲ�����ڴ���(����)
(2013·������ۣ�5B)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵������ȷ����(����)
A��Kspֻ�����ܵ���ʵ����ʺ��¶��й�
B������Ksp(ZnS)��Ksp(CuS)������ZnS��һ�������¿�ת��ΪCuS
C�������������䣬����Ũ�ȸı�ʱ��Ksp����
D���������ܵ�������Ƚ�ʱ��KspԽС�ĵ���ʣ����ܽ��һ��ԽС
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��(38Sr)Ԫ�ع㷺�����ڿ�Ȫˮ�У���һ������������Ԫ�أ���Ԫ�����ڱ�����20Ca��56Baͬ���ڵڢ�A�塣
(1)���ԣ�Sr(OH)2____Ba(OH)2(�>����<��)���ȵĻ�ѧ������ƺͱ����ƣ���ԭ�ӽṹ�Ĺ۵������ԭ����______________��
(2)̼����������Ҫ���Ȼ�����ú�SrSO4������BaSO4��BaCO3��FeO��Fe2O3��Al2O3��SiO2������ʯ�Ʊ�SrCO3��������������(���ֲ�����������)��
��.������ʯ��ۺ�Na2CO3��Һ��ֻ�ϣ����ˣ�
��.�������������ᣬ���ˣ�
��.���������Һ�м���Ũ���ᣬ���ˣ�
��.���������Һ���ȼ�������ᣬ��ַ�Ӧ�����ð�ˮ��pHԼΪ7�����ˣ�
��.���������Һ�м����Թ���NH4HCO3����ַ�Ӧ���ˣ�������ϴ������ɣ��õ�SrCO3��
��֪��ⅰ.��ͬ�¶�ʱ���ܽ�ȣ�BaSO4<SrCO3<SrSO4<CaSO4
ⅱ.�����������������pH
| ���� | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| ��ʼ����pH | 1.9 | 7.0 | 3.4 |
| ��ȫ����pH | 3.2 | 9.0 | 4.7 |
�٢��У���Ӧ�Ļ�ѧ����ʽ��_________________________________________��
�ڢ��У��������ᷴӦ�ܽ��������_________________________________��
�ۢ���Ŀ����_________________________________________________________��
�����й��ڸù������̵�˵����ȷ����________(����ĸ)��
a���ù��ղ����ķ�Һ���϶��NH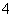 ��Na����Cl����SO
��Na����Cl����SO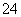
b�����з�Ӧʱ�������¶�һ���������SrCO3����������
c�����з�Ӧʱ��������Һһ���������NH4HCO3��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
(һ)ʵ�鷽���ⶨ��Ӧ��---------�к��Ȳⶨ
��1��ʵ�����ϱ����ձ�����С�����ձ�������ĭ���ϡ���ĭ���ϰ塢��ͷ�ιܡ����β�������0.5mol�� L-1 ���ᡢ0.55mol�� L-1NaOH��Һ����ȱ�ٵ�ʵ�鲣����Ʒ�� �� ��
| ʵ �� �� Ʒ | �� Һ �� �� | �к��ȡ�H | |||
| t1 | t2 | ||||
| �� | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20�� | 23.3�� | |
| �� | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20�� | 23.5�� |
��2�����Ǽ�¼��ʵ���������£�
��֪��Q=Cm(t2 -t1)����Ӧ����Һ�ı�����CΪ4.18KJ����-1�� Kg-1�������ʵ��ܶȾ�Ϊ1g��cm-3��
��������ϱ�����H=
��3��ij�о�С�齫V1 mL 1.0 mol/L HCl��Һ��V2 mLδ֪Ũ�ȵ�NaOH��Һ��Ͼ��Ⱥ��������¼��Һ�¶ȣ�ʵ��������ͼ��ʾ(ʵ����ʼ�ձ���V1��V2��50 mL)���ش��������⣺
�о�С������ʵ��ʱ�����¶� (����ڡ��������ڡ����ڡ�)22 �棬�˷�Ӧ����NaOH��Һ��Ũ��ӦΪ mol/L��
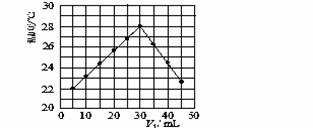
������ͨ����ѧ�����ӻ��
��1����֪��1mol��H��H����I��I��H��I���ֱ���Ҫ���յ�����Ϊ436kJ��153kJ��299kJ��
��ӦH2(g)��I2(g)��2HI(g)�ķ�Ӧ�ȡ�H�� kJ��mol��1
��2����֪��2H2(g)+ O2(g) �� 2H2O (l) ��H����571.6 kJ��mol��1
H2(g)+1/2O2(g) �� H2O(g) ��H����241.8 kJ��mol��1
����������Ӧȷ����H2ȼ����Ϊ kJ��mol��1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
֤������������Ԫ�صĴ��ڣ������м���������ȷ�IJ���˳����________(�����)��
�ټ�����������Һ���ڼ�������������Һ���ۼ��ȡ��ܼ�������ˮ���ݼ���ϡ��������Һ�����ԡ������������ƴ���Һ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com