
氯气常用于自来水厂杀菌消毒。
(1)工业上用铁电极和石墨做为电极电解饱和食盐水生产氯气,铁电极作 极,石墨电极上的电极反应式为 。
(2)氯氧化法是在碱性条件下,用Cl2将废水中的CN-氧化成无毒的N2和CO2。该反应的离子方程式为 。
(3)氯胺(NH2Cl)消毒法是在用液氯处理自来水的同时通入少量氨气,发生反应:Cl2 + NH3 === NH2Cl + HCl,生成的NH2Cl比HClO稳定,且能部分水解重新生成HClO,起到消毒杀菌的作用。
①氯胺能消毒杀菌的原因是 (用化学用语表示)。
②氯胺消毒法处理后的水中,氮元素多以NH4+的形式存在。
已知:NH4+(aq) + 1.5O2(g)=== NO2-(aq) + 2H+(aq) + H2O (l) ΔH=-273 kJ·mol-1
NH4+(aq) + 2O2(g)=== NO3-(aq) + 2H+(aq) + H2O (l) ΔH =-346 kJ·mol-1
NO2-(aq)被O2氧化成NO3-(aq)的热化学方程式为 。
(4)在水产养殖中,可以用Na2S2O3将水中残余的微量Cl2除去,某实验小组利用下图所示装置和药品制备Na2S2O3。

|
结合上述资料回答:
① 开始通SO2时,在B口检测到有新的气体生成,判断从B口排出的气体中是否含有H2S,并写出判断依据 。
② 为获得较多的Na2S2O3,当溶液的pH接近7时,应立即停止通入SO2,其原因 是 。
(1)阴 2Cl- - 2e- === Cl2↑
(2)5Cl2 + 2CN- + 4H2O === 10Cl- + N2↑+ 2CO2↑+ 8H +
(3)① NH2Cl + H2O  NH3 + HClO(不写可逆号扣1分)
NH3 + HClO(不写可逆号扣1分)
② 2NO2- (aq) + O2(g) === 2NO3-(aq) ΔH = -146 kJ·mol-1(反应热写错扣1分)
(4)①答案1:含H2S,由电离常数知H2SO3酸性强于H2S,溶液中的S2-与H2SO3反应生成H2S。
答案2:不含H2S,S2-还原性较强,能被SO2氧化生成其它含硫物质。
(只写“含”或“不含”为0分)
②通入过多SO2会使溶液的pH小于7,S2O32-在酸性溶液中不能稳定存在。


科目:高中化学 来源: 题型:
在反应3S+6KOH 加热 K2SO3+2K2S+3H2O中,还原剂和氧化剂的物质的量比为( )
A.1 :1 B.2 :1 C.1 :2 D.3 :2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质漂白的叙述中正确的是( )
A.氯水中通入一定量二氧化硫气体可增强氯水的漂白性
B.含有酚酞的氢氧化钠溶液中通入二氧化硫气体,溶液变无色,说明二氧化硫具有漂白性
C.漂白粉是混合物,其有效成分是次氯酸钙,漂白精是纯净物,其成分也是次氯酸钙
D.漂白粉放入稀酸中可以提高漂白速度
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醇可作为燃料电池的原料。通过下列反应可以制备甲醇:
 CO ( g ) + 2H2 ( g )
CO ( g ) + 2H2 ( g )  CH3OH ( g ) △H =-90.8 kJ·mol-1 在一容积可变的密闭容器中充入10 mol CO 和20 molH2,CO 的平衡转化率随温度(T)、压强(P)的变化如右图所示,当达到平衡状态A 时,容器的体积为20 L。
CH3OH ( g ) △H =-90.8 kJ·mol-1 在一容积可变的密闭容器中充入10 mol CO 和20 molH2,CO 的平衡转化率随温度(T)、压强(P)的变化如右图所示,当达到平衡状态A 时,容器的体积为20 L。
(1)该反应的化学平衡常数表达式为 ▲ 。
(2)如反应开始时仍充入10mol CO 和20mol H2,则在平衡状态B时容器的体积V(B)= ▲ L。
(3)关于反应CO(g)+2H2(g) CH3OH(g)在化学平衡状态时的描述正确的是 ▲ (填字母)。
CH3OH(g)在化学平衡状态时的描述正确的是 ▲ (填字母)。
A.CO的含量保持不变 B.容器中CH3OH浓度与CO浓度相等
C.2V正(CH3OH)=V正(H2)D.容器中混合气体的平均相对分子质量保持不变
(4)CO(g)+2H2(g) CH3OH(g),按照相同的物质的量
CH3OH(g),按照相同的物质的量
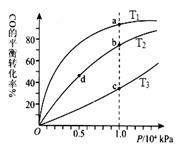 投料,测得CO在不同温度下的平衡转化率与压强的
投料,测得CO在不同温度下的平衡转化率与压强的
关系如右图所示。下列说法正确的是 ▲
A.温度:T1 < T2 <T3
B.正反应速率:ν(a)>ν(c); ν(b)>ν(d)
C.平衡常数: K(a) =K(c) ; K(b) >K(d)
D.平均摩尔质量:M(a)<M(c); M(b)>M(d)
(5)已知CO2(g)+H2(g) CO(g)+H2O(g) △H= + 41.3 kJ·mol-1 ,试写出由
CO(g)+H2O(g) △H= + 41.3 kJ·mol-1 ,试写出由
CO2和H2制取甲醇的热化学方程式 ▲ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,用 0.01 mol·L-1 NaOH溶液滴定 20.00 mL 0.01 mol·L-1 CH3COOH溶液,所得滴定曲线如右图。下列说法正确的是
A.a点对应溶液的pH=2
B.b点对应的溶液中:
c(OH-)+ c(CH3COO-) = c(Na+)+ c(H+)
C.c点表示NaOH溶液与CH3COOH溶液恰好完全反应
D.d点对应的溶液中,水的电离程度小于同温下纯水的电离程度
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关热化学方程式的叙述正确的是
A.已知甲烷的燃烧热为890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为
CH4(g)+2O2(g) ====2CO2(g)+2H2O(g) ΔH = - 890.3 kJ·mol-1
B.已知C(石墨,s)====C(金刚石,s) ΔH >0, 则金刚石比石墨稳定
C.已知中和热为ΔH =-57.4 kJ·mol-1,则1mol稀硫酸和足量稀NaOH溶液反应的反应热就是中和热
D.已知S(g)+O2(g) ==== SO2(g) ΔH1; S(s)+O2(g) ==== SO2(g) ΔH2, 则ΔH1﹤ΔH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【化学——选修化学与技术】
铝生产产业链由铝土矿开采、氧化铝制取、铝的冶炼和铝材加工等环节构成。请回答下列问题:
(1)工业上采用电解氧化铝-冰晶石(Na3AlF6)熔融体的方法冶炼得到金属铝:
2Al2O3  4Al+3O2↑加入冰晶石的作用:_______________________________。
4Al+3O2↑加入冰晶石的作用:_______________________________。
(2)上述工艺所得铝材中往往含有少量Fe和Si等杂质,可用电解方法进一步提纯,该电解池中阳极的电极反应式为 ,下列可作阴极材料的是________________。
A.铝材 B.石墨 C.铅板 D.纯铝
 (3)阳极氧化能使金属表面生成
(3)阳极氧化能使金属表面生成
致密的氧化膜。以稀硫酸为电解液,铝
阳极发生的电极反应式为
__________________________________。
(4)在铝阳极氧化过程中,需要不断
地调整电压,理由是____________ ___
。
(5)下列说法正确的是 。
A. 阳极氧化是应用原电池原理进行金属材料表面处理的技术
B. 铝的阳极氧化可增强铝表面的绝缘性能
C. 铝的阳极氧化可提高金属铝及其合金的耐腐蚀性,但耐磨性下降
D. 铝的阳极氧化膜富有多孔性,具有很强的吸附性能,能吸附染料而呈各种颜色
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对非金属元素(除稀有气体元素外)的相关判断正确的是
①非金属元素都是主族元素
②单质在反应中都只能作氧化剂
③氢化物常温下都是气态,所以都叫气态氢化物
④氧化物常温下都可以与水反应生成酸
⑤非金属元素R所形成的含氧酸盐(MaROb)中的R元素必定呈现正价
⑥氧化物都能与碱反应生成盐和水
A.①⑤ B.①⑤⑥ C.②④⑥ D.③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机化合物仅由碳、氢、氧三种元素组成 ,经测定其相对分子质量为90 。称取该有机物样品1.8 g ,在足量纯氧中完全燃烧 ,将产物先后通过浓硫酸和碱石灰 ,两者分别增重1.08 g和2.64 g 。
(1)通过计算得出该有机化合物的分子式为 (简要写出计算过程 )
(2)经过红外光谱分析得知该分子中存在C=O C-O C-H 等化学键,且核磁共振氢谱中只有一组峰,该有机物的结构简式为
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com