
| A. | 3 mol | B. | 1.5 mol | C. | 0.75 mol | D. | 0.6 mol |
科目:高中化学 来源: 题型:选择题
| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | .硅酸三钙 | B. | .碳酸二钙 | C. | 铝酸三钙 | D. | .碳酸钙 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1,2-二溴乙烷和1,1-二氯丙烷 | B. | 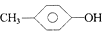 和 和 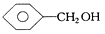 | ||
| C. | 苯 和 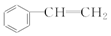 | D. | 丙炔 和 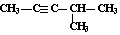 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验事实 | 结论 |
| A | 二氧化硅可以和NaOH溶液及HF溶液反应 | 二氧化硅属于两性氧化物 |
| B | 二氧化硫能漂白有色布料 | 二氧化硫具有强氧化性 |
| C | 向饱和Na2CO3溶液中通入足量CO2,溶液变浑浊 | 析出了NaHCO3 |
| D | 铝箔在酒精灯火焰上加热熔化但不滴落 | 铝的熔点高 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4L、0.5mol/L NaCl溶液 | B. | 1L、0.3mol/L Na2SO4溶液 | ||
| C. | 5L、0.4 mol/L NaOH溶液 | D. | 2L、0.15 mol/L、Na3PO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ②③④ | C. | ①③④⑤ | D. | ①②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 易溶于水的电解质一定是强电解质 | |
| B. | 强电解质在水溶液中以离子形式存在 | |
| C. | 难溶于水的电解质一定是弱电解质 | |
| D. | 强电解质溶液的导电性一定比弱电解质强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com