
| A. | 探究Na与水的反应可能有O2生成 | |
| B. | 探究SO2和Na2O2反应可能有Na2SO4生成 | |
| C. | 探究足量的铜与一定量的浓硝酸反应的气体产物是NO还是NO2 | |
| D. | 探究向滴有酚酞试液的NaOH溶液中通入Cl2,酚酞红色褪去的现象是溶液的酸碱性改变所致,还是HClO的漂白性所致 |
分析 A.同一氧化还原反应中有得电子的元素也有失电子的元素;
B.二氧化硫具有还原性、过氧化钠具有氧化性;
C.浓硝酸和Cu反应生成二氧化氮、稀硝酸和Cu反应生成NO;
D.氯气没有漂白性,次氯酸或次氯酸钠具有漂白性,碱性溶液能使酚酞试液变红色.
解答 解:A.根据质量守恒定律,化学反应前后元素的种类不变,钠和水中含有钠元素、氢元素和氧元素,猜测产生的气体可能为氧气,不符合氧化还原反应的基本规律,钠是还原剂,水只能做氧化剂,元素化合价需要降低,氧元素已是最低价-2价,不可能再降低,故A选;
B.二氧化硫具有还原性,过氧化钠具有氧化性,所以可以探究SO2和Na2O2反应可能有Na2SO4生成,故B不选;
C.铜与一定量的浓硝酸反应,硝酸作氧化剂,化合价降低,气体产物是NO还是NO2,有意义,故C不选;
D.氯气和氢氧化钠反应生成氯化钠次氯酸钠和水,消耗氢氧化钠溶液红色褪去,氯气可以与水反应生成的次氯酸或生成的次氯酸钠水解生成次氯酸具有漂白性,有探究意义,故D不选;
故选A.
点评 本题考查化学实验方案评价,为高频考点,涉及物质性质、氧化还原反应等知识点,明确实验原理及物质性质差异性是解本题关键,题目难度不大.


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:解答题
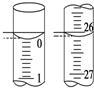 某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂.请填写下列空白:
某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂.请填写下列空白:| 滴定次数 | 待测NaOH溶液的体积/mL | 0.100 0 mol•L-1盐酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
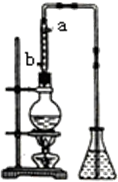 市售乙醛通常为40%左右的乙醛溶液.久置的乙醛溶液会产生分层现象,上层为无色油状液体,下层为水溶液.据测定,上层物质为乙醛的加合物(C2H4O)n,它的沸点比水的沸点高,分子中无醛基.乙醛在溶液中易被氧化,为从变质的乙醛溶液中提取乙醛(仍得到溶液),可利用如下反应原理:(C2H4O)n$\stackrel{H+}{→}$n(C2H4O).
市售乙醛通常为40%左右的乙醛溶液.久置的乙醛溶液会产生分层现象,上层为无色油状液体,下层为水溶液.据测定,上层物质为乙醛的加合物(C2H4O)n,它的沸点比水的沸点高,分子中无醛基.乙醛在溶液中易被氧化,为从变质的乙醛溶液中提取乙醛(仍得到溶液),可利用如下反应原理:(C2H4O)n$\stackrel{H+}{→}$n(C2H4O).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某氮肥硫酸铵中混有硫酸氢铵.为测定该氮肥的含氮量,一化学研究性学习小组取一定量氮肥样品,研磨使其混合均匀,备用.已知:
某氮肥硫酸铵中混有硫酸氢铵.为测定该氮肥的含氮量,一化学研究性学习小组取一定量氮肥样品,研磨使其混合均匀,备用.已知:| 氢氧化钠溶液体积/mL | 40.00mL | ||
| 样品质量/g | 7.750 | 15.50 | 23.25 |
| 氨气质量/g | 1.870 | 1.870 | 1.700 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
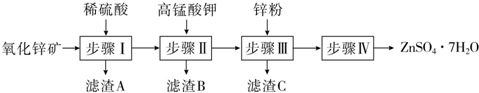
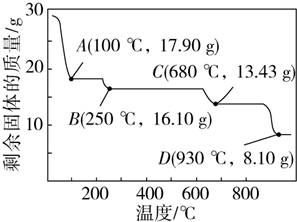
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A.秦朝铜车马 | B.春秋越王剑 | C.唐三彩 | D.商代司母戊鼎 |
 |  |  |  |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硫、二氧化氮、一氧化碳和二氧化碳是空气质量报告中涉及的主要污染物 | |
| B. | 正常雨水的pH等于7 | |
| C. | 二氧化硫和二氧化氮是引起酸雨的主要气体 | |
| D. | 家用汽车有利于人们出行,需要大力推广应用 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com