
| 充电 |
| 放电 |


 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案科目:高中化学 来源: 题型:
| A、铁元素在反应①和③中均被氧化 |
| B、Fe2+在氧化还原反应中只能做还原剂 |
| C、还原性强弱顺序为:I->Br->Fe2+>Cl- |
| D、反应③中当有2molFe3+ 被还原时,有2mol I-被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、质量数为37的氯原子:
| ||
B、二氧化碳分子的比例模型: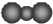 | ||
C、NH4Br的电子式: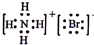 | ||
D、对羟基苯甲醛的结构简式: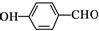 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2CO3溶液中:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+) |
| B、将pH=a的醋酸稀释为pH=a+1的过程中,c(OH-)不断增大 |
| C、等体积pH=a的醋酸与pH=b的NaOH溶液恰好中和时,a+b=14 |
| D、浓度均为0.1 mol-1的CH3COOH溶液和氨水等体积混合后:c(CH3COO-)+c(OH-)=c(NH4+)+c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| X | Y | |
| Z | W |
| A、原子半径:W>Z>Y>X |
| B、最高价氧化物对应水化物的酸性:Z>W>X |
| C、气态氢化物的沸点:Y>Z |
| D、四种元素的单质中,W单质的熔、沸点最高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、10 mL 0.2mol?L-1MgCl2溶液 |
| B、20 mL 0.5 mol?L-1 AgNO3溶液 |
| C、40 mL 0.3mol?L-1HCl溶液 |
| D、15 mL 0.1mol?L-1 AlCl3溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com