
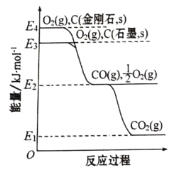
【题目】金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时充分燃烧生成二氧化碳,反应的能量变化如图所示。下列说法正确的是
A.在通常状况下,金刚石比石墨更稳定
B.石墨的燃烧热为![]()
C.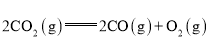
![]()
D.12g石墨在一定量的空气中燃烧,生成气体产物36g,该过程放出的热量为![]()
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数,下列说法中正确的是( )
A.54g H2O中含有3NA个氢原子
B.1mol Na2SO4溶于水中,所得溶液中Na+个数为NA
C.标准状况下,NA个H2O分子所占的体积约为22.4L
D.1mol CO2和NO2的混合物中含的氧原子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】200mL Fe2(SO4)3溶液中含Fe3+56g,在该溶液中加入1mol/LBaCl2溶液300mL,反应后溶液中SO42-的物质的量浓度是(忽略混合后溶液的体积变化) ( )
A.7.5mol/LB.5mol/LC.6mol/LD.2.4mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物X的结构简式如图所示,下列关于X的说法不正确的是
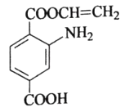
A.X分子中含有四种官能团
B.X能与金属钠反应,且相同条件下比水与金属钠反应要剧烈
C.1molX最多与5mol氢气发生加成反应
D.在一定条件下,X能发生加成、取代、加聚、缩聚、氧化、还原等反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请回答下列问题:
(1)取有机物A 3.0 g,完全燃烧后生成3.6 g水和3.36 L CO2(标准状况)。已知该有机物的蒸气对氢气的相对密度为30,则该有机物的分子式是___________。若该物质能与Na反应,则其所有可能的结构名称分别是_______________________,其中有一种结构能发生催化氧化并生成丙醛(CH3CH2CHO),请写出该反应的化学方程式:_________________________________________。
(2)链烃A有支链且只有一个官能团,其相对分子质量68,则A的结构简式是___________________,名称是_________________________。
(3)某有机物的分子结构为:![]() ,该分子中最多可以有______个原子共平面。
,该分子中最多可以有______个原子共平面。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求写出下列化学方程式:
(1)实验室可以用KClO3和浓盐酸反应制取氯气,写出发生反应的化学方程式并用双线桥表示电子转移方向和数目_____________。
(2)二氧化氯(ClO2)作为一种高效强氧化剂,可用KClO3和草酸(H2C2O4),稀硫酸,水浴加热制备。反应后产物中有ClO2、CO2和一种酸式盐,该反应的化学方程式为________________。
(3)写出工业上制备漂白粉的化学方程式___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温恒容条件下发生反应:2NO2(g)![]() N2O4(g),下列叙述能够标志该反应达到化学平衡状态的有
N2O4(g),下列叙述能够标志该反应达到化学平衡状态的有
①体系的压强不再改变 ②气体的颜色不再改变
③气体的平均摩尔质量不再改变 ④混合气体的密度不再改变
⑤各组分的体积分数不再改变 ⑥原子总数不再改变
⑦混合气体分子总数不再改变 ⑧c(NO2):c(N2O4)=2:1,且比值不再改变
⑨v(NO2)正=2v(N2O4)逆
A.①②③⑤⑦⑧⑨B.②③⑤⑦⑨C.④⑤⑥⑦D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环戊烯(![]() ,
,![]() )是一种重要的有机化工原料,可用环成二烯(
)是一种重要的有机化工原料,可用环成二烯(![]() ,
,![]() )制备。已知:
)制备。已知:
反应Ⅰ ![]()
![]()
反应Ⅱ ![]() (环戊烷)
(环戊烷) ![]()
反应Ⅲ ![]()
![]()
![]()
(1)某温度下,将环戊二烯和HI按物质的量之比1∶2(总物质的量为amol)充入容积为2L的恒容密闭容器中,发生反应:![]() 。
。
①该反应自发进行的条件是__________。
②下列有关该反应的叙述,不正确的是__________。
A.气体压强不变,说明反应达到平衡状态
B.升高温度,有利于提高环戊烯的产率
C.反应达到平衡时,C5H6和HI的转化率相等
D.通入惰性气体,有利于提高环戊二烯的平衡转化率
(2)以![]() 为催化剂,如图1为25℃时环戊二烯氢化过程,环戊烯与环戊烷的各组分含量(物质的量含量)随时间(t)的变化。为研究不同温度下催化剂活性,测得不同温度下反应4h时的转化率和选择性数据如图2(其它条件相同)。
为催化剂,如图1为25℃时环戊二烯氢化过程,环戊烯与环戊烷的各组分含量(物质的量含量)随时间(t)的变化。为研究不同温度下催化剂活性,测得不同温度下反应4h时的转化率和选择性数据如图2(其它条件相同)。

①环成二烯氢化制环成烯的最佳反应温度为__________,选择该温度的原因是__________。
②升高温度,环戊二烯转化率提高而环戊烯选择性降低,其原因是__________。
③在图1中画出40℃时环戊烯含量随t变化趋势的曲线。__________
(3)实际生产中,常由双环戊二烯通入水蒸气解聚成环戊二烯:

某温度,加入总压为70kPa的双环成二烯和水蒸气,达到平衡后总压为110kPa,双环戊二烯的转化率为80%,则该反应的平衡常数![]() __________(对于气相反应,用某组分B的平衡压强
__________(对于气相反应,用某组分B的平衡压强![]() 代替物质的量浓度
代替物质的量浓度![]() 也可表示平衡常数,记作
也可表示平衡常数,记作![]() )。
)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把4 mol X气体和6 mol Y气体混合于2 L密闭容器中,使它们发生如下反应:X(g)+2Y(g)=3Z(g)+nW(g),5 min末已生成3 mol Z,若测知以W的浓度变化来表示的反应速率为0.2 mol·L-1·min-1,下列选项正确的是( )
A.前5 min内用X的浓度变化表示的平均反应速率为0.5 mol·L-1·mol-1
B.5 min末时Y的浓度为2 mol·L-1
C.化学方程式中n=3
D.5 min末时W的物质的量为1 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com