

���� Aװ����C��Ũ���ᷢ��������ԭ��Ӧ����NO2����Ӧ����ʽΪC+4HNO3��Ũ��=CO2��+4NO2��+2H2O��NO2ͨ��B�к�ˮ������Ӧ3NO2+H2O=2HNO3+NO��Cu��ϡ���ᷢ����Ӧ3Cu+8HNO3=3CuNO3+2NO��+4H2O��C�з�����Ӧ 2NO+Na2O2=2NaNO2��ʣ���NO�����Ը��������Һ�����������ᣬ
��1��a�Ƿ�Һ©����NO�ж�����ֱ���ſգ�
��2��C��HNO3��Ũ��������Ӧ����CO2��NO2��H2O��
NO��Na2O2������Ӧ����NaNO2��
��3��a��A�����ɶ�����̼��������̼�������Ʒ�Ӧ����̼���ƣ�̼������ҺҲ�ʼ��ԣ�
b�����������ܺ�ϡ���ᷴӦ������ɫ����NO��NO���ȶ��ױ������������ɺ���ɫ�������������
��4���ٴ�Bװ���г����������к���NO��������̼��ˮ�������⼸�����ʶ��ܺ������Ʒ�Ӧ��ҪʹC��ֻ��NO�������Ʒ�Ӧ����BCװ�ü��Eװ��Ӧ��������ˮ�����Ͷ�����̼��
��Ҫ�ų�����������ֹ��Ӧ��Ӧ����ͨ��һ��ʱ��ĵ�����
��5�����ݵ��ӵ�ʧ�غ��֪�����������������أ����ԣ���Һ����������ԭ��Ӧ�Ĺ�ϵʽΪ5NaNO2��KMnO4���ɼ����1000g��ҹ������NaNO2�����������ݴ˼����ҹ������NaNO2�ĺ�����
��� �⣺Aװ����C��Ũ���ᷢ��������ԭ��Ӧ����NO2����Ӧ����ʽΪC+4HNO3��Ũ��=CO2��+4NO2��+2H2O��NO2ͨ��B�к�ˮ������Ӧ3NO2+H2O=2HNO3+NO��Cu��ϡ���ᷢ����Ӧ3Cu+8HNO3=3CuNO3+2NO��+4H2O��C�з�����Ӧ 2NO+Na2O2=2NaNO2��ʣ���NO�����Ը��������Һ�����������ᣬ
��1��a�����Ƿ�Һ©����NO�ж�����ֱ���ſգ�NO�����Ը��������Һ��Ӧ������������Ӻ������ӣ��Ӷ���ȥNO��
�ʴ�Ϊ����Һ©������ȥδ��Ӧ��NO����ֹ��Ⱦ������
��2��C��HNO3��Ũ��������Ӧ����CO2��NO2��H2O����Ӧ����ʽΪC+4HNO3��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CO2��+4NO2��+2H2O��NO��Na2O2������Ӧ����NaNO2����Ӧ����ʽΪ 2NO+Na2O2=2NaNO2��
�ʴ�Ϊ��C+4HNO3��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CO2��+4NO2��+2H2O��2NO+Na2O2=2NaNO2��
��3��a��A�����ɶ�����̼��������̼�������Ʒ�Ӧ����̼���ƣ�̼������ҺҲ�ʼ��ԣ�B�г����������л�����ˮ�����ܺ�C�еĹ������Ʒ�Ӧ����NaOH���ʼ��ԣ����Բ��ܸ�����ˮ��Һ�жϺ����������ƣ���a����
b�����������ܺ�ϡ���ᷴӦ������ɫ����NO��NO���ȶ��ױ������������ɺ���ɫ���������������ʵ������˵�������������ƣ���b��ȷ��
��ѡb��
��4���ٴ�Bװ���г����������к���NO��������̼��ˮ�������⼸�����ʶ��ܺ������Ʒ�Ӧ��ҪʹC��ֻ��NO�������Ʒ�Ӧ����BCװ�ü��Eװ��Ӧ��������ˮ�����Ͷ�����̼��ʹ�õ�ҩƷ�Ǽ�ʯ�ң�
�ʴ�Ϊ����ʯ�ң�
��Ҫ�ų�������ֹ������Ӧ��Ӧ����ͨ��һ��ʱ��ĵ������ʴ�Ϊ�����ɼУ�ͨ��N2һ��ʱ�䣻
��5�����ݵ��ӵ�ʧ�غ��֪�����������������أ����ԣ���Һ����������ԭ��Ӧ�Ĺ�ϵʽΪ5NaNO2��2KMnO4���ɼ����1000g��ҹ������NaNO2������Ϊ2.5��0.00500mol/L��16.00mL��10-3��69=13.8mg�����Ը�ҹ������NaNO2�ĺ���Ϊ13.8mg/kg��
�ʴ�Ϊ��13.8��
���� ���⿼�������Ʊ���Ϊ��Ƶ���㣬�漰������ԭ��Ӧ�����ʼ��顢ʵ�������ʵ�����ۼ�����ʽ�����֪ʶ�㣬��ȷ��ѧ��Ӧԭ����ʵ����������������������ʲ������ǽⱾ��ؼ���ע��ʵ��������Է����жϣ���Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
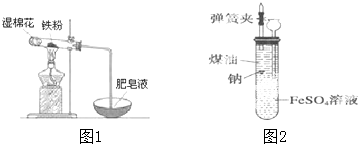 �����ճ���������;��㡢�������Ľ������ϣ�
�����ճ���������;��㡢�������Ľ������ϣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
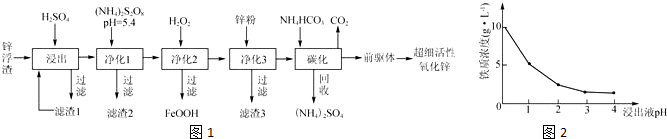
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
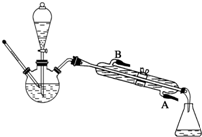 ��֪������Ҵ���Ũ������»ᷢ�����з�Ӧ��
��֪������Ҵ���Ũ������»ᷢ�����з�Ӧ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��֪�¶�Tʱˮ�����ӻ�����ΪKw�����¶��£���Ũ��Ϊa mol•L-1��һԪ��HA��b mol•L-1��һԪ��BOH�������ϣ������Һ�е�c��H+��=$\sqrt{{k}_{W}}$ mol•L-1ʱ���ж�����Һ������ | |
| B�� | pH=5��H2SO4��Һ����ˮϡ�͵�500������ϡ�ͺ�c��H+����c��SO42-���ı�Ϊ2��1 | |
| C�� | ij�¶��£�ˮ�����ӻ�����Kw=10-12�����¶��£���pH=4��H2SO4��Һ��pH=9��NaOH��Һ��ϲ����ֺ��£���ʹ�����Һ��pH=7����ϡ������NaOH��Һ�������Ϊ9��1 | |
| D�� | ��pH=1������ƽ���ֳ����ݣ�һ�ݼ�������ˮ����һ�ݼ�������������ʵ���Ũ����ͬ������NaOH��Һ��pH��������1��������ˮ��NaOH��Һ�������Ϊ11��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Fe2��SO4��3�T2Fe3++3SO42- | B�� | KClO3�TK++Cl-+O32- | ||
| C�� | KAl��SO4��2�TK++Al3++2SO42- | D�� | NaHSO4�TNa++H++SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
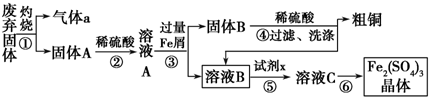
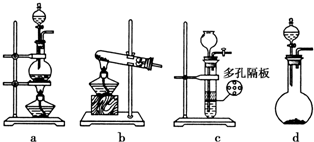
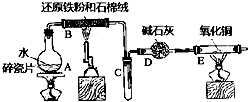 ijʵ��С��������ͼ����װ�ý��С�����ˮ������Ӧ����ʵ�飬�����ò����һ����ȡFeCl3•6H2O���壮��ͼ�мгּ�β������װ�þ�����ȥ��
ijʵ��С��������ͼ����װ�ý��С�����ˮ������Ӧ����ʵ�飬�����ò����һ����ȡFeCl3•6H2O���壮��ͼ�мгּ�β������װ�þ�����ȥ���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com