
【题目】钛呈银白色,因它坚硬、强度大、耐热、密度小,被称为高技术金属。目前生产钛采用氯化法,即将金红石或钛铁矿与焦炭混合,通入氯气并加热制得TiCl4:
2FeTiO3+7Cl2+6C![]() 2TiCl4+2FeCl3+6CO; TiO2+2Cl2+2C
2TiCl4+2FeCl3+6CO; TiO2+2Cl2+2C![]() TiCl4+2CO
TiCl4+2CO
将TiCl4蒸馏并提纯,在氩气保护下与镁共热得到钛:TiCl4+2Mg![]() Ti+2MgCl2
Ti+2MgCl2
MgCl2和过量Mg用稀盐酸溶解后得海绵状钛,再在真空熔化铸成钛锭。请回答下列问题:
(1)基态钛原子的价电子排布式为__________________。
(2)与CO互为等电子体的离子为__________(填化学式)。
(3)在CH2Cl2、C6H6、CO2、C2H4中,碳原子采取sp杂化的分子有__________ 。
(4) C60用做比金属及其合金更为有效的新型吸氢材料,其分子结构中每一个C原子皆为SP2杂化,含多个σ键和π键,36gC60最多可以吸收标准状况下的氢气____________L。
(5)与钛同周期的另一种元素钴(Co)可形成分子式均为Co(NH3)5BrSO4的两种配合物,其中一种化学式为[Co(NH3)5Br]SO4,往其溶液中加BaCl2溶液时,现象是__________________ ;往另一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则第二种配合物的化学式为 _______________ 。
(6)在自然界中TiO2有金红石、板钛矿、锐钛矿三种晶型,其中金红石的晶胞如下图所示,则其中Ti4+的配位数为__________。

【答案】(1)3d24s2(2) CN-(或NO+、C22-) CO2(4)分子
(5)产生白色沉淀 [Co (NH3)5SO4]Br(6) 6
【解析】试题分析:(1)钛为22号元素,基态电子排布式为:[Ar]3d24s2,则基态钛原子的价电子排布式为3d24s2;
(2)CO为双原子分子,价电子总数为10,则CO的等电子体为离子的为:CN-(或NO+.C22-);
(3)在CH2Cl2、C6H6、CO2、C2H4中,分子构型分别为四面体形、平面正六边形、直线形、平面形,所以碳原子的杂化方式分别为sp3、sp2、sp、sp2杂化,采取sp杂化的分子有CO2;
(4)因TiCl4在常温下是无色液体,说明熔点低,在水或潮湿空气中易水解而冒白烟,说明钛离子为弱碱阳离子,由此可判断 TiCl4是由共价键结合的分子,晶体类型属于分子晶体;
(5)由[Co(NH3)5Br]SO4可知,硫酸根离子为配合物的外界,在水溶液中以离子形式存在,所以会与钡离子结合成白色沉淀.加入BaCl2溶液时,无明显现象,说明硫酸根离子在内界,若加入AgNO3溶液时,产生淡黄色沉淀,说明溴离子在外界,因此另一配合物的化学式为[Co (NH3)5SO4]Br;
(6)观察晶胞结构,可知每个钛周围距离最近的氧原子有6个,即钛的配位数为6。


科目:高中化学 来源: 题型:
【题目】把主族元素X的最高价氧化物X2O4.7g溶于95.3g水中,得到溶质质量分数为5.6%的溶液,Y与X位于同一族,12gY的氢氧化物与400mL 0.75mol/L的盐酸完全中和,Z与Y同周期,标准状况下5.6 LZO2为16g。
(1)求X、Y、Z的相对原子质量;
(2)写出其元素符号。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2A+B![]() 3C十5D反应中,表示该反应速率最快的是
3C十5D反应中,表示该反应速率最快的是
A.v(A)= 0.5 mol/(L·s) B.v(B)= 0.3 mol/(L·s)
C.v(C)= 0.8 mol/(L·s) D.v(D)= 60 mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属锂是密度最小的金属,等质量的金属锂能释放出更多的电子,故常用来制高能量电池,已知锂的金属性介于钠和镁之间,则下列能冶炼出金属锂的方法是
A.电解法 B.热还原法 C.热分解法 D.铝热法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知热化学方程式:2SO2(g)+O2(g) ![]() 2SO3(g)ΔH=-Q kJ·mol-1(Q>0)。下列说法正确的是
2SO3(g)ΔH=-Q kJ·mol-1(Q>0)。下列说法正确的是
A.相同条件下,2 mol SO2(g)和1 mol O2(g)所具有的能量小于2 mol SO3(g)所具有的能量
B.2 mol SO2(g)和1 mol O2(g)在密闭容器中充分反应,放出热量小于Q kJ
C.增大压强或升高温度,该反应过程都能放出更多的热量
D.2 mol SO2(g)和1 mol O2(g)在密闭容器中充分反应,放出热量等于Q kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常见的一硝基甲苯有对硝基甲苯和邻硝基甲苯两种,均可用于合成各种染料。某探究小组利用下列反应和装置制备一硝基甲苯。
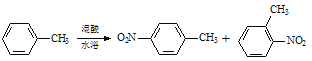
实验中可能用到的数据:
密度/gcm-3 | 沸点/ ℃ | 溶解性 | |
甲苯 | 0.866 | 110.6 | 不溶于水,易溶于硝基甲苯 |
对硝基甲苯 | 1.286 | 237.7 | 不溶于水,易溶于液态烃 |
邻硝基甲苯 | 1.162 | 222 | 不溶于水,易溶于液态烃 |
实验步骤:①浓硫酸与浓硝酸按体积比1:3配制混合溶液(即混酸)共40 mL;
②在三颈瓶中加入13g甲苯(易挥发),按图所示装好药品和其他仪器;
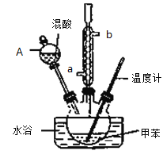
③向三颈瓶中加入混酸;
④控制水浴温度约为50℃,反应大约10 min,三颈瓶底有大量淡黄色油状液体出现;
⑤分离出一硝基甲苯,经提纯最终得到纯净的一硝基甲苯共15 g。
请回答下列问题:
(1)实验前需要在三颈瓶中加入少许 ,目的是 。
(2)冷凝管的作用是 ;冷却水从冷凝管的_______(填“a”或“b”)端进入。
(3)仪器A的名称是 ,使用该仪器前必须进行的操作是_________________。
(4)分离反应后产物的方案如下:

其中,操作1的名称为 ,操作2必需的玻璃仪器有酒精灯、温度计、锥形瓶、牛角管(尾接管)和 、 。
(5)该实验中一硝基甲苯的产率为 (保留三位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学常见反应的化学方程式有A+B→X+Y+H2O或H2O+A+B→X+Y(未配平,反应条件略去),下列问题所涉及反应是上述两个方程式之一。请回答:
(1)常温下,若A为黄绿色气体,B为非金属氧化物,A、B均能使品红溶液褪色,A+B+H2O→X+Y,且相对分子质量X>Y,则该反应的化学方程式________,检验Y中阴离子的试剂是__________。
(2)若A为常见的金属单质,Y为气态单质,B溶液呈强酸性或强碱性时,A和B反应都能进行。写出A与B反应的离子方程式: ; 。
(3)若A为常见的非金属单质,它是构成有机物的基本元素之一,B的溶液为某浓酸,其中A、B的物质的量之比为1∶4,则该反应化学方程式为 。
(4)若A、B均为化合物,Y为白色沉淀(不含金属元素),B为引起温室效应的主要气体,写出A与B反应生成Y的离子方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com