
��ĩ״����A���ɵ����ʵ�����MgO��Fe2O3��ɵĻ�����������ʵ�飺
��ȡ����A�������ȷ�Ӧ���������е���B���ɣ�
����ȡ20 g Aȫ������0.15 L 6.0 mol��L��1�����У�����ҺC��
�۽����еõ��ĵ���B����ҺC��Ӧ���ų�1.12 L(���)���壬ͬʱ������ҺD���������й�������B��
����KSCN��Һ����ʱ����ҺD����ɫ��
����գ�
��1�� �����������ȷ�Ӧ��ʵ�������_____________�������еĵ���B��_____________��
�����������ȷ�Ӧ��ʵ�������_____________�������еĵ���B��_____________��
��2�������������ĸ���Ӧ�Ļ�ѧ����ʽ��_______________________��
��3�������������ĸ���Ӧ�����ӷ���ʽ��_________________________��
��4������ҺD���������Ϊ0.15 L�������Һ��c(Mg2+)Ϊ__________��c(Fe2+)Ϊ__________��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
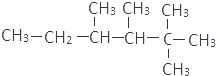 ��ij��ϩ���������ӳɺ�IJ�����ϩ��������5�ֽṹ�������Ȳ���������ӳɵIJ�����Ȳ��������1�ֽṹ��
��ij��ϩ���������ӳɺ�IJ�����ϩ��������5�ֽṹ�������Ȳ���������ӳɵIJ�����Ȳ��������1�ֽṹ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �մ� | B�� | ��ͭ | C�� | ����ϩ | D�� | ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �¶ȡ�Ũ�ȡ�ѹǿ������ | B�� | �¶ȡ�Ũ�ȡ����� | ||
| C�� | �¶ȡ�Ũ�� | D�� | �¶� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
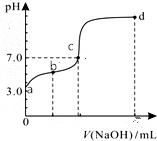 ��������20mL0.1mol/LHA��Һ����μ���0.1mol/LNaOH��Һ����pH�仯�����ͼ��ʾ�������¶ȱ仯��������˵���в���ȷ���ǣ�������
��������20mL0.1mol/LHA��Һ����μ���0.1mol/LNaOH��Һ����pH�仯�����ͼ��ʾ�������¶ȱ仯��������˵���в���ȷ���ǣ�������| A�� | �����֪HAΪ���� | |
| B�� | �ζ��յ�λ��c��d��֮�� | |
| C�� | �ζ���b��ʱ��n��Na+��+n��H+��-n��OH-��+n��HA��=0.002mol | |
| D�� | �ζ���d��ʱ��c��OH-����c��Na+����c��A-����c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ĸ����ϵڶ�����Ӧ�Կ��Ի�ѧ���������棩 ���ͣ�ѡ����
��һ�����ġ��������Ʒ����140 mL 5.0 mol��L��1����ǡ�ý�֮��ȫ�ܽ⣬������Һ��������0.025 mol Cl2��ǡ��ʹ���е�Fe2+ȫ��ת��ΪFe3+�������Ʒ���ܵĻ�ѧʽΪ( )
A��Fe2O3 B��Fe3O4 C��Fe4O5 D��Fe5O7
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ĸ����ϵڶ�����Ӧ�Կ��Ի�ѧ���������棩 ���ͣ�ѡ����
�����йؽ��������仯�����������ȷ����
A�����ڳ����²�����������Ӧ B����������������Ӧ
C�������������ᣬ�������ڼ� D��������ֻ�����ᷴӦ��������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�콭��ʡ�����ϵڶ����¿���ѧ�Ծ��������棩 ���ͣ�ʵ����
ijͬѧ�������ͼ��ʾװ���������ô�������ijŨ��ϡ���ᷴӦ��ȡNO���塣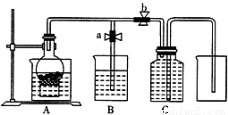
��1��������a���رտ���bʱ��A�и�����й۲쵽��ʵ�������� ���ձ�B��ʢ���� ��Һ���� ʱ�رտ���a������b����ʱC������ˮ���ռ�NO���塣��C����������رտ���b��װ��A�й۲쵽�������Ǣ� ���� ��
��2����a mol Fe�뺬b mol HNO3��ϡ��Һ��ַ�Ӧ��������Ļ�ԭ ����ֻ��NO�������۷����ձ�A�������Һ����Ҫ��������ɼ������ʵ���������������±�δ��ɵĿո��С�
����ֻ��NO�������۷����ձ�A�������Һ����Ҫ��������ɼ������ʵ���������������±�δ��ɵĿո��С�
a/bȡֵ��Χ | ������Һ�е���Ҫ�����Ӽ������ʵ��� |
<1/4 | |
=1/4 | a mol Fe3+ |
����1/4��3/8 | |
=3/8 | a mol Fe2+ |
>3/8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ | B�� | ��ˮ | C�� | ̼������Һ | D�� | ��̪�Լ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com