
根据砷元素的原子结构示意图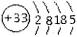 ,做出如下推理,其中与事实不符的是( )
,做出如下推理,其中与事实不符的是( )
A.砷元素位于元素周期的第四周期、第VA族
B.砷原子不如溴原子的得电子能力强
C.砷酸酸性比磷酸酸性强
D.在相同条件砷元素的氢化物的稳定性弱于氨气
科目:高中化学 来源:2015届山东省邹城市高三10月月考化学试卷(解析版) 题型:选择题
某化学兴趣小组在课外活动中,对某一份溶液成分(已知不含其他还原性离子)进行了检测,其中三次检测结果如下表所示
检测序号 | 溶液中检测出的离子组合 |
第一次 | KCl、K2SO4、Na2CO3、NaCl |
第二次 | KCl、AlCl3、Na2SO4、K2CO3 |
第三次 | Na2SO4、KCl、K2CO3、NaCl |
则下列说法合理的是
A.三次检测结果都正确
B.该溶液中的阳离子无法判断
C.为了检验SO42-,应先加过量稀硝酸后再滴加Ba(NO3)2,观察是否有沉淀现象
D.为了确定是否存在CO32-,可以向其中滴加CaCl2溶液,观察是否有沉淀现象
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三上学期第一次质量检测化学试卷(解析版) 题型:选择题
如图为含有同一种元素的a、b、c、d、e五种物质的转化关系。
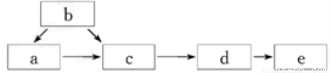
其中a是单质,b是气态氢化物,c、d是氧化物,e是该元素最高价氧化物对应的水化物,则a可能是( )
①C ②N2 ③S ④F2
A.只有①和③ B.只有④ C.①②③ D.①②③④
查看答案和解析>>
科目:高中化学 来源:2015届山东省聊城市高三上学期第一次阶段性测试化学试卷(解析版) 题型:选择题
将4.6 g Cu和Mg完全溶于浓硝酸溶液中,反应中硝酸的还原产物为4480mL NO2气和336 mL N2O4气体(标准状况下),反应后的溶液中,加入过量NaOH溶液,生成沉淀的质量为 ( )
A.9.02 g B.8.51 g C.8.26 g D.7.04 g
查看答案和解析>>
科目:高中化学 来源:2015届山东省聊城市高三上学期第一次阶段性测试化学试卷(解析版) 题型:选择题
下列各组反应最终有白色沉淀生成的是( )
①金属钠投入到FeCl2溶液中 ②过量NaOH溶液和AlCl3溶液混合
③少量Ca(OH)2投入NaHCO3溶液中 ④过量CO2通入NaAlO2溶液中
A.②③ B.③④ C.①③④ D.①②③④
查看答案和解析>>
科目:高中化学 来源:2015届山东省聊城市高三上学期第一次阶段性测试化学试卷(解析版) 题型:选择题
下列有关原子结构、元素性质的说法正确的是( )
A.ⅠA族元素的金属性一定比ⅡA族的金属性强
B.族序数等于周期序数的元素一定是金属元素
C.全部由非金属元素组成的化合物中只含共价键
D.13C和14C互为同位素,化学性质相似
查看答案和解析>>
科目:高中化学 来源:2015届山东省烟台市高三上学期期中考试化学试卷(解析版) 题型:填空题
(7分)实验证明,以下六种物质是一个氧化还原反应的反应物和生成物:NO、FeSO4、H2O、Fe(NO3)3、HNO3和Fe2(SO4)3。
(1)这六种物质中,反应物是____________;被还原的元素是____________。
(2)若该反应是恰好完全反应,且收集到NO的体积为4.48L(标况时),测得反应后溶液的体积为250mL。
反应过程中转移的电子数为___________;所得溶液中SO42-的物质的量浓度为________mol·L-1。
查看答案和解析>>
科目:高中化学 来源:2015届山东省潍坊市高三上学期期中考试化学试卷(解析版) 题型:填空题
(10分)空气吹出法工艺,是目前“海水提溴”的最主要方法之一。其工艺流程如下:

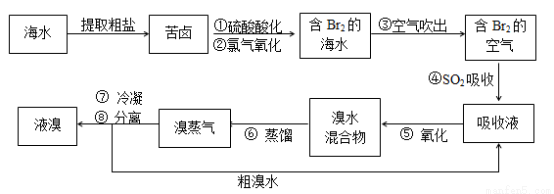
(1)步骤①中用硫酸酸化的目的是__ .步骤②发生反应的离子方程式为 。
(2)步骤④利用了SO2的还原性,反应的离子方程式:__________________________.
(3)步骤⑥的名称是 ____________ 。
(4)从含溴水中吹出的溴也可用纯碱吸收,纯碱吸收溴的主要反应是: 3Na2CO3+3Br2= NaBrO3+ 5NaBr+ 3CO2;吸收1mol Br2 时,转移的电子数为 mol。纯碱吸收后再用硫酸酸化,单质溴又从溶液中析出。
(5)化学上将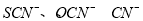 等离子称为“类卤离子”。现将KSCN溶液滴加到酸性
等离子称为“类卤离子”。现将KSCN溶液滴加到酸性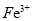 溶液中,溶液立即变成血红色;通入
溶液中,溶液立即变成血红色;通入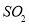 后,血红色消失。血红色消失过程中发生反应的离子方程式为 。
后,血红色消失。血红色消失过程中发生反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三10月阶段性考试化学试卷(解析版) 题型:填空题
(8分)铜合金是人类使用最早的金属材料,铜在化合物中的常见化合价有+l、+2。已知Cu2O与稀硫酸反应,溶液呈蓝色,同时溶液中还存在红色浑浊。现向Cu、Cu2O和CuO组成的混合物中,加入1 L 0.6 mol/L HNO3溶液恰好使混合物溶解,同时收集到2240 mL NO气体(标准状况)。
请回答下列问题:
(1)写出Cu2O跟稀硝酸反应的离子方程式 。
(2)若将上述混合物用足量的H2加热还原,所得到固体的质量为 。
(3)若混合物中含0.1 mol Cu,将该混合物与稀硫酸充分反应,消耗H2SO4的物质的量为 。
(4)若混合物中Cu的物质的量为n mol,则n的取值范围为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com