
| A. | 漂白粉的有效成分是CaCl2 | |
| B. | 漂白粉和明矾处理自来水的原理是相同的 | |
| C. | 漂白粉最好在弱酸性环境下使用 | |
| D. | 漂白粉因易在空气中氧化而密封保存 |
分析 A.漂白粉的有效成分是次氯酸钙;
B.明矾水解生成具有吸附性的氢氧化铝胶体,漂白粉具有强氧化性杀菌消毒;
C.漂白粉的漂白原理:次氯酸钙和弱酸性物质生成的次氯酸的漂白性,最好在弱酸性环境下使用;
D.漂白粉中的次氯酸钙能与空气中的水和二氧化碳反应而变质,不是被氧气氧化.
解答 解:A.漂白粉的主要成分是次氯酸钙和氯化钙,有效成分是次氯酸钙,即Ca(ClO)2,故A错误;
B.明矾水解生成具有吸附性的氢氧化铝胶体,不具有强氧化性,只能用于除去水的悬浮物,而漂白粉具有强氧化性杀菌消毒,故B错误;
C.漂白粉中含有Ca(ClO)2,易与空气中的水和二氧化碳反应Ca(ClO)2+2H2O+2CO2=Ca(HCO3)2+2HClO,生成HClO具有漂白性,所以漂白粉最好在弱酸性环境下使用,故C正确;
D.漂白粉因易易与空气中的水和二氧化碳反应生成不稳定的次氯酸而变质,需密封保存,不是因易在空气中氧化而密封保存,故D错误;
故选C.
点评 本题考查学生漂白粉的成分和漂白原理知识,可以根据教材知识来回答,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 钻木取火 | |
| B. | 青铜器生锈 | |
| C. | 焰色反应检验Na+ | |
| D. | 2015年9月3日,中国在抗日战争暨世界反法西斯战争胜利70周年之际,燃放烟花爆竹,举国欢庆 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 1mol/L | B. | 1.5mol/L | C. | 3mol/L | D. | 7mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
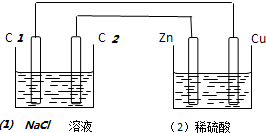
| A. | (1)中C2电极反应式为:2Cl--2e-═Cl2 | B. | (2)溶液中的SO42-向Cu极定向移动 | ||
| C. | (1)中滴入酚酞试液,C1极附近先变红 | D. | (2)中溶液的PH=1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
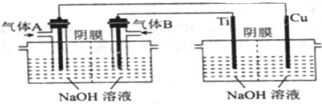 (1)工业上可利用CO2和H2生产甲醇,方程式如下:
(1)工业上可利用CO2和H2生产甲醇,方程式如下:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com