
下列实验操作中不正确的是( )
A.用容量瓶配制一定物质的量浓度的NaOH溶液时,溶解后的溶液要马上转移至容量瓶
B.蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口
C.蒸发结晶时当蒸发到剩有少量液体时,停止加热,利用余热将液体蒸干
D.分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出
 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源: 题型:
如图利用培养皿探究氨气的性质。实验时向NaOH固体上滴几滴浓氨水,立即用另一表面皿扣在上面。下表中对实验现象所做的解释正确的是( )
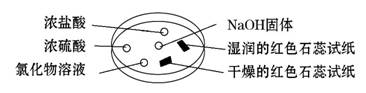
| 选项 | 实验现象 | 解释 |
| A | 浓盐酸附近产生白烟 | NH3与浓盐酸反应生成了NH4Cl固体 |
| B | 浓硫酸附近无明显现象 | NH3与浓硫酸不发生反应 |
| C | 氯化物溶液变浑浊 | 该溶液一定是AlCl3溶液 |
| D | 干燥的红色石蕊试纸不变色,湿润的红色石蕊试纸变蓝 | NH3是一种可溶性碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知101KPa时辛烷的标准燃烧热为—5518kJ·mol-1,含20gNaOH的稀溶液与稀盐酸充分反应放出热量28.7kJ,则下列热化学方程式书写正确的是
①C8H18(l)+ 25/2O2(g)= 8CO2(g)+ 9H2O(g); △H = +5518 kJ·mol-1
②C8H18(l)+ 25/2O2(g)= 8CO2(g)+ 9H2O(l); △H = -5518 kJ·mol-1
③H+(aq)+ OH-(aq)= H2O(l); △H = -57.4 kJ·mol-1
④HCl (aq) + NaOH(aq) =NaCl(aq) + H2O(l); △H = —28.7 kJ·mol-1
A.①③ B.②③ C.②④ D.②
查看答案和解析>>
科目:高中化学 来源: 题型:
相同质量的SO2和SO3,下列关系正确的是
A.含氧原子个数比为2:3
B.含硫元素质量比为4:5
C.含氧元素质量比为5:6
D.含硫原子个数比为1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
在配制一定物质的量浓度的NaCl溶液时,下列操作会造成所配溶液浓度偏高的是( )
A. 在用托盘天平称量所需NaCl的质量时,左盘放砝码右盘放NaCl
B. 定容时俯视刻度线
C. 转移时,把烧杯和玻璃棒用蒸馏水洗涤并把洗涤液也转移至容量瓶
D. 容量瓶中有少量水,转移溶液前将容量瓶烘干
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是给病人输液用的氯化钠注射溶液的标签。(友情提示:若要用到溶液密度,可用水的密度进行计算)

(1)氯化钠的摩尔质量____________________
(2)该注射溶液的物质的量浓度为 mol/L。(保留两位有效数字)
(3)某同学配制了1000mL氯化钠注射溶液,为测定所配氯化钠注射液是否达标,取该氯化钠注射液130 mL于烧杯中,然后滴入足量的AgNO3溶液,充分反应后,过滤得到白色沉淀2.87g。请你通过计算判断该氯化钠注射液是否符合上述要求,写出计算过程。
(保留两位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
过滤后的食盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4 等杂质,通过如下几个实验步骤,可制得纯净的食盐水:① 加入稍过量的Na2CO3溶液;② 加入稍过量的NaOH溶液;③ 加入稍过量的BaCl2 溶液;④滴入稀盐酸至无气泡产生;⑤ 过滤。正确的操作顺序是( )
A.③②①⑤④ B.①②③⑤④
C.②③①④⑤ D.③⑤②①④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于12 g C-12的说法不正确的是( )
A.碳原子的物质的量为1 mol
B.碳原子的个数为NA mol
C.碳原子的个数为NA
D.该原子常被称为标准碳原子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com