

 ;
; ;sp3;三角锥形;
;sp3;三角锥形;| 1 |
| 3 |
| 1 |
| 2 |
| 1 |
| 8 |
| 1 |
| 2 |
| 4×64 |
| NA |
| 4×64 |
| NA |
| 256 |
| ρa3 |
| 256 |
| ρa3 |


科目:高中化学 来源: 题型:
| A、a=b=c |
| B、a=c>b |
| C、b>a>c |
| D、c>a>b |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 3 |
| 73 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 化学课外活动小组设计了如图所示的一套气体发生、收集和尾气吸收装置,以探究该装置的多功能性能.
化学课外活动小组设计了如图所示的一套气体发生、收集和尾气吸收装置,以探究该装置的多功能性能.查看答案和解析>>
科目:高中化学 来源: 题型:
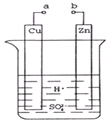 原电池是化学对人类的一项重大贡献.
原电池是化学对人类的一项重大贡献. 查看答案和解析>>
科目:高中化学 来源: 题型:
 ,芳香烃A能发生如图一系列转化:
,芳香烃A能发生如图一系列转化:
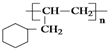 的线路.(用A→…→目标产物 在箭号上写明反应试剂及反应条件.)
的线路.(用A→…→目标产物 在箭号上写明反应试剂及反应条件.)查看答案和解析>>
科目:高中化学 来源: 题型:
| 14 |
| 6 |
| 14 |
| 7 |
| 16 |
| 8 |
| 35 |
| 17 |
| 235 |
| 92 |
| 238 |
| 92 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com