
【题目】一定温度下,在一固定容积的密闭容器中发生反应H2(g)+I2(g)![]() 2HI(g),判断该反应达到平衡的标志是 ( )
2HI(g),判断该反应达到平衡的标志是 ( )
A. 混合气体的颜色不再改变B. H2、I2、HI的浓度相等
C. 混合气体的密度保持不变D. H2、I2、HI分子个数比为1∶1∶2
科目:高中化学 来源: 题型:
【题目】如图是实验室常用的部分仪器,请回答下列问题
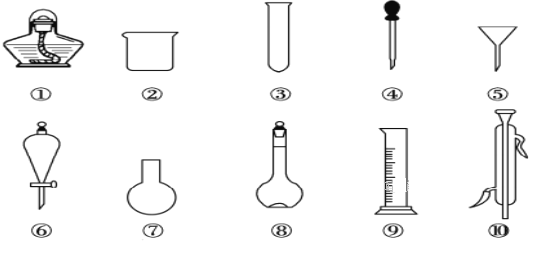
(1)序号为⑧和⑩的仪器名称分别为__________、__________。
(2)在分液操作中,必须用到上述仪器中的________(填序号)。
(3)能作反应仪器且可直接加热的仪器上述中的___________(填名称)。
(4)在配制一定物质的量浓度的溶液时,需要用到的仪器是___________(填序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定量的Fe、FeO、Fe3O4的混合物中加入100mL2mol/L的盐酸,恰好使混合物完全溶解,放出224mL(标准状况)的气体,所得溶液中加入KSCN溶液无血红色出现。若用足量的CO在高温下还原相同质量的此混合物,能得到铁的质量是( )
A. 11.2gB. 5.6gC. 2.8gD. 无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】强酸性溶液X中可能含有Na+ , K+、NH4+、 Fe3+、Fe2+、Al3+、CO32-、 SO32-、SO42-、C1-的若干种,某同学为了确认其成分,取X溶液进行连 续实验,实验过程及产物如下所示:

下列结论止确的是
A.气体A是SO2,证明原溶液中含有SO32-
B.沉淀G中加人盐酸溶解,滴加KSCN溶液显红色,可以确定原溶液中 有Fe3+
C.沉淀I―定是A1(OH)3
D.X中不能确定的离子是Al3+、Fe3+ 、Na+ 、K +和Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应A2+B2 =2AB的能量变化如图所示。下列说法正确的是( )

A. 该反应是吸热反应
B. 2 mol A—B键断裂需要吸收y kJ 的能量
C. 1 mol A—A键和1mol B—B键断裂能放出x kJ的能量
D. 2 mol AB的总能量高于1 mol A2和1 mol B2的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛(Ti)被称为继铁、铝之后的第三金属,钛白(TiO2)是目前最好的白色颜料。制备TiO2和Ti的原料是钛铁矿,我国的钛铁矿储量居世界首位。含有Fe2O3的钛铁矿(主要成分为FeTiO3)制取TiO2的流程如下:

(1)Ti的原子序数为22,位于元素周期表中第_________周期第___________族。
(2)步骤①加铁的目的是___________________;步骤②冷却的目的是__________。
(3)写出流程中生成H2TiO3的离子方程式__________________________________。
(4)上述制备TiO2的过程中,考虑成本和废物综合利用因素,废液中应加入______处理。
(5)由金红石(TiO2 )制取单质Ti,涉及到的步骤为:TiO2→TiCl4![]() Ti
Ti
已知:① C(s) + O2 (g) = CO2 (g) ΔH = -393.5 kJmol-1
② 2CO(g) + O2 (g) = 2CO2(g) ΔH =-566 kJmol-1
③ TiO2 (s) + 2Cl2 (g) = TiCl4 (s) + O2 (g) ΔH = +141kJmol-1
则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g) 的ΔH =___________。反应TiCl4+2Mg=2MgCl2+Ti在Ar气氛中进行的理由是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应属于氧化还原反应的是( )
A. SO3+ H2O= H2SO4 B. NH4Cl ![]() NH3
NH3![]() +HCl
+HCl![]()
C. Fe+CuSO4= FeSO4+Cu D. NaOH+HNO3=NaNO3+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关物质的量的计算填空:
(1)2 mol尿素[CO(NH2)2]含_____________个H原子,所含氧原子跟__________g H2O所含氧原子个数相等。
(2)①标准状况下,22.4 L CH4;②1.5 mol NH3;③1.806×1024个H2O;④标准状况下,73 g HCl。所含H原子个数由多到少的顺序是____________________。
(3)30.9 g NaR含有Na+0.3 mol,则NaR的摩尔质量为_________________。
(4)100mL某Al2(SO4)3溶液中,c(Al3+)=2.0 mol·L-1,则其中c(SO42-)=_________mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以葡萄糖为原料制得的山梨醇(A)和异山梨醇(B)都是重要的生物质转化平台化合物。E是一种治疗心绞痛的药物,由葡萄糖为原料合成E的过程如下:
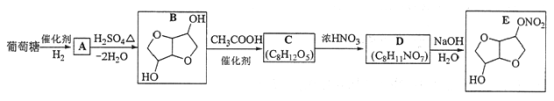
回答下列问题:
(1)葡萄糖的分子式为__________。
(2)A中含有的官能团的名称为__________。
(3)由B到C的反应类型为__________。
(4)C的结构简式为__________。
(5)由D到E的反应方程式为______________。
(6)F是B的同分异构体,7.30 g的F与足量饱和碳酸氢钠反应可释放出2.24 L二氧化碳(标准状况),F的可能结构共有________种(不考虑立体异构),其中核磁共振氢谱为三组峰,峰面积比为3∶1∶1的结构简式为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com