
下列关于晶体说法的正确组合是( )
①分子晶体中都存在共价键
②在晶体中只要有阳离子就一定有阴离子
③金刚石、SiC、NaF、NaCl、H2O、H2S晶体的熔点依次降低
④离子晶体中只有离子键没有共价键,分子晶体中肯定没有离子键
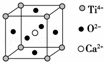
⑤CaTiO3晶体中(晶胞结构如图所示)每个Ti4+和12个O2﹣紧邻
⑥60gSi02中含Si﹣O键的个数为2NA
⑦晶体中分子间作用力越大,分子越稳定
⑧氯化钠熔化时离子键被破坏
⑨124g P4含有P﹣P键的个数为4NA.
|
| A. | ①②③⑥ | B. | ①②④ | C. | ③⑤⑦ | D. | ③⑤⑧ |
考点:
晶胞的计算;化学键.
专题:
化学键与晶体结构.
分析:
①分子晶体中不一定都存在共价键,单原子分子不存在共价键.
②在晶体中有阳离子不一定有阴离子.
③根据晶体类型判断熔点高低.
④离子晶体中一定含有离子键,可能含有共价键.
⑤采用沿X、Y、Z三轴切割的方法判断其配位数.
⑥每个硅原子存在4个Si﹣O键,根据二氧化硅质量计算硅原子个数,从而计算硅氧键个数.
⑦分子晶体中分子间作用力越大,分子越稳定
⑧氯化钠熔化时离子键被破坏.
⑨每个白磷分子中含有6个共价键,根据白磷的分子个数计算白磷中含有的P﹣P共价键个数.
解答:
解:①分子晶体中不一定都存在共价键,如:稀有气体是单原子分子,在分子内不存在共价键,故错误.
②在晶体中有阳离子不一定有阴离子,如:金属晶体中存在的微粒是金属阳离子和自由电子,故错误.
③晶体中熔点高低一般顺序是:原子晶体>离子晶体>分子晶体;在原子晶体中,原子半径越大熔点越低;在离子晶体中,离子半径越大,熔点越低,电荷越多,熔点越高;在分子晶体中,物质的熔点与相对分子质量成正比(含有氢键的物质除外),所以这几种物质的熔点高低顺序是:金刚石、SiC、NaF、NaCl、H2O、H2S晶体的熔点依次降低,故正确.
④离子晶体中一定含有离子键,可能含有共价键,分子晶体中肯定没有离子键,故错误.
⑤采用沿X、Y、Z三轴切割的方法知,CaTiO3晶体中(晶胞结构如图所示)每个Ti4+和12个O2﹣紧邻,故正确.
⑥一个硅原子含有4个硅氧键,60gSi02的物质的量1mol,所以含Si﹣O键的个数为4NA,故错误.
⑦分子晶体中分子间作用力越大,分子越稳定,在离子晶体、金属晶体和原子晶体中不存在分子间作用力,故错误.
⑧氯化钠熔化时离子键被破坏生成自由移动的阴阳离子,故正确.
⑨一个白磷分子中含有6个P﹣P键,124g P4的物质的量是1mol,所以含有P﹣P键的个数为6NA,故错误.
故选D.
点评:
本题考查的知识点较多,明确离子晶体中确定离子配位数的方法是:采用沿X、Y、Z三轴切割的方法;知道白磷分子是正四面体构型.


科目:高中化学 来源: 题型:
人类与食盐关系密切,食盐在老百姓生活和现代社会的工农业生产中均有重要作用.粗盐中含有Ca2+、Mg2+、SO42﹣以及泥沙等杂质,请回答粗盐提纯的有关问题:
(1)为了除去可溶性杂质,可以按以下实验步骤进行提纯:①加过量BaCl2溶液;②加过量NaOH溶液;③加过量Na2CO3溶液;④过滤;⑤ .请补全实验步骤,并回答步骤③的目的 .
(2)2010年7月26日,卫生部公布了《食用盐碘含量》的征求意见稿,面向社会征求意见.对于食用盐中碘含量平均水平的规定有所降低.食盐中添加的是KIO3.可用下列反应来检验食
盐中是否含KIO3:KIO3+KI+H2SO4﹣I2+K2SO4+H2O (未配平).请配平该反应并表示出电子转移的方向和数目 ;为了获取反应后溶液中的I2,可采取的实验操作方法的名称是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
为了验证木炭可被浓H2SO4氧化成CO2,选用下图所示仪器(内含物质)组装成实验装置:

(1)如按气流由左向右流向,连接上述装置的正确顺序是(填各接口字母): 接 , 接 ,接 ;
(2)仪器乙、丙应有怎样的实验现象才表明已检验出CO2?乙中 ,丙中丙 ;
(3)丁中酸性KMnO4溶液的作用是 ;
(4)写出甲中反应的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
有关Na2CO3和NaHCO3的叙述中正确的是()
A. 相同质量的Na2CO3和NaHCO3与足量盐酸作用时,产生的气体质量相同
B. Na2CO3比NaHCO3热稳定性强
C. Na2CO3不能与澄清石灰水反应
D. Na2CO3和NaHCO3均可与NaOH溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
|
| A. |
|
|
| B. | 不同元素的原子构成的分子只含极性共价键 |
|
| C. |
|
|
| D. | 短周期第ⅣA与ⅦA族元素的原子间构成的分子,均满足原子最外层8电子结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:
“类推”是一种常用的学习方法,但有时会产生错误的结论,下列类推结论中正确的是( )
|
| A. | ⅣA族元素氢化物沸点顺序是:GeH4>SiH4>CH4;则ⅤA族元素氢化物沸点顺序也是:AsH3>PH3>NH3 |
|
| B. | 第二周期元素氢化物的稳定性序是:HF>H2O>NH3;则第三周期元素氢化物的稳定性顺序也是:HCl>H2S>PH3 |
|
| C. | 晶体中有阴离子,必有阳离子;则晶体中有阳离子,必有阴离子 |
|
| D. | 干冰(CO2)是分子晶体,则SiO2也是分子晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关叙述正确的是( )
|
| A. | 已知NaH是离子化合物,则其电子式是 Na+[:H]﹣ |
|
| B. | 在PCl5分子中,磷原子满足最外层8电子结构 |
|
| C. | 在BCl3分子中,所有原子都满足最外层8电子结构 |
|
| D. | 石墨晶体是层状结构,在同一层上平均每个正六边形所含有的碳原子数为2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列萃取与分液相结合进行的操作(用苯从碘水中萃取碘单质,且已知苯的密度比水小)中错误的是()
A. 碘水和苯加入分液漏斗后,塞上上口部的塞子,用一手压住分液漏斗上口部,一手握住活塞部分,把分液漏斗倒转过来振荡,并不时地放气
B. 静置,待分液漏斗中液体分层后,先使分液漏斗内外空气相通(准备放出液体)
C. 打开分液漏斗的活塞,使全部下层液体沿承接液体的烧杯内壁慢慢流出,及时关闭活塞
D. 最后继续打开活塞,另用烧杯在分液漏斗的下口承接并保存上层液体
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作中错误的是()
A. 进行蒸发操作时,应加热至混合物中有大量晶体析出时停止加热,用余热蒸干
B. 进行蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C. 进行分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D. 进行萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com