
【题目】近年来AIST报告正在研制一种“高容量、低成本”的锂-铜空气燃料电池,该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为:2Li+Cu2O+H2O═2Cu+2Li++2OH-,下列说法正确的是
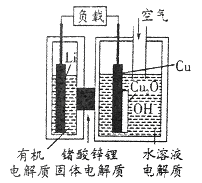
A. 正极为Li,负极为Cu
B. 放电时,正极的电极反应为:2Cu+2OH-+2e-==Cu2O+2H2O
C. Li极有机电解质可以换成Cu极的水溶液电解质
D. 通空气时,整个反应过程中,铜相当于催化剂
科目:高中化学 来源: 题型:
【题目】镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd +2NiOOH + 2H2O![]() Cd(OH)2 +2Ni(OH)2,有关该电池的说法正确的是
Cd(OH)2 +2Ni(OH)2,有关该电池的说法正确的是
A. 充电时阳极反应:Ni(OH)2-e—+OH-==NiOOH+H2O
B. 充电过程是化学能转化为电能的过程
C. 放电时负极附近溶液的碱性不变
D. 放电时电解质溶液中的OH-向负极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物 的分子式均为C5H8O2,下列说法正确的是( )
的分子式均为C5H8O2,下列说法正确的是( )
A.x分子中碳原子均位于同一平面
B.x、y均能与NaOH溶液发生反应
C.y、z均能与![]() 反应生成
反应生成![]()
D.与它们互为同分异构体的链状羧酸有6种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铅蓄电池是典型的可充型电池,起反应为Pb+PbO2+4H++2SO42-![]() 2PbSO4+2H2O:,下列说法正确的是
2PbSO4+2H2O:,下列说法正确的是
A. 放电时负极质量减少,正极质量增加,电解质溶液中H2SO4的浓度将变小
B. 放电时负极的电极反应为:PbO2+2e-+4H++SO42-=PbSO4+2H2O
C. 充电时Pb与电源正极相连
D. 充电时阳极上pbSO4变为PbO2,发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校的化学兴趣小组利用下列实验装置探究二氧化硫的性质,E中装有常见气体,与E装置相连的玻璃导管可根据需要变换长短。
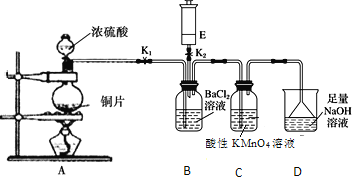
实验开始时关闭K2打开K1,从分液漏斗中向烧瓶内加入浓硫酸。
(1)A中发生反应的化学方程式是:________________________________________。
(2)C中的现象是______________,证明SO2有____________性。
(3)D的作用是_____________________,反应的离子方程式为____________。
(4)A中反应完成后,关闭K1,打开K2,将E中的无色气体缓缓注入B中,有白色沉淀产生:
①若E是无色有刺激性气味气体,它的分子式为________ (填化学式)
②若E是无色无味气体, 产生的白色沉淀是_________(填化学式)。
(5)若将B中溶液换成Ba(NO3)2溶液,将会有白色沉淀生成,请用离子方程式解释其原因________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上制备下列物质的生产流程合理的是( )
A. 由铝土矿冶炼铝:铝土矿![]() Al2O3
Al2O3![]() AlCl3
AlCl3![]() Al
Al
B. 从海水中提取镁:海水![]() Mg(OH)2
Mg(OH)2![]() MgO
MgO![]() Mg
Mg
C. 由NaCl制漂白粉:饱和食盐水![]() Cl2
Cl2![]() 漂白粉
漂白粉
D. 由黄铁矿制硫酸:黄铁矿![]() SO2
SO2![]() SO3
SO3![]() H2SO4
H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】马航失联事件震惊中外,事件发生后,联合搜救部门启用了“金枪鱼”水下搜救器展开水下搜救,其中![]() 电池是一种可用作水下动力的优良电源,其原理如图所示。该电池工作时总反应式为
电池是一种可用作水下动力的优良电源,其原理如图所示。该电池工作时总反应式为![]() ,则下列说法错误的是
,则下列说法错误的是![]()
![]()
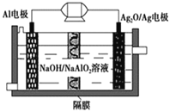
A.Al电极做负极,电极反应式为:![]()
B.工作时电解液中的OH-移向![]() 电极
电极
C.工作时正极发生还原反应,负极不断减重
D.当电极上生成![]() 时,电路中转移的电子为0.01mol
时,电路中转移的电子为0.01mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知断开 1mol Cl2(g)中Cl-Cl键需要吸收243kJ能量,根据能量变化示意图,下列说法或热化学方程式正确的是( )
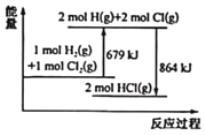
A.H2(g)+Cl2(g) = 2HCl(g) ΔH= + 185 kJ·mol-1
B.生成1mol H2(g)中的H-H键放出 121.5 kJ 能量
C.断开1mol HCl(g)中的H-C1键要吸收 864 kJ 能量
D.HCl(g) =![]() H2(g)+
H2(g)+![]() Cl2(g) ΔH= + 92.5kJ·mol-1
Cl2(g) ΔH= + 92.5kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石油是工业的血液,通过它可以得到很多重要的化工产品。

已知: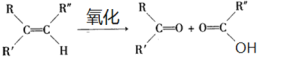
(1)B和A为同系物,B的结构简式为_________________;
(2)反应①的化学方程式为__________________,其反应类型为___________;
(3)写出检验C3H5Cl中含有Cl原子的方法:______________;
(4)C的结构简式为______________;
(5)反应④的化学方程式为_______________;
(6)设计一条由乙烯为原料制备D的合成路线(其他无机原料任选)____________。(合成路线格式如下:CH3CH2OH ![]() H2C=CH2
H2C=CH2 ![]() BrCH2CH2Br)
BrCH2CH2Br)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com