
| A、只含非极性键的分子一定是非极性分子 |
| B、含有极性键的分子一定是极性分子 |
| C、非极性分子一定含有非极性键 |
| D、由极性键构成的双原子分子一定是极性分子 |
 只含非极性键,空间构型不对称,正负电荷重心不重合,是极性分子,故A错误;
只含非极性键,空间构型不对称,正负电荷重心不重合,是极性分子,故A错误;

科目:高中化学 来源: 题型:
| A、在含硫的燃煤中加入适量生石灰 |
| B、使用酒精、天然气代替部分或全部燃油 |
| C、在汽油中添加四乙基铅提高汽油的稳定性和燃烧效率 |
| D、推广利用微生物发酵技术,将植物桔杆、动物粪便等制成沼气以替代液化石油气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaHSO4 |
| B、NaCl |
| C、HCl |
| D、Ba(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH3Cl+Cl2→CH2Cl2+HCl |
| B、CH3-CH=CH2+Br2─→CH3-CHBr-CH2Br |
C、 |
D、 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在101kPa时,1mol物质完全燃烧时所放出的热量,叫做该物质的燃烧热 |
| B、酸和碱发生中和反应生成1mol水,这时的反应热叫中和热 |
| C、燃烧热或中和热都属于反应热 |
| D、1mol CH3COOH和1mol NaOH完全中和时放出的热量小于57.3kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H-H键无方向性 |
| B、基态C原子有两个未成对电子,所以最多只能形成2个共价键 |
| C、1个N原子最多只能与3个H原子结合形成NH3分子,是由共价键的饱和性决定的 |
| D、所有的原子轨道都具有一定的伸展方向,因此所有的共价键都具有方向性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学式 | FeS | CuS | MnS |
| 溶度积 | 6.3×10-18 | 1.3×10-36 | 2.5×10-13 |
| A、25℃时,CuS的溶解度大于MnS的溶解度 |
| B、25℃时,饱和CuS溶液中,Cu2+的浓度为1.3×10-36 mol?L-1 |
| C、因为H2SO4是强酸,所以反应CuSO4+H2S=CuS↓+H2SO4不能发生 |
| D、除去某溶液中的Cu2+,可以选用FeS作沉淀剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、能与水反应 |
| B、能与氢氧化钠溶液反应 |
| C、能与硫酸反应 |
| D、能与碳酸钠溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
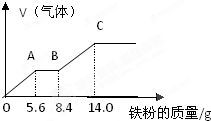 某稀硫酸和稀硝酸的混合溶液100mL,向其中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸的还原产物只有NO气体)
某稀硫酸和稀硝酸的混合溶液100mL,向其中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸的还原产物只有NO气体)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com