
����Ŀ����1����״���£�22.4LH2������Ϊ____________g��
��2��9.8g H2SO4�����ʵ���Ϊ__________mol��Լ����___________����ԭ�ӡ�
��3��VL Fe2(SO4)3��Һ�к���ag SO42-,ȡ����Һ0.5L����ˮϡ����2VL,��ϡ�ͺ����Һ��Fe3+�����ʵ���Ũ��Ϊ_________mol/L��
��4����״���£�16 gij��̬������RO2�����Ϊ5.6 L���������Ħ��������________��
��5��b%��������Һ��4b%��������Һ�������Ϻ�������Һ����������______���� �������� = ��ͬ��2.5b%��
��6����ij�¶�ʱ��һ������Ԫ��A����̬�⻯��AH3����һ��������ܱ���������ȫ�ֽ���������嵥�ʣ���ʱѹǿ������75%������A�Ļ�ѧʽΪ____________��
���𰸡�2 0.1 0.4 NA����2.408��1023) a/576V mol/L 64g/mol �� P4
��������
(1) ��״���£�22.4LH2�����ʵ���Ϊ1mol��������Ϊ2g��(2) 9.8g H2SO4�����ʵ���Ϊ9.8g/98g/mol=0.1mol������0.4mol��ԭ�ӣ�������0.4 NA����2.408��1023)�� (3) ag SO42-�����ʵ���Ϊa/96mol���������ӵ����ʵ���Ϊ![]() mol����ˮϡ����4����ϡ�ͺ��Ũ����ԭ��Ũ�ȵ�1/4�������ʵ���Ũ��Ϊ
mol����ˮϡ����4����ϡ�ͺ��Ũ����ԭ��Ũ�ȵ�1/4�������ʵ���Ũ��Ϊ![]() =a/576V mol/L�� (4) ��״���£�5.6 L ����������ʵ���Ϊ5.6L/22.4L/mol=0.25mol������Ħ������Ϊ16g/0.25mol=64g/mol��(5) ��Ϊ������ܶȱ�ˮ�����������������������������Һ���ܶ��������Լ���b%��������Һ���ܶ�Ϊd1��4b%��������Һ���ܶ�Ϊd2������Ϻ���Һ����������Ϊ��d1Vb%+4d2Vb%��/��d1V+d2V������Ϊd1С��d2������Һ��������������2.5b% �� (6) ����������д����ʽΪ��2xAH3=2Ax+3xH2����ȫ�ֽ�ѹǿ������75%��˵����������ʵ�����ԭ����175%����2+3x/2x=175%����x=4����õ����к���4��ԭ�ӣ����Ըõ���ΪP4��
=a/576V mol/L�� (4) ��״���£�5.6 L ����������ʵ���Ϊ5.6L/22.4L/mol=0.25mol������Ħ������Ϊ16g/0.25mol=64g/mol��(5) ��Ϊ������ܶȱ�ˮ�����������������������������Һ���ܶ��������Լ���b%��������Һ���ܶ�Ϊd1��4b%��������Һ���ܶ�Ϊd2������Ϻ���Һ����������Ϊ��d1Vb%+4d2Vb%��/��d1V+d2V������Ϊd1С��d2������Һ��������������2.5b% �� (6) ����������д����ʽΪ��2xAH3=2Ax+3xH2����ȫ�ֽ�ѹǿ������75%��˵����������ʵ�����ԭ����175%����2+3x/2x=175%����x=4����õ����к���4��ԭ�ӣ����Ըõ���ΪP4��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӵ����������������ֱ���ȣ����Dz�������
A.��������B.һ��ԭ�Ӻ�һ�ַ���
C.һ�ַ��Ӻ�һ������D.һ�ֵ��ʷ��Ӻ�һ�ֻ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ݱ������ҹ����Ϻ��������������еĿ�ȼ���������ˮ����)�Բɻ�óɹ���������һ����Ҫ�Ļ���ԭ�ϡ�
��1����������������������ʵ���Ҫ��ʽ������������������¶��֣�
ˮ����������CH4(g)+H2O(g)![]() CO(g)+3H2(g) ��H1=+205.9kJ��mol-1 ��
CO(g)+3H2(g) ��H1=+205.9kJ��mol-1 ��
CO(g)+H2O(g)![]() CO2(g)+H2(g) ��H2=��41.2kJ��mol-1 ��
CO2(g)+H2(g) ��H2=��41.2kJ��mol-1 ��
������̼������CH4(g)+CO2(g)![]() 2CO(g)+2H2(g) ��H3 ��
2CO(g)+2H2(g) ��H3 ��
��Ӧ ���Է����е�������________________����H3 =_____________kJ��mol-1��
�������Ĺ̶�һֱ�ǿ�ѧ���о�����Ҫ���⣬�ϳɰ������˹��̵��Ƚϳ���ļ�������ԭ��ΪN2(g)+3H2(g)![]() 2NH3(g)
2NH3(g)
��2���ڲ�ͬ�¶ȡ�ѹǿ����ͬ���������£���ʼʱN2��H2�ֱ�Ϊ0.1mol��0.3molʱ��ƽ��������а��������������������ͼ��ʾ��
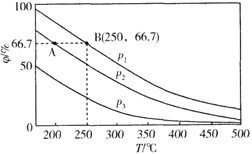
�����У�p1��p2��p3�ɴ�С��˳����________����ԭ����_________________��
�����ֱ���vA(N2)��vB(N2)��ʾ�ӷ�Ӧ��ʼ����ƽ��״̬A��Bʱ�Ļ�ѧ��Ӧ���ʣ���vA(N2)______ vB(N2)������>����<������=����
������250����p1Ϊ105Pa�����£���Ӧ�ﵽƽ��ʱ���������Ϊ1L�����������B��N2�ķ�ѹp(N2)Ϊ_________Pa (��ѹ=��ѹ�����ʵ�������������һλС��)��
���������������(S2O42��)Ϊý�飬ʹ�ü�ӵ绯ѧ��Ҳ�ɴ���ȼú�����е�NO��װ����ͼ��ʾ��
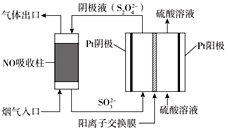
���������ĵ缫��ӦʽΪ_____________________________��
��NO����ת�������Ҫ����ΪNH4+����ͨ��ʱ��·��ת����0.3mole�������ͨ����������������յ�NO�ڱ�״���µ����Ϊ_______mL��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��WΪԭ������������������ֶ���������Ԫ�أ�����X��Zͬ���壬Yԭ�ӵ�����������Ϊ������������һ�룬Xԭ�ӵ��������������������Ӳ�����3��������˵������ȷ����
A. �����̬�⻯������ȶ���,W>Z>Y B. ���ʵķе㣺Y>X>Z
C. �����Ӱ뾶:Z>W>X D. X���⻯���п��ܺ��зǼ��Թ��ۼ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����п��Դ����������γ���ɫ��Һ��һ������Ӧ���ǣ� ��
A.Ag+��Cu2+��NO3����Na+
B.NO3����Fe3+��Mg2+��SO42��
C.Na+��Ca2+��Cl����CO32��
D.K+��Ba2+��Cl����NO3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ɲ⣬��������仯�����ʵ������ṹ�����˱仯�Ľ�����ش�����������
��1�������ӻ���������ж������з��ӵĿռ乹����V�ε���_____(����ĸ)��
A.BeCl2 B.H2O C.HCHO D.CS2
��2��ԭ������С��36��Ԫ��Q��T�������ڱ��м�λ��ͬһ������λ��ͬһ������T��ԭ��������Q��2��T�Ļ�̬ԭ�ӵ���Χ����(�۵���)�Ų�ʽΪ____��Q2+��δ�ɶԵ�������_____��
��3��ͭ����Ͻ�����������ʹ�õĽ���������Cu2+����NH3�γ���λ��Ϊ4�������[Cu(NH3)4]SO4��
����Ԫ�������ڱ��е�λ����______��[Cu(NH3)4]SO4����N��O��S����Ԫ�صĵ�һ�������ɴ�С��˳��Ϊ______��
��[Cu(NH3)4]SO4�У����ڵĻ�ѧ����������______(����ĸ)��
A���Ӽ� B������ C.��λ�� D.�Ǽ��Լ� E���Լ�
��NH3��Nԭ�ӵ��ӻ����������______��д��һ����SO42-��Ϊ�ȵ�����ķ��ӵĻ�ѧʽ:_ ______��
��[Cu(NH3)4]2+���жԳƵĿռ乹����[Cu(NH3)4]2+�е�����NH3������Cl-ȡ�����ܵõ����ֲ�ͬ�ṹ�IJ���.��[Cu(NH3)4]2+�Ŀռ乹��Ϊ_________��
��4������ͭ�γɵ�ij�����Ӿ���ľ�����ͼ��ʾ����û�����Ļ�ѧʽΪ_____������þ�����ܶ�Ϊ��g/cm3����þ�����ͭ�����������Ӽ���������Ϊ_____(�ú����Ĵ���ʽ��ʾ�����а����ӵ�������NA��ʾ)cm��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ԫ������Y��Z��W��ԭ������������������Wͬ������Wԭ�Ӻ˵��������Xԭ�Ӻ˵������2����Y��Zԭ�ӵĺ��������֮��������Wԭ�ӵĺ��������֮����ȡ�����˵����һ����ȷ����
A. ����ԭ�Ӱ뾶��Y��ԭ�Ӱ뾶��
B. ���γɵ��⻯������в����Ǽ��Լ�
C. Z��W������������Ӧ��ˮ��������
D. Y������ˮ��Ӧ��ˮ������������Ҳ��������ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ����������β���ŷų���NOx��SO2�ȣ����γ���������Ҫ���ʣ����ۺ������ǵ�ǰ��Ҫ���о����⡣
��. NOx������������β���е�NO(g)��CO(g)��һ���¶Ⱥʹ��������¿ɷ������·�Ӧ��2NO(g)+2CO(g) ![]() N2(g)+2CO2(g) ��H��
N2(g)+2CO2(g) ��H��
��1����֪��COȼ���ȵ���H1=��283.0kJ��mol-l��
N2(g)+O2(g) ![]() 2NO(g) ��H2=+180.5kJ��mol-1������H=____________��
2NO(g) ��H2=+180.5kJ��mol-1������H=____________��
��2��ij�о�С��̽��������CO��NOת����Ӱ�졣��NO��CO��һ��������ͨ�����ֲ�ͬ�Ĵ������з�Ӧ����ͬʱ���ڲ����ݳ�������NO�������Ӷ�ȷ��β���ѵ���(�ѵ��ʼ�NO��ת����)���������ͼ��ʾ��
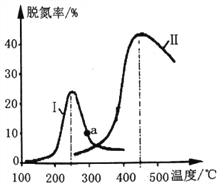
������˵����ȷ����__________________(����ĸ)��
A.���ִ������ܽ��ͻ�ܣ�����H����
B.��ͬ�����£��ı�ѹǿ���ѵ���û��Ӱ��
C.�������еĴ���������450�������ѵ�
D.�������д����ѵ��ʱ�����I�еĸ�
��������200����ͼ������I�ѵ������¶����߶��仯�������Ҫԭ��Ϊ___________���ж�a���Ƿ�Ϊ��Ӧ�¶��µ�ƽ���ѵ��ʣ���˵�������ɣ�____________��
��.SO2���ۺ�����
��3��ij�о�С��Է�ӦNO2+SO2![]() SO3+NO ��H<0�������ʵ��̽�����ڹ̶�������ܱ������У�ʹ��ij�ִ������ı�ԭ�������[no(NO2)��no(SO2)]���ж���ʵ��(����ʵ����¶ȿ�����ͬ��Ҳ���ܲ�ͬ)���ⶨNO2��ƽ��ת����[a(NO2)]������ʵ��������ͼ��ʾ��
SO3+NO ��H<0�������ʵ��̽�����ڹ̶�������ܱ������У�ʹ��ij�ִ������ı�ԭ�������[no(NO2)��no(SO2)]���ж���ʵ��(����ʵ����¶ȿ�����ͬ��Ҳ���ܲ�ͬ)���ⶨNO2��ƽ��ת����[a(NO2)]������ʵ��������ͼ��ʾ��
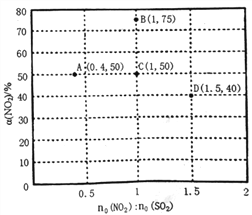
�������ͼ��C���ƽ��״̬�ı�ΪB���ƽ��״̬��Ӧ��ȡ�Ĵ�ʩ��________________��
��ͼ��C��D�����Ӧ��ʵ���¶ȷֱ�ΪTC��TD��ͨ�������жϣ�TC__________TD(����>������=������<��)��
��4����֪25��ʱ��NH3��H2O��Kb=1.8��10-5��H2SO3��Ka1=1.3��10-2��Ka2=6.2��10-8������ˮ��Ũ��Ϊ2.0mol��L-1����Һ�е�c(OH��)= ____________mol��L-1����SO2ͨ��ð�ˮ�У�����Һ������ʱ��Һ�е�![]() =__________��
=__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E����5��Ԫ�ء�����գ�
��1��AԪ�ػ�̬ԭ�ӵ��������3��δ�ɶԵ��ӣ��������2�����ӣ���Ԫ�ط���Ϊ______��
��2��BԪ�صĸ�һ�����Ӻ�CԪ�ص���һ�����ӵĵ��Ӳ�ṹ�������ͬ��B��һ�����ӵĽṹʾ��ͼΪ______��Cԭ�ӵĵ����Ų�ʽΪ______��
��3��DԪ�ص����������ӵ�3d�ܼ�Ϊ�������D��Ԫ�ط���Ϊ___�����̬ԭ�ӵĵ����Ų�ʽΪ______��
��4��EԪ�ػ�̬ԭ�ӵ�M��ȫ������N��û�гɶԵ��ӣ�ֻ��һ��δ�ɶԵ��ӣ�E��Ԫ�ط���Ϊ____�����̬ԭ�ӵļ۵����Ų�ͼΪ______��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com