
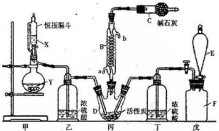
���� ��1������װ��ͼ��֪��EΪ��Һ©���������������ܵ�������������������Ӧ��û�м��ȣ��ݴ��ж�SO2��������ķ�Ӧ����ЧӦ�����ڻ���һ����Cl2��SO2ͨ���������ݳ�����C��Ӧʹ�ü����Լ�������SO2Cl2��ˮ��ˮ�⣬�ʼ�ʯ������������������SO2����ֹ�����е�ˮ��������B�У�
��2���������ü�װ���п���������������ѹǿ���ԭ�������������ԣ�
��3�������Ʊ�SO2��װ�ã�ͭ��Ũ���ᷴӦ��Ҫ���ȣ�����������SO2���ݴ˴��⣻
��4������ˮ�����ڱ���ʳ��ˮ����E�е��Լ��DZ���ʳ��ˮ��������ˮ���ڵ������¿ɽ�SO2���������ᣬ��������ԭΪHCl��
��5������е㲻ͬ��Һ�����������ķ�������״���£�896mlCl2Ϊ0.04mol���������Ͽɵõ�0.04molSO2Cl2���ɴ˿�������ʣ�
��� �⣺��1������װ��ͼ��֪��EΪ��Һ©���������������ܵ�������������������Ӧ��û�м��ȣ���SO2��������ķ�ӦΪ���ȷ�Ӧ�����ڻ���һ����Cl2��SO2ͨ���������ݳ�����C��Ӧʹ�ü����Լ�������SO2Cl2��ˮ��ˮ�⣬�ʼ�ʯ������������������SO2����ֹ�����е�ˮ��������B�У�
�ʴ�Ϊ����Һ©�����ţ������ݳ����ж���Cl2��SO2����ֹ�����е�ˮ��������C����ֹ��Ⱦ������������ˮ�⣻
��2�������װ�������Եķ����ǣ����ú�ѹ©���Ϸ������ӣ���������ƿ�ĵ����ܽ���ˮ�У��ƾ����ȣ����ܿ������ݲ�����ֹͣ���ȣ����ܿ���һ��Һ����������װ�õ����������ã�
�ʴ�Ϊ�����ú�ѹ©���Ϸ������ӣ���������ƿ�ĵ����ܽ���ˮ�У��ƾ����ȣ����ܿ������ݲ�����ֹͣ���ȣ����ܿ���һ��Һ����������װ�õ����������ã�
��3�������Ʊ�SO2��װ�ã�ͭ��Ũ���ᷴӦ��Ҫ���ȣ�����������SO2��������c.60% H2SO4+K2SO3���Ʊ�SO2����ѡc��
��4������ˮ�����ڱ���ʳ��ˮ����E�е��Լ��DZ���ʳ��ˮ��������ˮ���ڵ������¿ɽ�SO2���������ᣬ��������ԭΪHCl����Ӧ�ķ���ʽΪSO2+Cl2+2H2O=H2SO4+2HCl��
�ʴ�Ϊ������ʳ��ˮ��SO2+Cl2+2H2O=H2SO4+2HCl��
��5������е㲻ͬ��Һ�����������ķ��������Ա��л������뿪��ʵ�����������״���£�896mlCl2Ϊ0.04mol���������Ͽɵõ�0.04molSO2Cl2����Ϊ0.04��135g=5.4g������SO2Cl2�IJ�Ϊ$\frac{3.3g}{5.4g}$��100%=61.1%���ʴ�Ϊ������61.1%��
���� ���⿼��ʵ���Ʊ��������漰�Է�Ӧԭ����װ�ü������ķ������ۡ���������ʶ�����ʵķ����ᴿ�ȣ�ע�������������Ϣ��Ӧ�ã��Ѷ��еȣ�


 ͬ����ϰ���ϴ�ѧ������ϵ�д�
ͬ����ϰ���ϴ�ѧ������ϵ�д� ͬ����ϰ����ʦ����ѧ������ϵ�д�
ͬ����ϰ����ʦ����ѧ������ϵ�д� ����ϰ�⽭��ϵ�д�
����ϰ�⽭��ϵ�д� ѧ���쳵��������������������ϵ�д�
ѧ���쳵��������������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | a�ӷ���b��ˮ | B�� | a������b���� | C�� | a������b���� | D�� | a������b��ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ƹ���ˮ���� | B�� | ���ۻ���С����ˮ�����ζ� | ||
| C�� | ����ɫ��ζ���������� | D�� | ˮ��Һ��Ϊ��ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
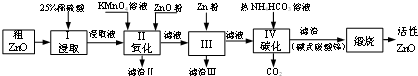
| Zn��OH��2 | Fe��OH��2 | Fe��OH��3 | Cu��OH��2 | |
| ��ʼ����pH | 5.4 | 7.0 | 2.3 | 4.7 |
| ��ȫ����pH | 8.0 | 9.0 | 4.1 | 6.7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Al��OH��3 | B�� | Al2O3 | C�� | H2SiO3 | D�� | MgCO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������������ά | |
| B�� | ��̬�⻯����ȶ��ԣ����������� | |
| C�� | �����£����ҵĵ��ʾ�����ˮ���ҷ�Ӧ | |
| D�� | �������ԭ���������28 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com