


 ϰ�⾫ѡϵ�д�
ϰ�⾫ѡϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ | B������Һ |
| C������Һ | D����Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
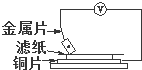 ���ྻ�Ľ���ƬA��B��C��D�ֱ�����ڽ���ʳ����Һ����ֽ���沢ѹ��������ͼ��ʾ������ÿ��ʵ��ʱ����¼��ѹ��ָ����ƶ�����͵�ѹ���Ķ������£�
���ྻ�Ľ���ƬA��B��C��D�ֱ�����ڽ���ʳ����Һ����ֽ���沢ѹ��������ͼ��ʾ������ÿ��ʵ��ʱ����¼��ѹ��ָ����ƶ�����͵�ѹ���Ķ������£�| ���� | �������� | ��ѹ/V |
| A | Cu��A | +0.78 |
| B | B��Cu | -0.30 |
| C | Cu��C | +1.35 |
| D | Cu��D | +0.15 |
| A����������ǿ������˳��Ϊ��C��A��B��D |
| B������B���ܴ�CuSO4��Һ���û�������ͭ |
| C���Ž���CʱͭƬ�Ϸ����ķ�ӦΪ��Cu-2e-=Cu2+ |
| D������D���淴ӦΪ��O2+2H2O+4e-=4OH- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����2.0mLŨ�Ⱦ�Ϊ0��lmol/L��KCl��KI�����Һ�еμ�l��2��0.01mol/LAgNO3��Һ���������ʻ�ɫ��˵��AgCl���ܽ�ȱ�AgI���ܽ��С |
| B���ֱ���Na2CO3��NaHCO3�������ʵ���Һ�У�������������ʯ��ˮ�����������������ְ�ɫ���� |
| C����0.1mol/L FeSO4��Һ�еμ���������KMnO4��Һ��KMnO4��Һ��ɫ��˵��Fe2+���������� |
| D�����ˮ�еμ�CCl4�����ú�ֲ㣬CCl4����Ϻ�ɫ��˵������CCl4�ӵ�ˮ����ȡ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��һδ֪����ɫ��Һ��ֻ���ܺ������������е������֣�������ˮ���������H+��OH-����H+��NH4+��K+��Mg2+��Cu2+��Al3+��NO3-��CO32-��SO42-����ȡ����100mL��Һ��������ʵ�飺
��һδ֪����ɫ��Һ��ֻ���ܺ������������е������֣�������ˮ���������H+��OH-����H+��NH4+��K+��Mg2+��Cu2+��Al3+��NO3-��CO32-��SO42-����ȡ����100mL��Һ��������ʵ�飺| ���� | H+ | NH4+ | K+ | Mg2+ | Cu2+ | Al3+ |
| c/mol?L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| 180-200�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����³�ѹ�£�8gO2�����Ϊ5.6L |
| B����״���£�22.4LCCl4�����ķ�����ΪNA |
| C����״���£�1.8gH2 O�к��е�����ΪNA |
| D�����³�ѹ�£�10g�������е�ԭ����ΪNA |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com