
分类思想以及用分类思想研究一类物质的通性和特殊性是学习化学的一种重要思维方式和手段。以下是依据一定的分类标准,对某些物质与水反应情况进行分类的分类图。请根据你所学的知识,按要求填空: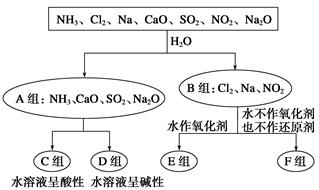
(1)上述第一级分类标准(分成A、B组的依据)是____________________。
(2)F组中物质除了Cl2外还有________(填化学式)。
(3)D组中的氨水呈弱碱性,用电离方程式表示其呈弱碱性的原因:
______________________________________________________________。
(4)由Al3+制备Al(OH)3,最好不选择D组中的NaOH溶液,用离子方程式说明理由:_______________________________________________________。
(5)FeCl3的水溶液滴入沸水可得到以Fe(OH)3为分散质的红褐色胶体
①该红褐色胶体中Z(OH)3粒子的直径大小范围是______________。
②FeCl3溶液滴入沸水可得到Fe(OH)3红褐色胶体的反应的离子方程式是____________________________。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
用数轴表示化学知识,并按某种共性对化学物质进行分类,有
简明易记的效果。例如,根据碳素钢的含碳量,将其分为低碳钢、中碳钢、高碳钢,利用数轴分类法可将其表示为:
根据这一分类方法请回答:
(1)25℃将pH与溶液酸碱性的关系粗略地表示在如下数轴上: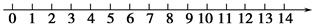
(2)某化学兴趣小组欲研究H2SO4、KCl、NaCl、Na2CO3、Na2SO3、NaOH六种物质的性质,对于如何研究,他们设计了两种研究方案:
方案Ⅰ:将它们按照酸、碱、盐分类,然后分别溶于水得到溶液,进行实验。
方法Ⅱ:将它们按照钠盐、钾盐和其他化合物分类,然后分别溶于水得到溶液,进行实验。
①根据方案Ⅰ进行分类时,经实验测得KCl、NaCl溶液的pH等于7;H2SO4溶液的pH小于7;Na2SO3、Na2CO3、NaOH溶液的pH大于7。由此有的同学按分类法思想把Na2SO3、Na2CO3与NaOH都划分为碱类是否合理?为什么? 。
②在方案Ⅰ中,某同学发现盐类物质中的KCl、NaCl在与其他物质混合时现象相同,无法区分,请设计一种简单的方法区分这两种物质 。
③在方案Ⅱ中,三种钠盐用其他物质中的 可加以区分,有关反应的化学方程式分别为 。
④该兴趣小组中的一位同学认为,还可以根据是否含有钠元素将上述六种物质分为Na2SO3、Na2CO3、NaCl、NaOH和H2SO4、KCl两类。在用H2SO4鉴别四种含钠元素的物质时,Na2SO3和Na2CO3很容易得到了区分,但鉴别NaCl和NaOH时却陷入了困境,请设计一个实验来解决这一难题: 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(1)下列说法不正确的是________(填字母序号)。
| A.60周年国庆阅兵车HQE顶级红旗采用全铝车身,铝的氧化物属于碱性氧化物 |
| B.用热的纯碱溶液洗涤沾有油污的器具时发生的主要是化学变化 |
| C.英国华裔科学家高锟因在“光在纤维中的传输应用于光学通信方面”做出了突破性成就,而获得了2009年诺贝尔物理学奖,光纤制品的基本原料为SiO2 |
| D.液氨、液氯、液态氯化氢都是非电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
实验室里常用的干燥剂有:①生石灰,②固体氢氧化钠,③变色硅胶[主要成分是二氧化硅,在其中掺入少量的无水氯化钴(CoCl2)作指示剂],④五氧化二磷,⑤无水氯化钙,⑥浓硫酸,⑦碱石灰(主要成分是氢氧化钠、氧化钙)等。
(1)上述物质中,属于纯净物的是__________。
A.①②④ B.②④⑥ C.①②④⑤ D.全部
(2)上述②、④、⑤、⑥四种干燥剂中,其主要化学成分所属的类别依次为______、________、________、______。(填序号)
A.酸 B.碱 C.盐 D.氧化物
(3)硅胶中无水氯化钴(CoCl2)呈蓝色,吸水后变为粉红色的CoCl2?6H2O,该变化过程属于____________(填“物理变化”或“化学变化”)。
(4)下列气体中,能用固体氢氧化钠干燥的是( )
A.CO2 B.HCl C.NO2 D.NH3 E.NO
(5)生石灰常用作食品干燥剂,久置后易失去干燥能力,其原因为_________________ (用化学方程式表示)
(6)上述干燥剂中,仅有浓硫酸为液体干燥剂,下列关于浓硫酸的叙述正确的是( )
A.浓硫酸具有吸水性,因而能使蔗糖炭化
B.浓硫酸在常温下可迅速与铜片反应放出二氧化硫气体
C.浓硫酸为液体干燥剂,干燥效率高,能用于干燥所有的气体
D.浓硫酸在常温下能够使铁、铝等金属钝化
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
胶体是一种重要的分散系。
(1)制备Fe(OH)3胶体是向煮沸的蒸馏水中逐滴加入 溶液,继续煮沸至 ,停止加热。
(2)向Fe(OH)3胶体中加入某种溶液,出现沉淀,继续滴加该溶液后沉淀溶解。滴入的溶液可能是 。
| A.NaOH溶液 | B.稀H2SO4 | C.Na2SO4溶液 | D.乙醇溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(14分)NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
(1)NH4Al(SO4)2可作净水剂,其理由是____________________________________________(用必要的化学用语和相关文字说明)。
(2)相同条件下,0.1 mol·L-1NH4Al(SO4)2中c(NH4+)________(填“等于”、“大于”或“小于”)0.1 mol·L-1NH4HSO4中c(NH4+))。
(3)如图是0.1 mol·L-1四种电解质溶液的pH随温度变化的图像。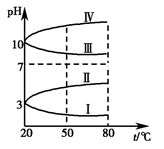
①其中符合0.1 mol·L-1NH4Al(SO4)2的pH随温度变化的曲线是________(填写序号),导致pH随温度变化的原因是____________________________;
②20 ℃时,0.1 mol·L-1NH4Al(SO4)2中2c(SO42-)-c(NH4+))-3c(Al3+)=________。(计算精确值)(4)室温时,向100 mL 0.1 mol·L-1 NH4HSO4溶液中滴加0.1 mol·L-1 NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示: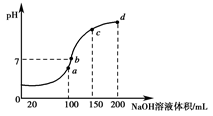
试分析图中a、b、c、d四个点,水的电离程度最大是________点;在b点,溶液中各离子浓度由大到小的排列顺序是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
FeCl3是一种用途比较广泛的盐。
(1)印刷电路板是由高分子材料和铜箔复合而成。刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,生成CuCl2和FeCl2。请写出反应的离子方程式 。
(2)FeCl3在天然水中可生成氢氧化铁胶体,其沉降水中悬浮物的速度高于铝盐(如硫酸铝等),是城市污水及工业废水处理的高效絮凝剂。实验室制取氢氧化铁胶体的方法是 (填字母序号)。
| A.将饱和的FeCl3溶液滴入沸水中,生成棕黄色液体即可。 |
| B.在FeCl3溶液中加入足量的NaOH溶液 |
| C.将饱和的FeCl3溶液滴入沸水,并继续煮沸至生成红褐色液体 |
| D.将饱和的FeCl3溶液滴入沸水,并继续煮沸至生成红褐色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列离子方程式正确的是
| A.实验室用大理石与醋酸反应制取二氧化碳:CaCO3+2H+=Ca2++CO2↑+H2O |
| B.氯乙酸与氢氧化钠溶液共热: CH2ClCOOH+OH- →CH2ClCOO-+H2O |
C.苯与浓硫酸、浓硝酸的混合液共热制硝基苯: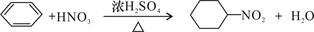 |
| D.用银氨溶液检验乙醛中的醛基: |
 CH3COO-+NH4+ +3NH3+2Ag↓+ H2O
CH3COO-+NH4+ +3NH3+2Ag↓+ H2O查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是
| A.电力、蒸汽都属于二次能源 |
| B.蔗糖、油脂及它们的水解产物均为非电解质 |
| C.合成纤维、光导纤维都是高分子化合物 |
| D.煤的气化和液化都是物理变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com