
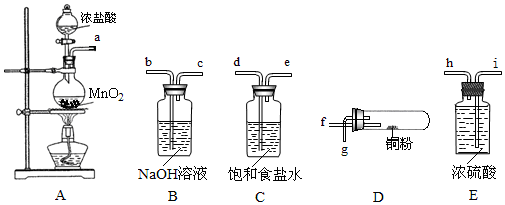
���� ������ͭ�۷�Ӧ��ʵ�飺MnO2��Ũ������ȡ��Cl2����HCl��H2O���ñ���ʳ��ˮ��ȥHCl����Ũ�����ȥH2O��Ȼ��Cl2��Cu��Ӧ�������NaOH��Һ����δ��Ӧ��Cl2����ֹ��Ⱦ�������ݴ˷�����
��� �⣺��1��װ��A����ȡ����������������Ũ���ᷢ����Ӧ�����Ȼ��̡�������ˮ����Ӧ����ʽΪMnO2+4HCl$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O��
�ʴ�Ϊ��MnO2+4HCl$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O��
��2����������˳��Cl2����װ�á���ȥHCl����װ�á�����װ�á��Ʊ�װ�á�����Cl2����װ�ã�MnO2��Ũ������ȡ��Cl2����HCl��H2O���ñ���ʳ��ˮ��ȥHCl����Ũ�����ȥH2O��Ȼ��Cl2��Cu��Ӧ�������NaOH��Һ����δ��Ӧ��Cl2����ֹ��Ⱦ������������������������ӿ�˳���ǣ�a��d��e��i��h��f��g��b��
�ʴ�Ϊ��d��e��i��h��f��g��b��
��3��װ��C�б���ʳ��ˮ�������dz�ȥ�Ȼ��⣬��С�������ܽ��ԣ�
�ʴ�Ϊ����ȥ�Ȼ��⣬��С�������ܽ��ԣ�
��4��װ��B��Ϊ���������������������Ȼ��ƺʹ������Ƶķ�Ӧ�����ӷ���ʽΪ��Cl2+2OH-�TCl-+ClO-+H2O��
�ʴ�Ϊ��Cl2+2OH-�TCl-+ClO-+H2O��
��5������װ��Dʱ��ͭ�۷�����Ӧ�Ļ�ѧ����ʽΪCl2+Cu$\frac{\underline{\;\;��\;\;}}{\;}$CuCl2���ʴ�Ϊ��Cl2+Cu$\frac{\underline{\;\;��\;\;}}{\;}$CuCl2��
���� ���⿼�������ʵ��Ʊ����漰������ʵ�����Ʒ�����ѧ���ʣ�װ�õ�ѡ���������������Ǹ߿����ȵ㣬ע��֪ʶ�Ļ�����Ŀ�ѶȲ���


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��С | B�� | ��� | C�� | ���� | D�� | ��ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C+O2$\stackrel{��ȼ}{��}$CO2 | B�� | C��s��+O2��g��$\stackrel{��ȼ}{��}$CO2��g��+393.5kJ | ||
| C�� | C��s��+O2��g��$\stackrel{��ȼ}{��}$CO2��g�� | D�� | C��s��+O2��g��=CO2��g��+393.5kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��֪2H2��g��+O2��g���T2H2O��g����H=-483.6 kJ/mol����H2��ȼ����Ϊ-241.8 kJ/mol | |
| B�� | ��֪C��ʯī��s���TC�����ʯ��s����H��0������ʯ��ʯī�ȶ� | |
| C�� | ��20.0g NaOH��ϡ��Һ��ϡ������ȫ�кͣ��ų�28.7 kJ����������÷�Ӧ���Ȼ�ѧ����ʽΪ��NaOH��aq��+HCl��aq���TNaCl��aq��+H2O��l����H=-57.4 kJ/mol | |
| D�� | ��֪2SO2��g��+O2��g��?2SO3��g����H=-QkJ•mol-1��Q��0������2mol SO2��g����1mol O2��g������һ�ܱ������г�ַ�Ӧ��ų�QkJ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��3-��-3-�촼
��3-��-3-�촼 ��4-��-2-��ϩ
��4-��-2-��ϩ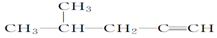 ��4-��-1-��Ȳ
��4-��-1-��Ȳ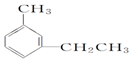 ��1-��-3-�ұ��������ұ�����
��1-��-3-�ұ��������ұ������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������Ʋ���¶���ڿ����У�Ҫ�ܷⱣ�� | |
| B�� | ʣ��Ľ�����Ӧ�Ż�ԭ�Լ�ƿ | |
| C�� | �����Ӧ�ܷⱣ���ڲ���ƿ�� | |
| D�� | ʵ���ұ���FeCl2ʱ�������м�����м |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
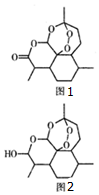 2011��9��12�գ��й���ѧ�������ϻ���˹��һ�ұ����ٴ�ҽѧ�о������Ա�����������һ��ҩ��--�����أ������ɾտ�ֲ���ڵ�������������������һ�ֻ����������ű������Чҩ����ṹͲʽ��ͼ1��ʾ�������й������ص�˵��������ǣ�������
2011��9��12�գ��й���ѧ�������ϻ���˹��һ�ұ����ٴ�ҽѧ�о������Ա�����������һ��ҩ��--�����أ������ɾտ�ֲ���ڵ�������������������һ�ֻ����������ű������Чҩ����ṹͲʽ��ͼ1��ʾ�������й������ص�˵��������ǣ�������| A�� | ������������������ˮ�����������ѡ������������л��ܼ� | |
| B�� | �����ط����ڵ�1�����������ǶԸ�űԭ��ĺ��Ļ��� | |
| C�� | 1mol�����ط����ڼ��������³���ˮ��������1mol����ˮ | |
| D�� | ҩЧ�������ظ�10����˫�������أ���ͼ2����ѧʽΪC15H24O5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
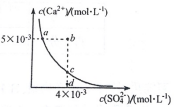 �����£�Ksp��CaSO4��=9 �� 10?6��CaSO4 ��ˮ��Һ�еij����ܽ�ƽ��������ͼ��ʾ������˵������ȷ���ǣ�������
�����£�Ksp��CaSO4��=9 �� 10?6��CaSO4 ��ˮ��Һ�еij����ܽ�ƽ��������ͼ��ʾ������˵������ȷ���ǣ�������| A�� | b ������г������� | |
| B�� | a ���Ӧ��Ksp ����c ���Ӧ��Ksp | |
| C�� | ��d ����Һ�м���һ������CaCl2���ܻ��г������� | |
| D�� | CaSO4 �ܽ���ˮ�У�һ����c��Ca2+��=c��SO42-��=3��10-3mol•L-1 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com