
| V |
| Vm |
| n |
| V |
| 44.8L |
| 22.4L/mol |
| 2mol |
| 0.5L |


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 的系统命名是:
的系统命名是: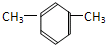 的名称是
的名称是 的系统命名是
的系统命名是查看答案和解析>>
科目:高中化学 来源: 题型:
- 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH4 |
| B、C2H6 |
| C、C3H6 |
| D、C3H8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、2HgO
| ||||
B、2NaCl(熔融)
| ||||
C、2MgO(熔融)
| ||||
D、Fe2O3+3CO
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该晶体类型是原子晶体 |
| B、该晶体中碳原子和氧原子的个数比为1:2 |
| C、每摩尔该晶体中含4molC-O |
| D、晶体的空间最小环共有6个原子构成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com