
| A. | 硝酸、纯碱、胆矾、铜 | B. | 硫酸、烧碱、小苏打、纯碱 | ||
| C. | 盐酸、乙醇、氯化钠、碘酒 | D. | 醋酸、漂白粉、石灰石、二氧化碳 |
分析 根据酸、碱、盐、电解质的组成特点进行分析;电离时生成的阳离子都是氢离子的化合物是酸,电离时生成的阴离子都是氢氧根离子的化合物是碱,由金属离子(或铵根离子)和酸根离子组成的化合物是盐,在水溶液中或熔融状态下能导电的化合物是电解质.
解答 解:A、硝酸属于酸,纯碱属于盐不是碱,胆矾即硫酸铜晶体属于盐,铜是单质不是电解质,故A错误;
B、硫酸电离时生成的阳离子都是氢离子,属于酸;烧碱即氢氧化钠,属于碱;小苏打即碳酸氢钠属于盐,纯碱即碳酸钠属于盐是电解质,故B正确;
C、盐酸是HCl的水溶液,乙醇属于有机物不是碱,氯化钠属于盐,碘酒是混合物不是电解质,故C错误;
D、醋酸属于酸;漂白粉是氯化钙和次氯酸钙的混合物,不属于碱;石灰石的主要成分是碳酸钙,属于盐,二氧化碳在水溶液中和熔融状态下都不导电的化合物,属于非电解质,故D错误;
故选B.
点评 本题考查了酸、碱、盐、电解质的判别方法,要依据各种化合物的组成特点加以判断,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,2.24L CCl4中含有的分子数为0.1NA | |
| B. | 常温常压下,46 g NO2气体中含有原子数为3NA | |
| C. | 18 g重水(D2O)中含有的电子数为10NA | |
| D. | 1 molNa2O2与足量水蒸气反应转移电子总数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 ,所含化学键类型为离子键、共价键.向甲中滴加足量水时发生反应的化学方程式是2Na2O2+2H2O=4NaOH+O2↑.
,所含化学键类型为离子键、共价键.向甲中滴加足量水时发生反应的化学方程式是2Na2O2+2H2O=4NaOH+O2↑.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
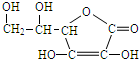
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | X的氢化物比Z的氢化物熔、沸点低 | |
| B. | Y的原子半径比X的原子半径小 | |
| C. | 四种元素的氢化物中,X的氢化物受热最难分解 | |
| D. | R所在周期的元素种数为32种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 冬天,块状锌与2 mol•L-1硫酸溶液反应 | |
| B. | 冬天,粉末状锌与2 mol•L-1硫酸溶液反应 | |
| C. | 夏天,块状锌与2 mol•L-1硫酸溶液反应 | |
| D. | 夏天,粉末状锌与2mol•L-1硫酸溶液反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com