

分析 工业生产碘酸钾的流程:用碘和氯酸钾溶液反应生成碘酸氢钾、氯化钾和氯气,再加入硝酸,加热促使氯气从反应体系中逸出,经冷却结晶,过滤得碘酸氢钾晶体,将碘酸氢钾晶体溶于水,加入氢氧化钾溶液,使碘酸氢钾生成碘酸钾,过滤后得碘酸钾溶液,将滤液进行蒸发浓缩、冷却结晶、过滤洗涤,可得碘酸钾晶体,
(1)反应中I2→KH(IO3)2,I元素化合价由0价升高为+5价,共升高10价.KClO3→KCl、Cl2,氯元素化合价降低,还原产物为KCl、Cl2,KClO3→KCl氯元素化合价由+5降低为-1价,化合价降低6价,KClO3→Cl2氯元素化合价由+5降低为0价,化合价总共降低10价,二者获得的电子数目相同,获得电子最小公倍数为30,则KCl的系数为5,Cl2的系数为3,所以化合价降低60价,故I2系数为6,根据元素守恒配平KClO3、H2O、KH(IO3)2的系数;
(2)酸性条件下碘酸钾是一种较强的氧化剂,HI具有还原性,但是硝酸不具备;
(3)由题中信息可知,在碱性条件下碘酸钾能被氯气氧化为高碘酸钾;
(4)从溶液中获得晶体一般的步骤为蒸发浓缩、冷却结晶、过滤洗涤、干燥.
解答 解:工业生产碘酸钾的流程:用碘和氯酸钾溶液反应生成碘酸氢钾、氯化钾和氯气,再加入硝酸,加热促使氯气从反应体系中逸出,经冷却结晶,过滤得碘酸氢钾晶体,将碘酸氢钾晶体溶于水,加入氢氧化钾溶液,使碘酸氢钾生成碘酸钾,过滤后得碘酸钾溶液,将滤液进行蒸发浓缩、冷却结晶、过滤洗涤,可得碘酸钾晶体,
(1)反应中I2→KH(IO3)2,I元素化合价由0价升高为+5价,共升高10价.KClO3→KCl、Cl2,氯元素化合价降低,还原产物为KCl、Cl2,KClO3→KCl氯元素化合价由+5降低为-1价,化合价降低6价,KClO3→Cl2氯元素化合价由+5降低为0价,化合价总共降低10价,二者获得的电子数目相同,获得电子最小公倍数为30,则KCl的系数为5,Cl2的系数为3,所以化合价降低共60价,故I2系数为6,根据氯元素守恒可知KClO3系数为11,根据碘元素守恒可知KH(IO3)2的系数为6,根据氢元素守恒可知H2O、系数为3,检查氧元素守恒,故方程式为:6I2+11KClO3+3H2O=6KH(IO3)2+5KCl+3Cl2↑,电子转移方向和数目为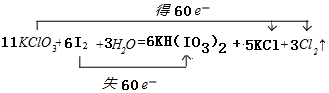 ,
,
故答案为:6,11,3,6;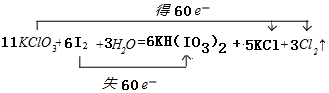 ;
;
(2)步骤中产生氯气,需要将氯气排出反应体系,加入硝酸的目的是制造酸性环境,促进氯气从反应体系中逸出,酸性条件下碘酸钾是一种较强的氧化剂,HI具有还原性,能将已生成的碘酸氢钾还原,
故答案为:HI具有还原性能将已生成的碘酸氢钾还原;
(3)由题中信息可知,在碱性条件下碘酸钾能被氯气氧化为高碘酸钾,所以应将氯气排出,
故答案为:反应产生氯气跟KOH反应生成KClO,KClO能将KIO3氧化成KIO4,从而不能得到KIO3;
(4)从溶液中获得晶体一般的步骤为蒸发浓缩、冷却结晶、过滤洗涤、干燥,故操作顺序是A、B、D,
故答案为:A、B、D.
点评 本题以工业生产碘酸钾为载体,为高频考点,侧重于学生的分析能力、实验能力和计算能力的考查,内容涉及方程式配平、对工艺流程的理解评价、方案设计等,难度中等,是对知识的综合运用和能力的考查.


 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源: 题型:实验题
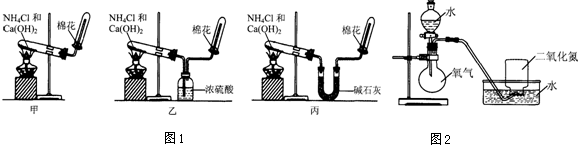
| 实验过程 | 实验现象 | |
| 步骤一 | 将收集满NO2的集气瓶倒立在水槽中. | 集气瓶中液面上升;集气瓶中气体由红棕色变成无色;最终剩余气体约占集气瓶体积的三分之一. |
| 步骤二 | 将分液漏斗中的水逐滴滴入烧瓶,使少量O2进入盛有NO2的集气瓶后,停止滴水. | 集气瓶中气体颜色的变化情况是先由无色变为红棕色,再变成无色;集气瓶中液面继续上升. |
| 步骤三 | 多次重复步骤二操作,并依次减少O2通入量,直至O2通入后,气体不再变成红棕色. | 现象与步骤二相同,最后集气瓶内几乎充满液体,只含极少量气体. |
| 计算 | 用上述实验方法,将标准状况下448mLNO2全部溶于水,得到500mL溶液,则溶液中HNO3的物质的量浓度为0.04mol/L. | |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
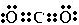 ,将其转变其他化工原料,必须破坏的化学键属于极性(填“极性”或“非极性”)键.
,将其转变其他化工原料,必须破坏的化学键属于极性(填“极性”或“非极性”)键.| 共价键 | H-H | H-F | H-Cl | H-Br | H-O | H-S | H-N | H-P |
| 键长(pm) | 74 | 92 | 127 | 141 | 98 | 135 | 101 | 321 |
| 键能(kJ/mol) | 436 | 568 | 432 | 368 | 464 | 364 | 391 | 142 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | C3H8中碳原子都采用的是sp3杂化 | |
| B. | O2、CO2、N2都是非极性分子 | |
| C. | 酸性:H2CO3<H3PO4<H2SO4<HClO | |
| D. | CO的一种等电子体为NO+,它的电子式为+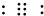 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液、萃取、蒸馏 | B. | 分液、蒸馏、萃取 | C. | 蒸馏、分液、萃取 | D. | 蒸馏、萃取、分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由非金属元素组成的化合物不一定都是共价化合物 | |
| B. | 共价化合物中一定含有极性键 | |
| C. | 含有离子键的化合物一定是离子化合物 | |
| D. | 所有气体单质分子中一定含有非极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某离子晶体晶胞结构如图所示,x位于立方体的顶点,Y位于立方体中心.试分析:
某离子晶体晶胞结构如图所示,x位于立方体的顶点,Y位于立方体中心.试分析:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com