
·ÖĪö £Ø1£©2NaNO2+4HIØT2NO+I2+2NaI+2H2OÖŠ£¬NŌŖĖŲµÄ»ÆŗĻ¼Ū½µµĶ£¬IŌŖĖŲµÄ»ÆŗĻ¼ŪÉżøߣ»
£Ø2£©NaNO2Ö±½ÓÅÅ·Å»įŌģ³ÉĪŪČ¾£¬ŠčŅŖ¾ßÓŠ»¹ŌŠŌµÄĪļÖŹ½«ĘäŃõ»ÆÉś³ÉµŖĘų£»
£Ø3£©µČĪļÖŹµÄĮæÅØ¶ČµÄNaOHŗĶNa2CO3µÄ»ģŗĻČÜŅŗÖŠŗ¬ÓŠĒāŃõ»ÆÄĘÓėĢ¼ĖįÄʵÄĪļÖŹµÄĮæĻąµČ£¬Ļ”ŃĪĖį¼ÓČėµ½NaOHŗĶNa2CO3µÄ»ģŗĻČÜŅŗÖŠ£¬ŃĪĖįĻČÓėĒāŃõ»ÆÄĘ·¢ÉśĖį¼īÖŠŗĶ£¬Ź£ÓąµÄŃĪĖįŌŁÓėĢ¼ĖįÄĘ·¢Éś·“Ó¦£¬ŃĪĖįÉŁĮæŹ±·¢Éś·“Ó¦CO32-+H+=HCO3-£¬ŃĪĖį¹żĮæŹ±·¢Éś·“Ó¦£ŗCO32-+2H+=CO2”ü+H2O£¬ŅŌ“ĖĄ“½ā“š£®
½ā“š ½ā£ŗ£Ø1£©2NaNO2+4HIØT2NO+I2+2NaI+2H2OÖŠ£¬NŌŖĖŲµÄ»ÆŗĻ¼Ū½µµĶ£¬IŌŖĖŲµÄ»ÆŗĻ¼ŪÉżøߣ¬ŌņNaNO2ĪŖŃõ»Æ¼Į£¬Ńõ»Æ¼ĮÓė»¹Ō¼ĮµÄĪļÖŹµÄĮæÖ®±ČĪŖ1£ŗ1£¬ÓŠ1.75molµÄ»¹Ō¼Į±»Ńõ»Æ£¬Ōņ±»»¹ŌµÄŃõ»Æ¼ĮÓŠ1.75mol£¬
¹Ź“š°øĪŖ£ŗ1.75£»
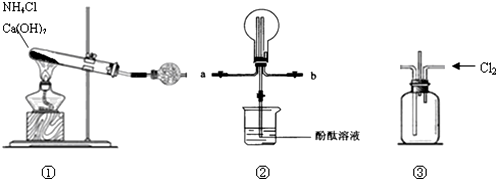
£Ø2£©NaNO2Ö±½ÓÅÅ·Å»įŌģ³ÉĪŪČ¾£¬ŠčŅŖ¾ßÓŠ»¹ŌŠŌµÄĪļÖŹ½«ĘäŃõ»ÆÉś³ÉµŖĘų£¬ŌņŃ”ŌńĀČ»Æļ§¼“æÉ£¬·¢ÉśNaNO2+NH4ClØTNaCl+N2”ü+2H2O£¬ĘäӹєĻī²»·ūŗĻ£»“Ė·ĻĖ®³ŹĒæ¼īŠŌ£¬Ščµ÷½ŚČÜŅŗµÄpH½Ó½üÖŠŠŌ£¬ŌŁĢķ¼ÓĀČ»Æļ§ČÜŅŗ£¬·¢ÉśNH4++OH-=NH3”ü+H2O£¬·ńŌņ»įŅżĘš¶ž“ĪĪŪČ¾£¬
¹Ź“š°øĪŖ£ŗ¢Ś£»NaNO2+NH4ClØTNaCl+N2”ü+2H2O£»NH4++OH-=NH3”ü+H2O£»
£Ø3£©A£®ÉčNaOHŗĶNa2CO3µÄĪļÖŹµÄĮ涼ĪŖ1mol£¬Ōņ¼ÓČėŃĪĖįÉŁĮ棬ĻČ·¢Éś·“Ó¦£ŗOH-+H+=H2O£¬1molĒāŃõ»ÆÄĘĻūŗÄ1molŃĪĖį£¬ŌŁ·¢Éś·“Ó¦CO32-+H+=HCO3-£¬½«Į½øö·½³ĢŹ½Ļą¼ÓµĆ£ŗOH-+CO32-+2H+=HCO3-+H2O£¬¹ŹAÕżČ·£»
B£®ÉčNaOHŗĶNa2CO3µÄĪļÖŹµÄĮ涼ĪŖ2mol£¬Ōņ¼ÓČėŃĪĖįÉŁĮ棬ĻČ·¢Éś·“Ó¦£ŗ2OH-+2H+=2H2O£¬2molĒāŃõ»ÆÄĘĻūŗÄ2molŃĪĖį£¬ŌŁ·¢Éś·“Ó¦CO32-+H+=HCO3-£¬ŃĪĖį²»×ćÖ®ĻūŗÄ1molĢ¼ĖįÄĘ£¬½«Į½øö·½³ĢŹ½Ļą¼ÓµĆ£ŗ2OH-+CO32-+3H+=HCO3-+2H2O£¬¹ŹBÕżČ·£»
C£®ÉčNaOHŗĶNa2CO3µÄĪļÖŹµÄĮ涼ĪŖ2mol£¬2molĒāŃõ»ÆÄĘĻūŗÄ2molĒāĄė×Ó£¬Ź£Óą2molĒāĄė×ÓÓė2molĢ¼ĖįÄĘ·“Ӧɜ³É2molĢ¼ĖįĒāøłĄė×Ó£¬Ąė×Ó·½³ĢŹ½Ó¦ĪŖ2OH-+2CO32-+4H+=2HCO3-+2H2O£¬¼“OH-+CO32-+2H+=HCO3-+H2O£¬¹ŹC“ķĪó£»
D£®ÉčNaOHŗĶNa2CO3µÄĪļÖŹµÄĮ涼ĪŖ1mol£¬Ōņ¼ÓČėŃĪĖį¹żĮ棬ĻČ·¢Éś·“Ó¦£ŗOH-+H+”śH2O£¬1molĒāŃõ»ÆÄĘĻūŗÄ1molŃĪĖį£¬ŌŁ·¢Éś·“Ó¦CO32-+2H+=CO2”ü+H2O£¬½«Į½øö·½³ĢŹ½Ļą¼ÓµĆ£ŗOH-+CO32-+3H+=CO2”ü+2H2O£¬¹ŹDÕżČ·£»
¹Ź“š°øĪŖ£ŗC£®
µćĘĄ ±¾Ģāæ¼²éŃõ»Æ»¹Ō·“Ó¦ŗĶĄė×Ó·“Ó¦£¬ĪŖøßĘµæ¼µć£¬Ć÷Č··“Ó¦ÖŠŌŖĖŲµÄ»ÆŗĻ¼Ū±ä»ÆŹĒ½ā“š±¾ĢāµÄ¹Ų¼ü£¬²ąÖŲ»ł±¾øÅÄīµÄ漲飬עÖŲÖŖŹ¶ĒØŅĘÓ¦ÓĆ£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
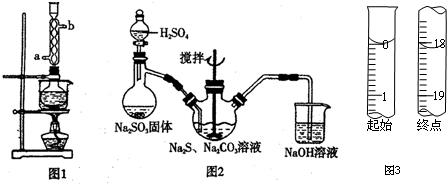
| ŹµŃé²½Öč | ÓŠ¹ŲĪŹĢā |
| ¢Ł¼ĘĖćĖłŠčNa2SO4µÄÖŹĮæ | ŠčŅŖ³ĘĮæNa2SO4µÄÖŹĮæĪŖ14.2æĖ |
| ¢Ś³ĘĮæNa2SO4¹ĢĢå | ³ĘĮæŠčŅŖÓƵ½µÄÖ÷ŅŖŅĒĘ÷ŹĒ£ŗĶŠÅĢĢģĘ½ŗĶŅ©³× |
| ¢Ū½«Na2SO4¼ÓČė100mLÉÕ±ÖŠ£¬²¢¼ÓČėŹŹĮæĖ® | ĪŖĮĖ¼ÓæģČܽāĖŁĀŹ£¬æÉŅŌ²ÉČ”ÄÄŠ©“ėŹ©£ŗ ÓĆ²£Į§°ō½Į°č |
| ¢Ü½«ÉÕ±ÖŠČÜŅŗ×ŖŅĘÖĮ500mLČŻĮæĘæÖŠ | ĪŖĮĖ·ĄÖ¹ČÜŅŗ½¦³ö£¬Ó¦²ÉČ”Ź²Ć““ėŹ©£ŗ ×ŖŅĘ¹ż³ĢÖŠÓĆ²£°ō½ųŠŠŅżĮ÷ |
| ¢ŻĻņČŻĮæĘæÖŠ¼ÓÕōĮóĖ®ÖĮæĢ¶ČĻß | ŌŚ½ųŠŠ“Ė²Ł×÷Ź±µ±¼ÓĖ®ÖĮæĢ¶ČĻß1-2ĄåĆד¦Ó¦ČēŗĪ²Ł×÷£ŗ øÄÓĆ½ŗĶ·µĪ¹Ü¼ÓĖ®ÖĮ°¼ŅŗĆęÓėæĢ¶ČĻßĻąĒŠ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ŹµŃé ±ąŗÅ | ŹµŃéĪĀ¶Č /”ę | Na2S2O3 | H2SO4 | ÕōĮóĖ®Ģå»ż /mL | ||
| Ģå»ż/mL | ÅضČ/mol•L-1 | Ģå»ż/mL | ÅضČ/mol•L-1 | |||
| ¢Ł | 25 | 10 | 0.1 | 10 | 0.1 | 0 |
| ¢Ś | 25 | 5 | 0.1 | 10 | 0.1 | 5 |
| ¢Ū | 25 | 5 | 0.2 | 10 | 0.2 | 5 |
| ¢Ü | 50 | 5 | 0.1 | 10 | 0.1 | 5 |
| ¢Ż | 50 | 10 | 0.2 | 5 | 0.2 | 5 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±½²»ÄÜŹ¹ĖįŠŌKMnO4ČÜŅŗĶŹÉ«£¬Óė¼×ĶéŠŌÖŹĻąĖĘ£¬Ņņ“Ė±½ĪŖ±„ŗĶĢž | |
| B£® | ±½µÄ½į¹¹¼ņŹ½ĪŖ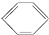 ÓŠČżøöĖ«¼ü£¬æÉÓėäåĖ®·¢Éś¼Ó³É·“Ó¦ ÓŠČżøöĖ«¼ü£¬æÉÓėäåĖ®·¢Éś¼Ó³É·“Ó¦ | |
| C£® | ±½µÄ6øöĢ¼Ō×ÓŗĶ6øöĒāŌ×ÓŌŚĶ¬Ņ»Ę½ĆęÄŚ | |
| D£® | ½«1 mL±½ŗĶ1 mLĖ®³ä·Ö»ģŗĻŗó¾²ÖĆ£¬¶žÕß»„ČÜ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
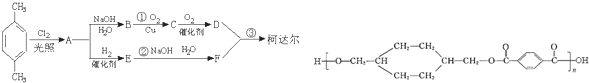
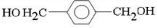 £»D
£»D £»E
£»E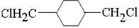
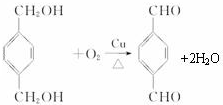 £¬·“Ó¦ĄąŠĶŃõ»Æ·“Ó¦
£¬·“Ó¦ĄąŠĶŃõ»Æ·“Ó¦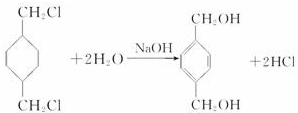 £¬·“Ó¦ĄąŠĶČ”“ś·“Ó¦
£¬·“Ó¦ĄąŠĶČ”“ś·“Ó¦ +
+ $\stackrel{Ņ»¶ØĢõ¼žĻĀ}{”ś}$
$\stackrel{Ņ»¶ØĢõ¼žĻĀ}{”ś}$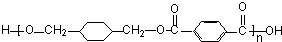 +£Ø2n-1£©H2O£¬·“Ó¦ĄąŠĶĖõ¾Ū·“Ó¦£®
+£Ø2n-1£©H2O£¬·“Ó¦ĄąŠĶĖõ¾Ū·“Ó¦£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| NaCl | MgCl2 | AlCl3 | SiCl4 | µ„ÖŹB | |
| ČŪµć/”ę | 810 | 710 | 190 | -68 | 2 300 |
| ·Šµć/”ę | 1 465 | 1418 | 182.7 | 57 | 2 500 |
| A£® | SiCl4ŹĒ·Ö×Ó¾§Ģå | B£® | µ„ÖŹBæÉÄÜŹĒŌ×Ó¾§Ģå | ||
| C£® | AlCl3¼ÓČČÄÜÉż»Ŗ | D£® | KClµÄČŪµć“óÓŚ810”ę |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā


 £»
£»²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | m+11 | B£® | m+4 | C£® | m-6 | D£® | m-5 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com