
【题目】甲、乙、丙、丁均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去),下列各组物质中不能按图示关系转化的是( )
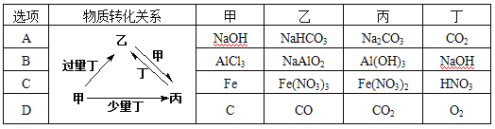
A.AB.BC.CD.D
【答案】D
【解析】
据钠、铝、铁、碳元素的单质及其化合物的转化关系分析判断,注意反应物用量对产物种类的影响。
A. 甲(NaOH)+过量丁(CO2)→乙(NaHCO3),甲(NaOH)+少量丁(CO2)→丙(Na2CO3)+H2O,乙(NaHCO3)+甲(NaOH)→丙(Na2CO3)+H2O,丙(Na2CO3)+丁(CO2)+H2O→乙(NaHCO3),A项能实现图示转化;
B. 甲(AlCl3)+过量丁(NaOH)→乙(NaAlO2)+NaCl+H2O,甲(AlCl3)+少量丁(NaOH)→丙(Al(OH)3)+NaCl,乙(NaAlO2)+甲(AlCl3)+H2O→丙(Al(OH)3)+NaCl,丙(Al(OH)3)+丁(NaOH)→乙(NaAlO2)+H2O,B项能实现图示转化;
C. 甲(Fe)+过量丁(HNO3)→乙[Fe(NO3)3]+NO+H2O,甲(Fe)+少量丁(HNO3)→丙[Fe(NO3)2]+NO+H2O,乙[Fe(NO3)3]+甲(Fe)→丙[Fe(NO3)2],丙[Fe(NO3)2]+丁(HNO3)→乙[Fe(NO3)3]+NO+H2O,C项能实现图示转化;
D. 甲(C)+过量丁(O2)→丙(CO2)而非乙(CO),甲(C)+少量丁(O2)→乙(CO)而非丙(CO2),乙(CO)+甲(C)→不反应,丙(CO2)+丁(O2)→不反应,D项不能实现图示转化。
本题选D。


 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:
【题目】氢气作为清洁能源有着广泛的应用前景,含硫天然气制备氢气的流程如图。

请回答下列问题:
Ⅰ.转化脱硫:将天然气压入吸收塔,30℃时,在T·F菌作用下,酸性环境中脱硫过程示意图如图。
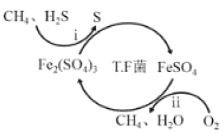
过程i的离子反应方程式为_____。
已知:①Fe3+在pH=1.9时开始沉淀,pH=3.2时沉淀完全。
②30℃时,在T·F菌作用下,不同pH的FeSO4溶液中Fe2+的氧化速率如表。
pH | 0.7 | 1.1 | 1.5 | 1.9 | 2.3 | 2.7 |
Fe2+的氧化速率 | 4.5 | 5.3 | 6.2 | 6.8 | 7.0 | 6.6 |
在转化脱硫中,请在表中选择最佳pH范围是____<pH<____,这样选择的原因是:______。
Ⅱ.蒸气转化:在催化剂的作用下,水蒸气将CH4氧化。结合如图回答问题。
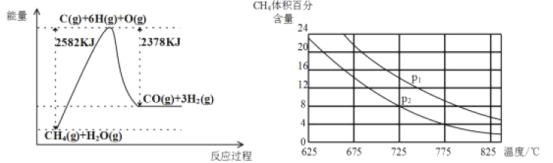
(3)①该过程的热化学方程式是_____。
②比较压强P1和P2的大小关系:P1____P2(选填“<”、“>”或“=”)。
Ⅲ.CO变换:500℃时,CO进一步与水反应生成CO2和H2。
Ⅳ.提纯:将CO2和H2分离得到H2的过程如示意图如图。
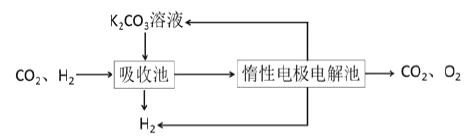
(4)吸收池中发生反应的离子方程式是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胡椒酚是植物挥发油中的一种成分。关于胡椒酚的下列说法:
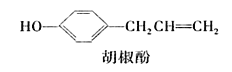
①该化合物属于芳香烃;
②分子中至少有7个碳原子处于同一平面;
③它的部分同分异构体能发生银镜反应;
④1 mol该化合物最多可与2 mol Br2发生反应。其中正确的是( )
A. ①③B. ①②④C. ②③D. ②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中溴元素以Br-形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如图:
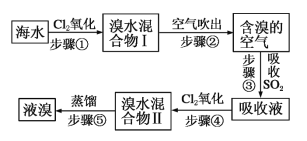
(1)步骤①反应的离子方程式是___________________。
(2)步骤③反应的化学方程式是___________________,从理论上考虑,下列也能吸收Br2的是___________________。
A.FeCl2 B.Na2SO3 C.H2O
(3)步骤①中已获得Br2,步骤③中又将Br2还原为Br-,步骤④又生成Br2,这样做的目的为___________________。
(4)已知海水中Br-含量为64mg/L,依据上述流程,若将10m3海水中的溴元素转化为工业溴,至少需要标准状况下Cl2的体积为___________________L(忽略Cl2的溶解)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组拟用下列装置做炼铁原理的实验,同时检测氧化铁的纯度(假设矿石中不含其他与CO反应的成分),并除去尾气。CO气体用H2C2O4![]() CO2↑+CO↑+H2O来制取,与Fe2O3反应的CO需纯净、干燥。
CO2↑+CO↑+H2O来制取,与Fe2O3反应的CO需纯净、干燥。
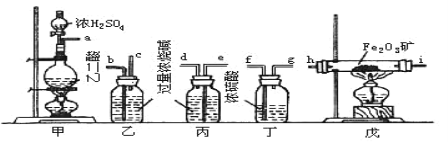
(1)若所制气体从左向右流向时,上述仪器组装连接的顺序是(用a、b…表示) 接 , 接 , 接 , 接 。___________________
(2)装置乙的作用是___________________;装置丙的目的是____________________。
(3)实验结束后,先熄灭戊处的酒精灯,再熄灭甲处的酒精灯,其主要原因是____________________。
(4)实验前氧化铁矿粉末为xg,实验后测得乙、丙质量分别增加yg和zg,则氧化铁的质量分数为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出至少六种,C与H原子个数比为1:2且相对分子量最小的不同类别的有机物的名称____、_____、____、_____、_____、______。
(2)有一种耐热型树脂材料的结构简式为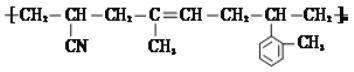
写出其合成单体除丙烯氰(CH2=CHCN)外,还需要的单体名称是:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 碳燃烧的热化学方程式为C(s)+1/2O2(g)=CO(g) ΔH=+110.5kJ·mol-1
B. 镀锌铁皮发生电化学腐蚀时,负极反应式为:Zn-2e–= Zn2+
C. NaHS水解的离子方程式是:HS﹣+H2O![]() S2﹣+H3O+
S2﹣+H3O+
D. 溶液中碳酸的电离方程式为:H2CO3![]() 2H++ CO32–
2H++ CO32–
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是( )
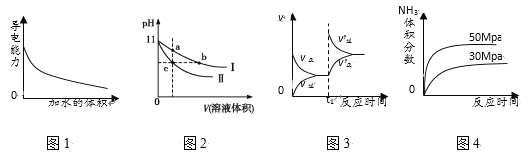
A. 图1表示一定量冰醋酸晶体加水过程中溶液导电性的变化
B. 图2表示某温度下,相同pH的氨水和氢氧化钠溶液分别加水稀释,a、b、c三点溶液的KW:c=b<a
C. 图3表示t1时刻改变的条件为升高温度,平衡向逆反应方向移动
D. 图4表示一定条件下,合成氨反应中压强对氨气体积分数的影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图A~J分别代表相关反应中的一种物质,已知A分解得到等物质的量的B、C、D,常温下B、D为气态化合物,C为液态化合物,图中有部分生成物未标出。已知﹕2Mg+CO2![]() 2MgO+C。
2MgO+C。
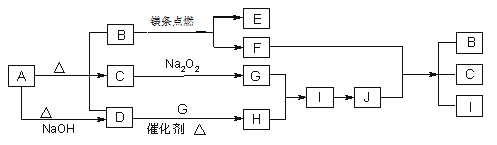
请回答下列问题:
(1)写出A的化学式:___。
(2)写出下列反应的化学方程式:
D+G→H___。
F+J→B+C+I___。
(3)写出A+NaOH→D的离子方程式___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com