
| A、Al(OH)3→Al2O3 |
| B、S→SO3 |
| C、Si→SiO2 |
| D、Na→Na2O |
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
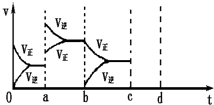 (1)如图表示在密闭容器中反应:2SO2+O2?2SO3△H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,ab过程中改变的条件可能是
(1)如图表示在密闭容器中反应:2SO2+O2?2SO3△H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,ab过程中改变的条件可能是| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
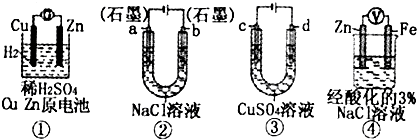
| A、装置①中,溶液中的Zn2+移向Cu电极 |
| B、装置②工作一段时间后,a极附近溶液的pH增大 |
| C、用装置③精炼铜时,c极为粗铜 |
| D、装置④中电子由Zn沿导线流向Fe,溶液中有Fe2+生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、参加反应物质的性质是决定化学反应速率的主要因素 |
| B、化学反应速率只能加快不能减慢 |
| C、决定化学反应速率的主要因素是浓度 |
| D、增加反应物的用量一定能增大反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、实验室用氯化铁溶液制取氢氧化铁胶体:Fe3++3H2O
| ||||
| B、碳酸钙溶于醋酸:CaCO3+2H+═Ca2++H2O+CO2↑ | ||||
| C、铝和烧碱溶液:2Al+2OH-+2H2O═2Al3++3H2↑ | ||||
| D、AlCl3溶液中加入过量氨水:Al3++4OH-═AlO2-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol/L NH4Cl溶液:c(NH4+ )=c(Cl-) |
| B、0.1mol/L NaHCO3溶液:c(OH-)+c(CO32-)=c(H+)+c(H2CO3) |
| C、0.3mol/L和0.1mol/L的两醋酸溶液中H+离子浓度之比为3:1 |
| D、25℃时,pH=4.75,浓度均为0.1mol?L-1的CH3COOH、CH3COONa混合溶液:c(CH3COO-)+c(OH-)<c(CH3COOH)+c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、平衡正移 |
| B、(a+b)<(c+d) |
| C、Z的体积分数变大 |
| D、X的转化率变大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com