

·ÖĪö £Ø1£©H3PO3±»Ńõ»ÆĪŖH3PO4£¬Ag+±»»¹ŌĪŖAg£¬½įŗĻŌ×ÓŹŲŗćŗĶµēŗÉŹŲŗ抓³ö£»
£Ø2£©ŃĒĮ×ĖįµŚŅ»²½µēĄė²śÉśµÄĒāĄė×ÓŅÖÖĘĮĖŃĒĮ×ĖįµÄµŚ¶ž²½µēĄė£»
£Ø3£©ŌŚĻ”ČÜŅŗÖŠ¢ŁH3PO3£Øaq£©?H2PO3-£Øaq£©+H+£Øaq£©”÷H=akJ/mol
¢ŚH2PO3-£Øaq£©?HPO32-£Øaq£©+H+£Øaq£©”÷H=bkJ/mol
¢ŪH+£Øaq£©+OH-£Øaq£©=H2O£Øl£©”÷H=ckJ/mol
øĒĖ¹¶ØĀɼĘĖć¢Ł+¢Ś-2¢ŪµĆµ½£»
£Ø4£©NaH2PO3Ė®½ā·“Ó¦ĪŖ£ŗH2PO3-+H2O?H3PO3+OH-£¬Kh=$\frac{c£Ø{H}_{3}P{O}_{3}£©c£ØO{H}^{-}£©}{c£Ø{H}_{2}P{{O}_{3}}^{-}£©}$=$\frac{c£Ø{H}_{3}P{O}_{3}£©c£ØO{H}^{-}£©}{c£Ø{H}_{2}P{{O}_{3}}^{-}£©}$”Į$\frac{c£Ø{H}^{+}£©}{c£Ø{H}^{+}£©}$=$\frac{Kw}{K{a}_{1}}$£¬Ę½ŗā³£ŹżÖ»ĖęĪĀ¶Č±ä»Æ£»
£Ø5£©aĪŖµēŌ“Õż¼«£¬bĪŖµēŌ“øŗ¼«£¬AĪŖŃō¼«ŹŅ£¬BĪŖŅõ¼«ŹŅ£®²śĘ·ŹŅÖŠ·¢Éś2H++HPO32-=H3PO3·“Ó¦µĆµ½ŃĒĮ×Ėį£¬½įŗĻµē×ÓŹŲŗć¼ĘĖćÉś³ÉĒāŃõ»ÆÄʵÄÖŹĮ森
½ā“š ½ā£ŗ£Ø1£©H3PO3±»Ńõ»ÆĪŖH3PO4£¬Ag+±»»¹ŌĪŖAg£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗH3PO3+2Ag++H2O=H3PO4+2Ag+2H+£¬
¹Ź“š°øĪŖ£ŗH3PO3+2Ag++H2O=H3PO4+2Ag+2H+£»
£Ø2£©µēĄėĘ½ŗāŅĘ¶ÆµÄ½Ē¶Č½āŹĶ£¬ŃĒĮ×ĖįµŚŅ»²½µēĄė²śÉśµÄĒāĄė×ÓŅÖÖĘĮĖŃĒĮ×ĖįµÄµŚ¶ž²½µēĄė£¬ĖłŅŌµŚŅ»²½µēĄėµÄKa1Ō¶“óÓŚµŚ¶ž²½µēĄėµÄKa2£¬
¹Ź“š°øĪŖ£ŗŃĒĮ×ĖįµŚŅ»²½µēĄė²śÉśµÄĒāĄė×ÓŅÖÖĘĮĖŃĒĮ×ĖįµÄµŚ¶ž²½µēĄė£¬ĖłŅŌµŚŅ»²½µēĄėµÄKa1Ō¶“óÓŚµŚ¶ž²½µēĄėµÄKa2£»
£Ø3£©ŌŚĻ”ČÜŅŗÖŠ¢ŁH3PO3£Øaq£©?H2PO3-£Øaq£©+H+£Øaq£©”÷H=akJ/mol
¢ŚH2PO3-£Øaq£©?HPO32-£Øaq£©+H+£Øaq£©”÷H=bkJ/mol
¢ŪH+£Øaq£©+OH-£Øaq£©=H2O£Øl£©”÷H=ckJ/mol
øĒĖ¹¶ØĀɼĘĖć¢Ł+¢Ś-2¢ŪµĆµ½£ŗH3PO3£Øaq£©+2NaOH£Øaq£©?Na2HPO3£Øaq£©+2H2O£Øl£©”÷H=£Øa+b+2c£©KJ/mol£¬
¹Ź“š°øĪŖ£ŗa+b+2c£»
£Ø4£©NaH2PO3Ė®½ā·“Ó¦ĪŖ£ŗH2PO3-+H2O?H3PO3+OH-£¬Kh=$\frac{c£Ø{H}_{3}P{O}_{3}£©c£ØO{H}^{-}£©}{c£Ø{H}_{2}P{{O}_{3}}^{-}£©}$=$\frac{c£Ø{H}_{3}P{O}_{3}£©c£ØO{H}^{-}£©}{c£Ø{H}_{2}P{{O}_{3}}^{-}£©}$”Į$\frac{c£Ø{H}^{+}£©}{c£Ø{H}^{+}£©}$=$\frac{Kw}{K{a}_{1}}$£¬Ka1”ĮKh=Kw£¬ĖłŅŌKh=$\frac{1{0}^{-14}}{5”Į1{0}^{-2}}$=2”Į10-13£¬¼ÓČėÉŁĮæI2£¬ŃĒĮ×ĖįĒāÄĘÓėµā·“Ó¦£¬ČÜŅŗµÄ¼īŠŌ±äČõ£¬$\frac{c£Ø{H}_{3}P{O}_{3}£©c£ØO{H}^{-}£©}{c£Ø{H}_{2}P{{O}_{3}}^{-}£©}$±£³Ö²»±ä£¬ĖłŅŌ$\frac{c£Ø{H}_{3}P{O}_{3}£©}{c£Ø{H}_{2}P{{O}_{3}}^{-}£©}$½«Ōö“ó£¬
¹Ź“š°øĪŖ£ŗ2”Į10-13£»Ōö“ó£»
£Ø5£©¢ŁaĪŖµēŌ“Õż¼«£¬bĪŖµēŌ“øŗ¼«£¬AĪŖŃō¼«ŹŅ£¬BĪŖŅõ¼«ŹŅ£®²śĘ·ŹŅÖŠ·¢Éś2H++HPO32-=H3PO3·“Ó¦µĆµ½ŃĒĮ×Ėį£¬
¹Ź“š°øĪŖ£ŗÕż£»2H++HPO32-=H3PO3£»
¢ŚµĆµ½0.1molŃĒĮ×Ėį×ŖŅĘ0.2molµē×Ó£¬Éś³É0.2molNaOH£¬ÖŹĮæ=0.2mol”Į40g/mol=8g£¬
¹Ź“š°øĪŖ£ŗ8£®
µćĘĄ ±¾Ģāæ¼²éĮĖČõµē½āÖŹµēĄėĘ½ŗāÓ°ĻģŅņĖŲ”¢ČČ»Æѧ·½³ĢŹ½ŹéŠ“ŗĶøĒĖ¹¶ØĀɼĘĖć”¢ŃĪĄąĖ®½āŗĶĖ®½āĘ½ŗā³£Źż¼ĘĖć”¢Ōµē³ŲŃĪĄąŗĶµē½ā³ŲŌĄķÓ¦ÓĆ£¬ÕĘĪÕ»ł“”ŹĒ½āĢā¹Ų¼ü£¬ĢāÄæÄѶČÖŠµČ£®


 ĆūŹ¦Öøµ¼ĘŚÄ©³å“Ģ¾ķĻµĮŠ“š°ø
ĆūŹ¦Öøµ¼ĘŚÄ©³å“Ģ¾ķĻµĮŠ“š°ø æŖŠÄĶÜæŚĖćĢāæØĻµĮŠ“š°ø
æŖŠÄĶÜæŚĖćĢāæØĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĻąĶ¬ĪĀ¶ČĻĀ£¬½«×ćĮæĀČ»ÆŅų¹ĢĢå·Ö±š·ÅČėĻąĶ¬Ģå»żµÄ¢ŁÕōĮóĖ®”¢¢Ś0.1 mol•L-1ŃĪĖį”¢¢Ū0.1 mol•L-1ĀČ»ÆĆ¾ČÜŅŗ”¢¢Ü0.1 mol•L-1ĻõĖįŅųČÜŅŗÖŠ£¬Ag+ÅØ¶Č£ŗ¢Ł£¾¢Ü=¢Ś£¾¢Ū | |
| B£® | ½«NH4HCO3”¢AlCl3”¢FeCl2”¢KAl£ØSO4£©2µÄČÜŅŗ·Ö±š¼ÓČČÕōøÉ”¢×ĘÉÕ£¬¾ł²»ÄܵƵ½ŌĪļÖŹ | |
| C£® | æÉÖ±½Óøł¾ŻKspµÄŹżÖµ“óŠ”±Č½ĻÄŃČÜĪļŌŚĖ®ÖŠµÄČܽā¶Č“óŠ” | |
| D£® | 25”ꏱ£¬Ksp£ØAgCl£©£¾Ksp£ØAgI£©£¬ĻņAgClµÄŠü×ĒŅŗÖŠ¼ÓČėKI¹ĢĢ壬ӊ»ĘÉ«³ĮµķÉś³É |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
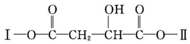 £ØĘäÖŠ¢ń”¢¢ņĪŖĪ“ÖŖ²æ·ÖµÄ½į¹¹£©£®
£ØĘäÖŠ¢ń”¢¢ņĪŖĪ“ÖŖ²æ·ÖµÄ½į¹¹£©£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā

| ŠņŗÅ | ²½Öč | ĻÖĻó |
| I | ĻņĶ¼2×°ÖĆÄŚ³äSO2ĘųĢå | GÖŠ£ŗÓŠĘųÅŻĆ°³ö£¬²śÉś°×É«³Įµķ£»HÖŠ£ŗÓŠĘųÅŻĆ°³ö£¬²śÉś°×É«³Įµķ£»ŅŗĆęÉĻ·½ĻČĀŌĻŌŗģ×ŲÉ«£¬ŗóÖš½„ĻūŹ§ |
| ¢ņ | “ÓG”¢HÖŠ¹żĀĖ³ö°×É«³Įµķ£¬·Ö±š¼ÓČėĻ”ŃĪĖįÖŠ | G”¢HÖŠµÄ°×É«³Įµķ¾ł²»Čܽā |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ×å ÖÜĘŚ | ¢ńA | ¢ņA | ¢óA | ¢ōA | ¢õA | ¢öA | ¢õ¢ņA | 0 |
| 1 | ¢Ł | |||||||
| 2 | ¢Ś | ¢Ū | ¢Ü | |||||
| 3 | ¢Ż | ¢Ž | ¢ß | ¢ą | ¢į | ¢ā | ||
 £¬øĆ»ÆŗĻĪļĖįŠŌĢõ¼žĻĀÓėøßĆĢĖį¼Ų·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2”ü
£¬øĆ»ÆŗĻĪļĖįŠŌĢõ¼žĻĀÓėøßĆĢĖį¼Ų·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2”ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 6ÖÖ | B£® | 8ÖÖ | C£® | 10ÖÖ | D£® | 14ÖÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģ½Ī÷Ź”øßČżÉĻѧʌµŚČż“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Ļņŗ¬ÓŠc(FeCl3)£½0.3 mol”¤L£1”¢c(FeCl2)£½0.15 mol”¤L£1µÄ»ģŗĻČÜŅŗÖŠµĪ¼ÓĻ”NaOHČÜŅŗ£¬æɵƵ½Ņ»ÖÖŗŚÉ«·ÖÉ¢Ļµ£¬ĘäÖŠ·ÖÉ¢ÖŹĮ£×ÓŹĒ Ö±¾¶Ō¼ĪŖ9.3 nmµÄ½šŹōŃõ»ÆĪļ£¬ĻĀĮŠÓŠ¹ŲĖµ·ØÖŠÕżČ·µÄŹĒ( )
Ö±¾¶Ō¼ĪŖ9.3 nmµÄ½šŹōŃõ»ÆĪļ£¬ĻĀĮŠÓŠ¹ŲĖµ·ØÖŠÕżČ·µÄŹĒ( )
A£®øĆ·ÖÉ¢ĻµµÄ·ÖÉ¢ÖŹĪŖFe2O3
B£®ŌŚµē³”×÷ÓĆĻĀ£¬Ņõ¼«ø½½ü·ÖÉ¢ĻµŗŚÉ«±äÉī£¬ŌņĖµĆ÷øĆ·ÖÉ¢Ļµ“ųÕżµēŗÉ
C£®æÉÓĆ¹żĀĖµÄ·½·Ø½«ŗŚÉ«½šŹōŃõ»ÆĪļÓėNa£«·ÖĄėæŖ
D£®¼ÓČėNaOHŹ±·¢ÉśµÄ·“Ó¦æÉÄÜĪŖ£ŗFe2£«£«2Fe3£«£«8OH£===Fe3O4£«4H2O
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com