
| A. | 任何化学反应,只要是放热反应,理论上都能设计成原电池 | |
| B. | 周期表中所有元素都是从自然界中发现的 | |
| C. | 需要加热才能发生的反应一定是吸热反应 | |
| D. | 原子结合成分子过程中一定释放出能量 |
分析 A.自发进行的氧化还原反应可以设计为原电池的化学反应;
B.周期表中的元素大多是自然界存在的,但有些属于人造元素,如106号元素;
C.需要加热才能进行的化学反应不一定是吸热反应;
D.化学键的形成要放出能量.
解答 解:A.能设计成原电池的反应必须是自发进行的、放热的氧化还原反应,故A错误;
B.周期表中的元素大多是自然界存在的,但有些属于人造元素,都是放射性元素,包括Tc、Pm、At、Np、Pu、Am、Cm、Bk、Cf、Es、Fm、Md、No、Lr、Rf、Db、Es、Bh、Hs、Mt和110、111、112号元素,故B错误;
C.需要加热才能进行的化学反应不一定是吸热反应,如铝热反应,需要加热,但属于放热反应,故C错误;
D.化学键的形成要放出能量,所以原子组成分子一定释放出能量,故D正确;
故选D.
点评 本题考查了化学反应能量变化的分析判断以及原电池的设计等,变化过程实质分析是解题关键,题目较简单.


科目:高中化学 来源: 题型:填空题
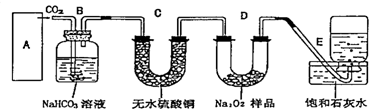
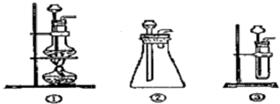
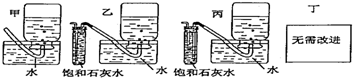
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 +CaCl2+H2O
+CaCl2+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放电时,Fe作负极,发生氧化反应 | |
| B. | 放电时,NiO2作正极,发生还原反应 | |
| C. | 蓄电池的电极应浸入碱性电解质溶液中 | |
| D. | 充电时,充电机的正极接在该蓄电池的负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | IA族金属元素是同周期中金属性最强的元素 | |
| B. | 非金属元素组成的化合物中只含共价键 | |
| C. | 同种元素的原子均有相同的质子数和中子数 | |
| D. | VIIA族元素的阴离子还原性越强,其最高价氧化物对应水化物的酸性越强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | X的分子式为C12H16O3 | |
| B. | 可用酸性高锰酸钾溶液区分苯和X | |
| C. | X在一定条件下能发生水解、酯化、加成等反应 | |
| D. | 在Ni作催化剂的条件下,1 mol X最多只能与1 mol H2加成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com