
【题目】下列关于金属及其化合物的说法正确的是 ( )
A. Na2O为淡黄色固体,MgO为白色固体
B. 金属钠具有强还原性,可用与TiCl4溶液反应制取金属Ti
C. 铁放入浓硝酸中无明显现象,说明铁与浓硝酸不反应
D. 工业上常用电解熔融氯化镁的方法制取金属镁
科目:高中化学 来源: 题型:
【题目】如图是一个制取氯气并以氯气为原料进行特定反应的装置,请回答下列问题. 
(1)A是氯气发生装置,其中发生反应的离子方程式为 .
(2)实验开始时,先点燃装置A处的酒精灯,打开弹簧夹K,让Cl2充满整个装置,再点装置D处的酒精灯,Cl2通过C瓶后再进入D(D装置的硬质玻璃管内盛有碳粉)发生氧化还原反应,其产物为CO2和HCl.D中发生反应的化学方程式为 , 装置C的作用是 .
(3)实验过程中,E处产生的现象为 .
(4)D处反应完毕后,关闭弹簧夹K,移去酒精灯,由于余热的作用,A处仍有Cl2产生,此时B中出现的现象是 , 装置B的作用是 .
(5)若实验中使12molL﹣1的浓盐酸10mL与足量的MnO2反应,则生成的Cl2的物质的量总是小于0.03mol,其原因是 .
(6)若要吸收从硬质玻璃管中导出的气体,E中应盛放溶液,其中有毒气体与之反应的离子方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用氢氧燃料电池进行下图实验(图中所用电极均为惰性电极):

(1)电极a为______极(填“正”或“负”),溶液中OH-移向______极(填“a”或“b”);
(2)电极b处所发生的电极反应方程式为___________________;
(3)随着反应的进行,氢氧燃料电池内部的pH将______(填“增大”或“减小”);
(4)c极为________(填“阴”或“阳”)极,电极反应式为_____________________;
(5)右边装置中盛有足量的 AgNO3溶液,当氢氧燃料电池中消耗氢气1.12L(标准状况下)时,则此时右边装置中________电极质量增加_________g。
(6)若把上图中的氢气换成甲醇,该燃料电池负极电极反应式为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】经一定时间后,可逆反应aA+bBcC中物质的含量A%和C%随温度的变化曲线如图所示.下列说法正确的是( ) 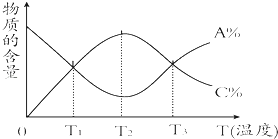
A.该反应在T1、T3温度时达到化学平衡
B.该反应在T2温度时达到化学平衡
C.该反应的逆反应是放热反应
D.升高温度,平衡会向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于化学反应方向的确定,下列说法正确的是( )
A. 在温度、压强一定的条件下,焓因素和熵因素共同决定一个化学反应的方向
B. 温度、压强一定时,放热的、熵增加反应不一定能自发进行
C. 反应焓变是决定反应能否自发进行的唯一因素
D. 固体的溶解过程与焓变有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组用碱式碳酸铜[CuCO3·Cu(OH)2]制取铜粉并测定铜粉纯度的实验如下:
步骤1:将一定量的碱式碳酸铜置于烧杯中,向烧杯中加入N2H4的水溶液,边搅拌边加热,有大量的气体生成和红色铜析出,将沉淀过滤、低温干燥得红色粉末。
步骤2:称取1.9600 g红色粉末于烧杯中,缓慢加入足量稀硫酸,边加热边通入氧气使粉末完全溶解。冷却,将溶液移入100 mL 容量瓶中,用水稀释至刻度。
书骤3:准确量取20.00mL的溶液,调节溶液呈弱酸性,向其中加入过量的KI.,充分反应后,以淀粉溶液作指示剂,用0.2000mol/LNa2S2O3标准溶液滴定,滴定终点时共消耗Na2S2O3标准溶液30.00 mL.过程中所发生的反应如下:Cu2++I-![]() CuI↓+I3-(未配平),I3-+S2O32-=S4O62-+I-(未配平)。
CuI↓+I3-(未配平),I3-+S2O32-=S4O62-+I-(未配平)。
(1)步骤1中所发生反应的化学方程式为_________________。
(2)步骤2 中所发生反应的离子方程式为_________________。
(3)步骤3 中加入过量KI的作用是_________________。
(4)若铜粉中杂质不参与步骤3 的反应,通过计算确定红色粉末中含铜质量分数(写出计算过程)________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)火箭推进器中装有还原剂肼(N2H4)和强氧化剂过氧化氢(H2O2),当它们混合时,即产生大量氮气和水蒸气,并放出大量热。已知0.4 mol液态肼与足量过氧化氢反应,生成氮气和水蒸气,放出256.65 kJ的热量。
①写出反应的热化学方程式: ________________________________,其中氧化剂是____________,若反应中当有1molN2生成时转移的电子物质的量是__________。
②此反应用于火箭推进,除释放大量热和产生气体外,还有一个很大的优点是___________。
(2)已知:2CO(g) + O2(g) = 2CO2(g) △H= -566 kJ/mol
Na2O2(s) + CO2(g) = Na2CO3(s) + ![]() O2(g) △H= -226 kJ/mol
O2(g) △H= -226 kJ/mol
请写出常温下,过氧化钠与一氧化碳反应生成碳酸钠的热化学方程式:____________________。
(3)中学化学实验中的中和热的测定所需的玻璃仪器除了大烧杯、小烧杯、量筒外还有:_____,在大小烧杯之间填满碎泡沫(或纸条)其作用是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯碱工业中关于电极材料的选用,下列说法合理的是( )
A.两极可用任意可导电固体材料
B.阳极必须用惰性电极
C.阴极必须用惰性电极
D.石墨阳极比金属阳极更节电
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com