
【题目】现有A、B,C、D四种常见烃,A、B、C在常温常压下是无色气体且都是链烃,D为无色液体。①A完全燃烧后的气态产物(CO2和H2O)的体积比为2:1, ②标准状况下lOOmLB恰好能使含1.43g Br2的溴水褪色,生成物经测定每个碳原子都结合有溴原子;③C不能使酸性高锰酸钾溶液褪色,但在光照最多能和6倍体积的氯气发生反应;④D不能使溴水褪色但能使酸性高锰酸钾溶液褪色;在140℃和1.01×105Pa压强下,250mL D蒸气的质量为O.782g,在铁为催化剂时D和溴发生反应生成的一溴代物只有一种,试确定A、B、C、D各是什么物质?
【答案】A:C2H2 乙炔; B:CH2=CH-CH=CH2 1,3丁二烯;C:C2H6 乙烷 D: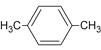 1,4-二甲基苯
1,4-二甲基苯
【解析】
A完全燃烧后的气态产物(CO2和H2O)的体积比为2:1,说明A分子中C、H原子个数比为1:1,则A为乙炔;标况下100mLB的物质的量为:0.1L÷22.4L/mol=![]() mol,1.43gBr2的物质的量为:1.43g÷160g/mol=
mol,1.43gBr2的物质的量为:1.43g÷160g/mol=![]() mol,n(B):n(Br)=
mol,n(B):n(Br)=![]() mol:
mol:![]() mol=1:2,则B分子中含有两个双键或一个碳碳叁键,因B与溴加成反应后的生成物每个碳原子都结合有溴原子,则B分子中含有两个双键,结构简式为:CH2=CH-CH=CH2;C不能使酸性高锰酸钾溶液褪色,说明C为饱和烃;在光照最多能和6倍体积的氯气发生反应,说明分子中含有6个氢原子,故C为乙烷;由理想气体的状态方程可得D的相对分子质量M=
mol=1:2,则B分子中含有两个双键或一个碳碳叁键,因B与溴加成反应后的生成物每个碳原子都结合有溴原子,则B分子中含有两个双键,结构简式为:CH2=CH-CH=CH2;C不能使酸性高锰酸钾溶液褪色,说明C为饱和烃;在光照最多能和6倍体积的氯气发生反应,说明分子中含有6个氢原子,故C为乙烷;由理想气体的状态方程可得D的相对分子质量M=![]() =
=![]() =106,D不能使溴水褪色但能使酸性高锰酸钾溶液褪色,说有D为苯的同系物,在铁为催化剂时D和溴发生反应生成的一溴代物只有一种,说明D中两个甲基位于苯环的对位,结构简式为:
=106,D不能使溴水褪色但能使酸性高锰酸钾溶液褪色,说有D为苯的同系物,在铁为催化剂时D和溴发生反应生成的一溴代物只有一种,说明D中两个甲基位于苯环的对位,结构简式为: ;故答案为:A:C2H2 乙炔; B:CH2=CH-CH=CH2 1,3丁二烯;C:C2H6 乙烷 D:
;故答案为:A:C2H2 乙炔; B:CH2=CH-CH=CH2 1,3丁二烯;C:C2H6 乙烷 D: 1,4-二甲基苯。
1,4-二甲基苯。


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
【题目】已知自然界氧的同位素有16O , 17O ,18O,若氢的同位素有H、D、T,从水分子的原子组成来看,自然界的水一共有几种
A.18种B.6种C.9种D.12种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究金属桥墩腐蚀及防护是跨海建桥的重要课题。下列有关判断中正确的是


A. 用装置①模拟研究时未见a上有气泡,说明铁没有被腐蚀
B. ②中桥墩与外加电源正极连接能确保桥墩不被腐蚀
C. ③中采用了牺牲阳极的阴极保护法保护桥墩
D. ①②③中海水均是实现化学能与电能相互转化的电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物m、n、P存在如下转化关系。下列说法正确的是

A. m、n不存在同分异构体,p存在多种同分异构体
B. m、n、p均能使酸性高锰酸钾溶液褪色
C. m、n、p中所有原子可能共面
D. 等质量的m、n、p,完全燃烧耗氧量不相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】空气污染物NO通常用含Ce4+的溶液吸收,生成HNO2、NO3-,再利用电解法将上述吸收液中的HNO2转化为无毒物质,同时生成Ce4+,其原理如图所示。下列说法正确的是

A. H+由右室进入左室
B. Ce4+从电解槽的c口流出,且可循环使用
C. 阴极的电极反应式:2HNO2+6H++6e-===N2↑+4H2O
D. 若用甲烷燃料电池作为电源,当消耗标准状况下33.6 L甲烷时,理论上可转化2mol HNO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知烃被酸性KMn04溶液氧化时,碳碳双键或叁键将断裂生成-![]() -或—COOH。某烃的分子式为某烃的分子式为C11H20, lmol该烃在催化剂作用下可以吸收2mol H2;用热的酸性KMn04溶液氧化,得到下列三种有机物:CH3-CO-CH2-CH3 , CH3-CO-CH3,HOOC-CH2CH2—COOH由此推断写出该烃可能的结构简式是_________________ 。
-或—COOH。某烃的分子式为某烃的分子式为C11H20, lmol该烃在催化剂作用下可以吸收2mol H2;用热的酸性KMn04溶液氧化,得到下列三种有机物:CH3-CO-CH2-CH3 , CH3-CO-CH3,HOOC-CH2CH2—COOH由此推断写出该烃可能的结构简式是_________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气是一种清洁、高效新能源,也是重要的化工原料。
(1)工业上利用甲烷制备氢气的反应为:CH4(g)+H2O(g)![]() CO(g)+3H2(g)
CO(g)+3H2(g)
已知:
①H2(g)+1/2O2(g)![]() H2O(g) △H1=-198kJ/mol
H2O(g) △H1=-198kJ/mol
②CO(g)+1/2O2(g)![]() CO2(g) △H2=-283kJ/mol
CO2(g) △H2=-283kJ/mol
③CH4(g)+2O2(g)![]() CO2(g)+2H2O(g) △H3=-846.3kJ/mol
CO2(g)+2H2O(g) △H3=-846.3kJ/mol
则CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H4=________。
CO(g)+3H2(g) △H4=________。
(2)工业上利用CO和H2合成清洁能源CH3OH,其反应为:CO(g)+2H2(g)![]() CH3OH(g) △H=-116kJ/mo1
CH3OH(g) △H=-116kJ/mo1
①如图表示CO的平衡转化率(α)随温度和压强变化的示意图。X表示的是_______,理由_________;Y1_____Y2(填“<”“=”或“>”)。

②在2L恒容密闭容器中充入2 mol CO和4 mol H2,在一定条件下经过10 min达到平衡状态c点处。则在该条件下,从开始至达到平衡状态v(CH3OH)=_______________,平衡常数Ka、Kb、Kc 的大小关系:___________。
③下列措施既能增大反应速率又能提高反应物的转化率的是_______。
A.使用催化剂 B.及时分离CH3OH C.升高温度 D.增大压强
(3)已知燃料电池的比能量与单位质量燃料物质失去的电子数成正比。理论上H2、CH4、CH3OH的碱性电池的比能量由大到小的顺序为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除去杂质的方法,正确的是
A.除去乙烷中少量的乙烯:光照条件下通入Cl2,气液分离
B.除去乙醇中少量乙酸:加入碳酸钠溶液,分液
C.除去FeCl3溶液中少量的CuCl2:加入过量铁粉,过滤
D.除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤,分液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com