

���� ��ʵ��Ŀ���Dzⶨ����������������ȡ�ķ�����ʹ��Ʒ�ܽ⡢��Ӧ������������������Ȼ��ͨ������������������������������
��1����ͼ��֪������I�ǽ��������ᷴӦ����Һϡ�ͳ�250.00mL��Һ������Ҫ100mL������ƿ��������Ҫ��ͷ�ιܣ�
��2��������Һ���ƹ��̺�ʵ�鲽������ж�ѡ���У���������Ũ�ȵ�Ӱ������ж�
��3������ˮ������+2������Ϊ+3�ۣ�
��4�����ȷֽ����õ�������Fe2O3��������Ϊ3g��������ȥ25mL��Һ����250mL��Һ���Եõ�Fe2O3����Ϊ30g�����ݻ�ѧʽ������Ԫ�ص����������������������Ķ������ԭ��������Ʒ����Ԫ�ص�����������
��� �⣺��1����ͼ��֪������I�ǽ��������ᷴӦ����Һϡ�ͳ�250.00mL��Һ�����õ��IJ����������ձ����������⣬��Ҫ250mL����ƿ������Ҫ�ý�ͷ�ιܶ��ݣ�
�ʴ�Ϊ��250mL����ƿ����ͷ�ιܣ�
��2��������Һ���ƹ��̺�ʵ�鲽������ж�ѡ���������ʹ������ҺŨ��ƫС��
��δϴ���ձ��Ͳ�����������δȫ��ת�Ƶ�����ƿ��Ũ��ƫ�ͣ��ʢ���ȷ��
�ڶ���ʱ��������ƿ�Ŀ̶��ߣ�����ƿ��ˮδ�ӵ��̶��ߣ�Ũ��ƫ�ʢڴ���
������Һǰ����ƿ������������ˮ��������ҺŨ����Ӱ�죬�ʢ۴���
��ҡ�Ⱥ���Һ����ڿ̶��ߺ������ˮ����Һ����̶������У���ҺŨ��ϡ��ƫС���ʢ���ȷ��
�ʴ�Ϊ���٢ܣ�
��3������ˮ������+2������Ϊ+3�ۣ�������Ӧ�����ӷ���ʽΪ��2Fe2++Cl2=2Fe3++2Cl-��
�ʴ�Ϊ��2Fe2++Cl2=2Fe3++2Cl-��
��4�����ȷֽ����õ�������Fe2O3��������Ϊ3g��������ȥ25mL��Һ����250mL��Һ���Եõ�Fe2O3����Ϊ30g��������Ԫ���غ������Ԫ�ص���������=$\frac{\frac{30g}{160g/mol}��2��56}{50g}$100%=42%��
�ʴ�Ϊ��42%��
���� ���⿼��̽����������뺬������Ŀ�Ѷ��еȣ��漰��Һ���ơ����Ӽ��顢��ʵ�������������ʵ�鷽�������ۡ���ѧ�����֪ʶ����ȷ�ⶨԭ���ǽ���Ĺؼ����Ƕ���ѧ֪ʶ���ۺ����ã���Ҫѧ��������ʵ�Ļ���������֪ʶ������������������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
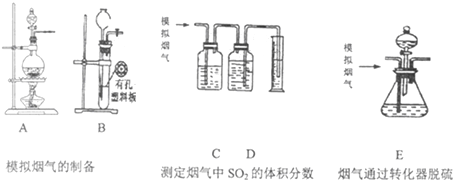
 �����ѣ�CH3OCH3������Ϊ21���������ȼ�ϣ���δ������������͡�Һ������ú���Ȳ����������Ļ������ܣ���ҵ�Ʊ��������ڴ���Ӧ���У�ѹ��2.0��10.0Mpa���¶�230��280�棩�������з�Ӧ��
�����ѣ�CH3OCH3������Ϊ21���������ȼ�ϣ���δ������������͡�Һ������ú���Ȳ����������Ļ������ܣ���ҵ�Ʊ��������ڴ���Ӧ���У�ѹ��2.0��10.0Mpa���¶�230��280�棩�������з�Ӧ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Ũ�Ȳ��䣬ʹ��������1�� | B�� | ����Ũ������1��������������1/2 | ||
| C�� | ��̼��ƹ����Ϊ̼��Ʒ�ĩ | D�� | ���ȴ˷�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
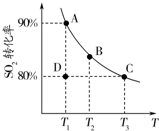 �о����仯������������Ҫ���壮
�о����仯������������Ҫ���壮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڻ�����м�������Ũ���ᣬ���ȡ����� | |
| B�� | �ڻ�����м�������NaOH��Һ������ | |
| C�� | �ô�ʯ���������� | |
| D�� | �ڻ�����м�������Ũ���ᣬ���ȡ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2KClO3$\frac{\underline{MnO_2}}{��}$2KCl+3O2�� | B�� | Fe+CuSO4�TFeSO4+Cu | ||
| C�� | 2H2O��$\frac{\underline{\;ͨ��\;}}{\;}$��2H2��+O2�� | D�� | Cl2+2NaOH�TNaCl+NaClO+H2O |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com