
����Ŀ��ijʵ����Ҫ���ʵ���Ũ��Ϊ0.5mol/L��NaOH��Һ960mL��������к�ʵ�飬����NaOH��Һ�IJ������£��ش��������⣺
��һ������ȡNaOH���壬������������ˮ�ܽ⣻
�ڶ���������ȴ��ת��������ƿ�У�
��������������ˮϴ���ձ��Ͳ�����2��3�Σ���ϴ��ҺҲע������ƿ�У�
���IJ�������
���岽��ҡ�ȡ�
��1����һ���г���NaOH���������Ϊ____g��
��2�����IJ������ݡ��ľ������Ϊ____��
��3�����������Һ�����г������������������Ƶ���Һ���ʵ���Ũ���к�Ӱ�죿���ƫ����ƫС������Ӱ�족��
������ƿ��ԭ����������ˮ___��
�ڶ���ʱ���ӹ۲�____��
�۰��ռ����ֽ�ϳ���____��
���ܽ����õ��ձ�δϴ��____��
��4��ȡ������Һ10mL���Թ��У�����5mLijŨ�ȵ�������Һǡ���кͣ������ӵ�������Һ�����ʵ���Ũ����____mol/L��
���𰸡�20.0 �ò�����������������ƿ�м�������ˮ���̶�����1-2cm����ƽ�ӿ̶��ߣ����ý�ͷ�ι���μ�����ˮ����Һ����̶������� ��Ӱ�� ƫ�� ƫС ƫС 1
��������
��1��ʵ����û��960mL����ƿ��Ӧ��1000mL������ƿ�������Ҫ������NaOH������Ϊ1000��10��3L��0.5mol��L��1��40g��mol��1=20.0g��
��Ϊ20.0��
��2������ʱ�����ò�����������������ƿ�м�������ˮ��������̶�����1��2cmʱ�����ý�ͷ�ιܵμ�����ˮ����Һ����̶������У�
��Ϊ���ò�����������������ƿ�м�������ˮ���̶�����1-2cm����ƽ�ӿ̶��ߣ����ý�ͷ�ι���μ�����ˮ����Һ����̶������У�
��3������c=![]() ���������
���������
������ƿ����������ˮ����ʵ������Ӱ�죻
��Ϊ��Ӱ�죻
�ڶ���ʱ���ӣ�����ƿ����Һ�����С��Ũ��ƫ��
��Ϊƫ��
���ռ��ܳ��⣬��NaOH����ֽ�ϳ�����ֽ�ϲ���NaOH����������Һ���ʵ����ʵ������ٻ��������٣���������Һ��Ũ��ƫС��
��ΪƫС��
���ܽ�ʱ�����ձ�Ϊϴ�ӣ�������ʵ����������ʵ������٣�������Һ��Ũ��ƫС��
��ΪƫС��
��4��ȡ������Һ10mL����NaOH��Ũ����Ϊ0.5mol��L��1��NaOH������ǡ���кͣ���n(NaOH)=n(HCl)��10��10��3L��0.5mol��L��1=5��10��3L��c(HCl)�����c(HCl)=1mol��L��1��
��Ϊ1��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�����������������ȷ���ǣ� ��
A. ��״���£�1molFe�ֱ��������������ˮ������Ӧת�Ƶĵ�������Ϊ2NA
B. 11.2LH2�к��е�ԭ����ΪNA
C. Na2O��Na2O2�Ļ���ﹲ1mol����������ĿΪNA
D. 1.0L1mol/L��Na2SO4ˮ��Һ�к��е���ԭ����ĿΪ4NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪2A(g)��B(g)![]() 2C(g)����H����akJ/mol(a��0)����һ���д����Ĺ̶��ݻ��������м���2molA��1molB����500��ʱ��ַ�Ӧ��ƽ���C��Ũ��Ϊ��mol/L���ų�����ΪbkJ��
2C(g)����H����akJ/mol(a��0)����һ���д����Ĺ̶��ݻ��������м���2molA��1molB����500��ʱ��ַ�Ӧ��ƽ���C��Ũ��Ϊ��mol/L���ų�����ΪbkJ��
(1)�Ƚ�a__b(����������������������)��
(2)������Ӧ�¶����ߵ�700�棬�÷�Ӧ��ƽ�ⳣ����___________(��������������С������������)��
(3)������˵���÷�Ӧ�Ѿ��ﵽƽ��״̬����__________��
a. v(C)=2 v(B)b. ����������ѹǿ���ֲ���
c. v��(A)=2v��(B) d.�����������ܶȱ��ֲ���
e.�����������ƽ����Է����������ֲ���
(4)Ϊʹ�÷�Ӧ�ķ�Ӧ����������ƽ��������Ӧ�����ƶ��IJ�����______________��
a. ��ʱ�����C����b. �ʵ������¶�
c. ����B��Ũ��d. ѡ���Ч����
(5) ��������������Ϊ��ѹ����(��Ӧǰ�����ͬ)����ʼʱ����2molA��1molB��500��ʱ��ַ�Ӧ��ƽ��ų�����ΪdkJ����d___b(����������������������)��������______________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ��ȥ�����е�Ca2+. Mg2+. SO42-�Լ���ɳ�����ʣ�ijͬѧ�����һ���Ʊ����ε�ʵ�鷽�����������£����ڳ������Լ��Թ�����
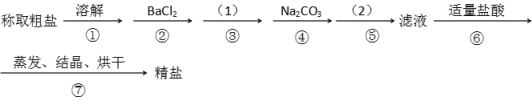
��1���ڢܲ��У�д����Ӧ�����ӷ���ʽ���������Һ��Ca2+����Ҫ������ʽΪCaCl2��_______________ ��____________��
��2��ʵ�鷽���ģ�1����Ӧʹ�ó����Լ��Ļ�ѧʽ__________�����������ӷ���ʽ��__________����ʵ�鷽���ģ�2���еIJ���������_______��
��3����ʵ����Ʒ����Ż��ĽǶȷ�������ںܿ͢ɷ�ߵ�____________����ǡ������������˵�����ɡ�___________________________________________��
��4���ж�BaCl2�ѹ����ķ�����_________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���ǣ� ��
A. SiO2��SiCl4����Է���������ͬ�����Էе㲻ͬ
B. NH4C1��NaOH������ѧ�����ͺ;������;���ͬ
C. ����Ag�Ķѻ���ʽ�������������ܶѻ�
D. CO2��ˮ��Ӧ�����У��й��ۼ��Ķ��Ѻ��γ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼�͵��Ļ����������������й㷺���ڡ��ش���������:
��1�����Ȼ�����NCl3����һ�ֻ�ɫ����״�����д̼�����ζ�Ļӷ����ж�Һ�壬��ԭ�Ӿ�����8e���ṹ��д�������ʽ_____________________���ȼҵ����ʱ������ʳ��ˮ��ͨ����������NH4Cl�����������������ɵ�������Ӧ�����������Ȼ������÷�Ӧ�Ļ�ѧ����ʽΪ______________��
��2����֪��2CO2(g) + 3NaOH(aq)=NaHCO3(aq)+Na2CO3(aq)+H2O(l) ��H=��4a kJ/mol
CO2(g) +2NaOH(aq)=Na2CO3(aq)+H2O(l) ��H=��b kJ/mol
��������CO2��NaOH��Һ��Ӧ����NaHCO3���Ȼ�ѧ��Ӧ����ʽΪ:____________��
��3������CO���Խ�NOת��Ϊ����N2���䷴ӦΪ��2NO(g)+2CO(g)![]() N2(g)+2CO2(g)�����ݻ���ΪIL�ļס��ҡ����������£���Ӧ�¶ȷֱ�Ϊ300�桢T�桢300�棩�����зֱ������ͬ��NO��CO����ø�������n(CO)�淴Ӧʱ��t�ı仯������±���ʾ:
N2(g)+2CO2(g)�����ݻ���ΪIL�ļס��ҡ����������£���Ӧ�¶ȷֱ�Ϊ300�桢T�桢300�棩�����зֱ������ͬ��NO��CO����ø�������n(CO)�淴Ӧʱ��t�ı仯������±���ʾ:
t/min | 0 | 40 | 80 | 120 | 160 |
n(CO)����������/mol | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
n(CO)����������/mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
n(CO)����������/mol | 1.00 | 0.80 | 0.65 | 0.53 | 0.45 |
�ټ������У�0��40min����NO��Ũ�ȱ仯��ʾ��ƽ����Ӧ����v(NO)=_______��
�ڸ÷�Ӧ�ġ�H______0���>����<������
�ۼס��������ﵽƽ��ʱ��CO��ת����Ϊ��(��)________��(��)���>��,��< ������������
��4�������£���(NH4)2C2O4��Һ�У���ӦNH4++C2O42��+H2O![]() NH3��H2O+HC2O4����ƽ�ⳣ��K=___������֪�����£�H2C2O4�ĵ���ƽ�ⳣ��Ka1��5��10-2��Ka2��5��10-5 H2O�ĵ���ƽ�ⳣ��Kw=1��10-14 NH3��H2O�ĵ���ƽ�ⳣ��Kb��2��10-5��
NH3��H2O+HC2O4����ƽ�ⳣ��K=___������֪�����£�H2C2O4�ĵ���ƽ�ⳣ��Ka1��5��10-2��Ka2��5��10-5 H2O�ĵ���ƽ�ⳣ��Kw=1��10-14 NH3��H2O�ĵ���ƽ�ⳣ��Kb��2��10-5��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��ͭ��Һ�к���һ������CuSO4�������ŷŻ���Ⱦ���������õ绯ѧԭ���ɶԷ�Һ���л��մ�����װ����ͼ���������ӽ���Ĥֻ����H+ͨ������֪����Cu2++ HCHO + 3OH��=Cu + HCOO��+ 2H2O������ԭ�ԣ�HCHO > M(���ֽ�����> Cu��
����˵����ȷ����
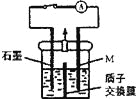
A. ��Ӧ֮ǰ��Ӧ����OH����HCHO��Һ���뵽װ�õ����
B. �Ҳ���ĵ缫��Ӧʽ��HCHO-2e��+H2O=HCOO��+3H+
C. �������ӽ���Ĥ���������ӽ���Ĥ���ŵ�����У�������OH���������Ǩ��
D. �ŵ�һ��ʱ�����أ���ȥ���ӽ���Ĥ��װ���п��ܻ��к�ɫ���塢��ɫ��״�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ü�������NO2��Ⱦ�����о���CH4+2NO2![]() N2+CO2+2H2O����1L�ܱ������У����Ʋ�ͬ�¶ȣ��ֱ����0.50molCH4��1.2molNO2�����n(CH4)��ʱ��仯���й�ʵ�����ݼ�����
N2+CO2+2H2O����1L�ܱ������У����Ʋ�ͬ�¶ȣ��ֱ����0.50molCH4��1.2molNO2�����n(CH4)��ʱ��仯���й�ʵ�����ݼ�����
��� | �¶� | ʱ��/min n/mol | 0 | 10 | 20 | 40 | 50 |
�� | T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
�� | T2 | n(CH4) | 0.50 | 0.30 | 0.18 | �� | 0.15 |
����˵����ȷ���ǣ� ��
A. �����У�0~20min�ڣ�NO2�Ľ�������Ϊ0.0125mol��L-1��min-1
B. ��ʵ�����ݿ�֪�÷�Ӧ�����˵��¶�ΪT1
C. 40minʱ��������T2Ӧ�������Ϊ0.18
D. 0��10min�ڣ�CH4�Ľ������ʢ�>��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NA���������ӵ�������ֵ�������й�������ȷ����
A. ��״���£�����22.4L��������ȫȼ��ʱת�Ƶ�����Ϊ3NA
B. 1 L 0.1 mol��L1��NaHCO3��Һ��![]() ��
��![]() ������֮��Ϊ0.1NA
������֮��Ϊ0.1NA
C. ��һ���¶���64gSO2������������ַ�Ӧ��ת�Ƶ�����Ϊ4NA
D. ����NA��Fe( OH)3�������������������У���Ԫ�ص���������56g
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com