
| 216×22.2% |
| 12 |
| 216-12×4-8 |
| 2 |
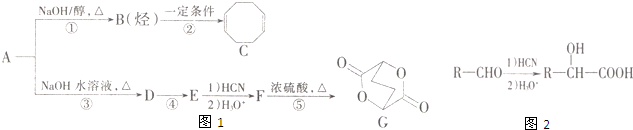
 ,根据已知信息,可知E为OHC-CH2-CH2-CHO,逆推可知D为HOCH2CH2CH2CH2OH,则A为BrCH2CH2CH2CH2Br,据此解答.
,根据已知信息,可知E为OHC-CH2-CH2-CHO,逆推可知D为HOCH2CH2CH2CH2OH,则A为BrCH2CH2CH2CH2Br,据此解答.| 216×22.2% |
| 12 |
| 216-12×4-8 |
| 2 |
 ,根据已知信息,可知E为OHC-CH2-CH2-CHO,逆推可知D为HOCH2CH2CH2CH2OH,则A为BrCH2CH2CH2CH2Br,
,根据已知信息,可知E为OHC-CH2-CH2-CHO,逆推可知D为HOCH2CH2CH2CH2OH,则A为BrCH2CH2CH2CH2Br, ,
,| 10 |
| 4 |
| 6 |
| 2 |
| 水 |
| △ |

| 浓硫酸 |
| △ |
 +2H2O,
+2H2O,| 水 |
| △ |

| 浓硫酸 |
| △ |
 +2H2O;
+2H2O; ,
,

 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| n(MnO2) |
| n(Fe) |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CaCl2=Ca2++2Cl- |
| B、Ba(OH)2=Ba2++2OH- |
| C、HNO3=H++NO3- |
| D、NaHCO3=Na++H++CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、Ba2+、Cl-、NO3- |
| B、K+、Na+、Br-、S2- |
| C、H+、Fe3+、I-、NO3- |
| D、Na+、Ba2+、OH-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D |
| 淀粉--混合物 | 液氯--非电解质 | 苯酚--有机物 | 水晶--分子晶体 |
| 胆矾--纯净物 | 碳酸钙--强电解质 | 纯碱--盐 | 食盐--离子晶体 |
| 盐酸--化合物 | 醋酸--弱电解质 | 水--氧化物 | 金刚石--原子晶体 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
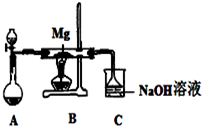 SiO2、SO2和CO2都是酸性氧化物,它们的化学性质有一定的相似性;Mg和Na的化学性质也有一定相似性.某兴趣小组用如图所示装置进行Mg与SO2反应的实验.
SiO2、SO2和CO2都是酸性氧化物,它们的化学性质有一定的相似性;Mg和Na的化学性质也有一定相似性.某兴趣小组用如图所示装置进行Mg与SO2反应的实验.
| ||
| ||
| 序号 | 实验步骤 | 预期现象和结论 |
| ① | 取少量反应后的固体于试管I中 | / |
② | 向试管I中的固体慢慢滴加 试管I口塞上带导管的单孔塞,并将导管通入盛有 | 若试管I中的 则丙同学推测正确.若试管I中的固体未完全溶解,且 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com