
| KW |
| c(H+) |
| A、④⑦ | B、②③④ |
| C、③⑧ | D、①⑤⑥ |
| KW |
| c(H+) |
| KW |
| c(H+) |


科目:高中化学 来源: 题型:
| A、钠与水反应:Na+2H2O=Na++2OH-+H2↑ |
| B、硅酸钠溶液与醋酸溶液混合:SiO32-+2H+=H2SiO3↓ |
| C、0.01mol/LNH4Al(SO4)2溶液与0.02mol/LBa(OH)2溶液等体积混合:NH4++A13++2SO42-+2Ba2++4OH-=2BaSO4↓+A1(OH)3↓+NH3?H2O |
| D、向次氯酸钙溶液通入SO2:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学式 | 电离常数 |
| HClO | K=3×10-8 |
| H2CO3 | K1=4×10-7 K2=6×10-11 |
| A、向Na2CO3溶液中滴加少量氯水:CO32-+2Cl2+H2O=2Cl-+2HClO+CO2↑ |
| B、向NaHCO3溶液中滴加少量氯水:2HCO3-+Cl2=Cl-+ClO-+2CO2↑+H2O |
| C、向NaClO溶液中通少量CO2:CO2+NaClO+H2O=NaHCO3+HClO |
| D、向NaClO溶液中通过量CO2:CO2+2NaClO+H2O=Na2CO3+2HclO |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、导致易拉罐变瘪的离子反应是:CO2+OH-=HCO3- |
| B、导致易拉罐又鼓起来的反应是:Al3++3HCO3-=Al(OH)3+3CO2 |
| C、若将CO2换为NH3,浓NaOH溶液换为水,易拉罐也会出现先瘪后鼓的现象 |
| D、上述过程中与NaOH溶液反应的物质有三种,且反应结束后的溶液显碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作及现象 | 实验结论 |
| A | 向某溶液中加入2滴含[Fe(CN)6]3-溶液,出现蓝色沉淀. | 该溶液中一定含有Fe2+ |
| B | 向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成 | 该溶液中一定含有SO42- |
| C | 某气体能使湿润的蓝色石蕊试纸变红 | 该气体是NH3 |
| D | 将少量某有机物滴加到新制氢氧化铜中,充分振荡,未见砖红色沉淀生成 | 该有机物不含醛基 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
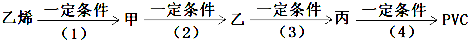
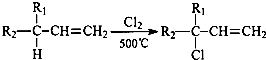
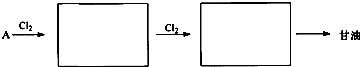
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、适当加热 |
| B、适量加NaOH. |
| C、适量加盐酸 |
| D、适量加KOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素编号 | 元素性质或原子结构 |
| T | 单质能与水剧烈反应,所得溶液呈弱酸性 |
| X | L层p电子数比s电子数多2个 |
| Y | 第3周期元素的简单离子中半径最小 |
| Z | L层有三个未成对电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com