
【题目】一定条件下,向密闭恒容容器中加入1.0mol/L X,发生反应:2X(g)Y(g)+Z(g),△H<0,反应到8min时达到平衡;在14min时改变的温度,16min时建立新平衡.X的物质的量浓度变化如图所示.下列有关说法正确的是( ) 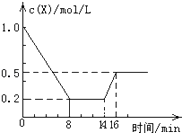
A.0~8min用Y表示的该反应的速度为0.1mol/Lmin
B.8min时达到平衡,该反应的平衡常数为 K=0.5
C.14min时,改变的反应条件是降低了体系的温度
D.16min时的正反应速率,比8min时的正反应速率大
【答案】D
【解析】解:A.由图可知,0~8min内X的浓度变化量为1mol/L﹣0.2mol/L=0.8mol/L,故v(X)= ![]() =0.1mol/(Lmin),根据速率之比等于化学计量数之比,则v(Y)=
=0.1mol/(Lmin),根据速率之比等于化学计量数之比,则v(Y)= ![]() v(X)=
v(X)= ![]() ×0.1mol/(Lmin)=0.05mol/(Lmin),故A错误;
×0.1mol/(Lmin)=0.05mol/(Lmin),故A错误;
B.由图可知,0~8min内X的浓度变化量为1mol/L﹣0.2mol/L=0.8mol/L,则:
2X(g) | Y(g)+ | Z(g) | ||
开始(mol/L) | 1 | 0 | 0 | |
变化(mol/L) | 0.8 | 0.4 | 0.4 | |
平衡(mol/L) | 0.2 | 0.4 | 0.4 |
故该温度下平衡常数k= ![]() =4,故B错误;
=4,故B错误;
C.由图可知,14min时瞬间X的浓度不变,不可能为改变压强,改变条件X的浓度增大,该反应正反应是放热反应,可能为升高温度或增大生成物的物质的量,故C错误;
D.由C分析可知,14min时改变条件为升高温度或增大生成物的物质的量,反应速率加快,故16min平衡时正、逆速率都高于8min时,故D正确;
故选D.
【考点精析】认真审题,首先需要了解化学平衡的计算(反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%).


科目:高中化学 来源: 题型:
【题目】根据如图可判断下列离子方程式中错误的是( ) 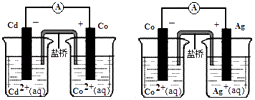
A.2Ag(s)+Cd2+(aq)=2Ag+(aq)+Cd(s)
B.Co2+(aq)+Cd(s)=Co(s)+Cd2+(aq)
C.2Ag+(aq)+Cd(s)=2Ag(s)+Cd2+(aq)
D.2Ag+(aq)+Co(s)=2Ag(s)+Co2+(aq)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列诗句或谚语, 说法不正确的是( )
A. “千淘万漉虽辛苦,吹尽狂沙始到金” (唐·刘禹锡 )描述的过程主要是物理变化
B. “水乳交融,火上浇油” 前者包含物理变化,而后者包含化学变化
C. “滴水石穿、绳锯木断” 不包含化学变化
D. “落汤螃蟹着红袍” 肯定发生了化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.常温下,PH=9的碳酸钠溶液中由水电离出的c(OH﹣)=1×10﹣9molL﹣1
B.饱和氯水中:c(Cl﹣)=c(ClO﹣)+c(HClO)
C.将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低
D.中和等体积pH相同的H2SO4和HCl溶液,消耗NaOH的物质的量为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原电池总反应离子方程式为:2Fe3++Fe═3Fe2+ , 能实现该反应的原电池是( )
A.正极为Cu,负极为Fe,电解质溶液为Fe(NO3)2溶液
B.正极为Cu,负极为Fe,电解质溶液为FeCl3溶液
C.正极为Fe,负极为Zn,电解质溶液为Fe2(SO4)3溶液
D.正极为Ag,负极为Fe,电解质溶液为CuSO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.向50mL 1mol?L﹣1的盐酸中加入烧碱,水的KW不变
B.NH4Cl和NH3?H2O混合液中,二者对对方的平衡都起了抑制作用
C.有两种弱酸HX和HY且酸性HX>HY,则体积和浓度相同的NaX和NaY溶液中有c(Y﹣)>c(X﹣)>c(OH﹣)>c(H+)
D.常温下0.1 mol?L﹣1的HA溶液中 ![]() =1×10﹣8 , 则0.01 mol?L﹣1 HA溶液中c(H+)=1×10﹣4mol?L﹣1
=1×10﹣8 , 则0.01 mol?L﹣1 HA溶液中c(H+)=1×10﹣4mol?L﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚铁是血红蛋白重要组成成分,起着向人体组织传送O2的作用,如果缺铁就可能出现缺铁性贫血,但是摄入过量的铁也有害.下面是一种常见补药品说明书中的部分内容:该药品含Fe2+33%~36%,不溶于水但能溶于人体中的胃酸:与Vc(维生素C)同服可增加本品吸收.
(1)(一)甲同学设计了以下下实验检测该补铁药品中是否含有Fe2+并探究Vc的作用:
加入新制氯水后溶液中发生的离子反应方程式是、Fe3++SCN﹣[Fe(SCN)]2+ .
(2)加入KSCN溶液后溶液变为淡红色,说明溶液中有少量Fe3+ . 该离子存在的原因可能是(填编号) .
A.药品中的铁本来就应该以三价铁的形式存在
B.在制药过程中生成少量三价铁
C.药品储存过程中有少量三价铁生成
(3)药品说明书中“与Vc同服可增加本品吸收”请说明理由 .
(4)(二)乙同学采用在酸性条件下用高锰酸钾标准溶液滴定的方法测定该药品是否合格,反应原理为5Fe2++8H++MnO4﹣=5Fe3++Mn2++4H2O.准确称量上述药品10.00g,将其全部溶于试剂2中,配 制成1000mL溶液,取出20.00mL,用0.0200mol/L的KMnO4溶液滴定,用去KMnO4溶液12.00mL. 该实验中的试剂2与甲同学设计的实验中的试剂1都可以是(填序号).
A.蒸馏水
B.稀盐酸
C.稀硫酸
D.稀硝酸
(5)本实验滴定过程中操作滴定管的图示正确的(填编号).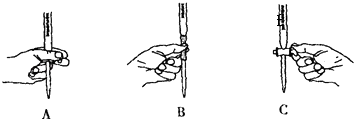
(6)请通过计算,说明该药品含“铁”量是否合格(写出主要计算过程)?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在15℃下将氨气通入一盛水的玻璃球内,至氨气不再溶解为止。经称量得知玻璃球内的饱和溶液质量为3.400g,然后将玻璃球浸入体积为50.00mL浓度为0.5000mol/L的硫酸溶液中,将球击破。充分反应后溶液中剩余的酸还能与10.00mL 1.000mol/L的NaOH溶液恰好完全反应生成正盐。该氨水中的溶质全部以NH3计,则:
(1)饱和溶液中NH3的物质的量为____________________。
(2)饱和溶液中NH3的质量分数为__________。
(3)测得所得饱和氨水的密度为0.918g/cm3,则饱和溶液中NH3的物质的量浓度为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对电解质的叙述正确的是( )
A.溶于水后得到的溶液能导电的物质
B.NaCl溶液在电流作用下电离成Na+和Cl-
C.NaCl是电解质故NaCl晶体能导电
D.氯化氢溶于水能导电,但气态氯化氢不能导电
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com