
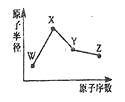
【题目】W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差l;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强.下列说法不正确的是( )
A. 对应简单离子半径:W>X
B. 对应气态氢化物的稳定性:Y<Z
C. 化合物XZW既含离子键,又含极性共价键
D. Z的氢化物和X的最高价氧化物对应水化物的溶液均能与Y的氧化物反应
【答案】D
【解析】试题分析:W、X、Y、Z是四种常见的短周期元素,W的一种核素的质量数为18,中子数为10,可知W的质子数为8,则W是氧元素;X和Ne原子的核外电子数相差1,且原子半径比W大,可知X为11号元素,故X为Na元素;Y的原子半径介于X和W之间,Y的单质是一种常见的半导体材料,所以Y是Si元素;Z的非金属性在同周期元素中最强,原子序数大于Si,故Z为Cl元素;A.O2-、Na+离子电子层结构相同,核电荷数越大,离子半径越小,故离子半径:O2->Na+,故A正确;B.非金属性Si<Cl,非金属性越强,氢化物越稳定,故B正确;C.化合物NaClO既含离子键,又含极性共价键,故C正确;D.Y的氧化物为二氧化硅,Z的氢化物为HCl,X高价氧化物对应的水化物为NaOH,二氧化硅能与氢氧化钠溶液反应,不能与盐酸反应,故D错误;故选D。


科目:高中化学 来源: 题型:
【题目】海洋约占地球表面积的71%,对其开发利用的部分流程如图所示。下列说法错误的( )

①试剂1可以选用NaOH溶液;
②从苦卤中提取Br2的反应的离子方程式为:2Br-+Cl2=Br2+2Cl-
③工业上,电解熔融MgO冶炼金属镁可减小能耗;
④制铝:工业上电解熔融氯化铝来制备铝;
⑤制钠:电解饱和NaCl溶液;
⑥炼铁:CO在高温下还原铁矿石中的铁
A. ①②④⑥B. ②③④⑥C. ①③④⑥D. ①③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】加热N2O5依次发生的分解反应为:
①N2O5(g) ![]() N2O3(g)+O2(g)
N2O3(g)+O2(g)
②N2O3(g) ![]() N2O(g)+O2(g)
N2O(g)+O2(g)
在容积为2 L的密闭容器中充入8 mol N2O5,加热到t ℃,达到平衡状态后O2为9 mol,N2O3为3.4 mol。则平衡体系中N2O5的物质的量浓度为
A. 1.8mol/L B. 0.9 mol/L C. 2.3 mol/L D. 4.0 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,化合物M对番茄灰霉菌有较好的抑菌活性,其合成路线如下图所示。
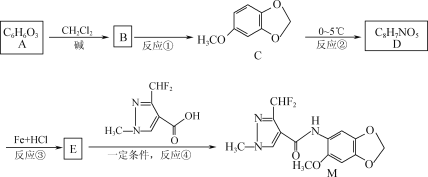
已知:
![]()
回答下列问题:
(1)化合物C中的含氧官能团为____________,反应④的反应类型为____________。
(2)写出E的结构简式:________________________。
(3)写出反应②的化学方程式:_____________________________________________。
(4)写出化合物C满足下列条件的一种同分异构体的结构简式:_________________。
① 含苯环结构,能在碱性条件下发生水解;
② 能与FeCl3发生显色反应;
③ 分子中含有4种不同化学环境的氢。
(5)已知CH3CH2CN![]() CH3CH2COOH。请以
CH3CH2COOH。请以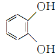 、CH2==CHCN和乙醇为原料合成化合物
、CH2==CHCN和乙醇为原料合成化合物 ![]() ,写出制备的合成路线流程图(无机试剂任用)_____。
,写出制备的合成路线流程图(无机试剂任用)_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝热反应的实验装置如图。下列有关铝热反应的说法中,不正确的是
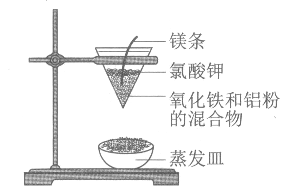
A. 铝热反应是放热反应
B. 铝热反应可用于冶炼某些高熔点金属
C. 实验中镁条的主要作用是还原氧化铁
D. 实验现象为火星四溅,漏斗下方有红热熔融物流出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸铁铵aFe2(SO4) 3·b(NH4) 2SO4·cH2O]广泛用于城镇生活饮用水、工业循环水的净化处理等。某化工厂以硫酸亚铁(含少量硝酸钙)和硫酸铵为原料,设计了如下工艺流程制取硫酸铁铵。
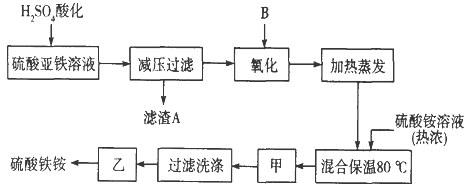
请回答下列问题:
(1)滤渣A的主要成分是__________________。
(2)下列物质中最适合的氧化剂B是________;反应的离子方程式__________________。
a.NaClO b.H2O2 c.KMnO4 d.K2Cr2O7
(3)操作甲、乙的名称分别是:甲______________,乙___________________。
(4)上述流程中,氧化之后和加热蒸发之前,需取少量溶液检验Fe2+是否已全部被氧化,所加试剂能否用酸性的KMnO4溶液?____(填“能”或“不能”)理由是: ________________________。(可用语言或方程式说明)
(5)检验硫酸铁铵中NH4+的方法是________________________________________。
(6)称取14.00 g样品,将其溶于水配制成100 mL溶液,分成两等份,向其中一份中加入足量NaOH溶液,过滤洗涤得到2.14 g沉淀;向另一份溶液中加入0.05 mol Ba (NO3) 2溶液,恰好完全反应。则该硫酸铁铵的化学式为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组的同学查阅相关资料知,氧化性:Cr2O72->Fe3+,设计了如图所示的盐桥原电池。盐桥中装有琼脂与饱和K2SO4溶液。下列叙述中正确的是
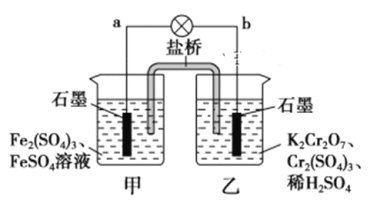
A. 甲烧杯的溶液中发生还原反应
B. 外电路的电流方向是从b到a
C. 电池工作时,盐桥中的SO42-移向乙烧杯
D. 乙烧杯中发生的电极反应为:2Cr3++7H2O-6e-===Cr2O72-+14H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学己经渗透到人类生活的方方面面。下列说法不正确的是
A. 为加快漂白精的漂白速率,使用时可滴加几滴醋酸
B. 明矾![]() 溶于水会形成胶体,因此可用于自来水的杀菌消毒
溶于水会形成胶体,因此可用于自来水的杀菌消毒
C. 月饼因富含油脂而易发生氧化,保存时常放入装有铁粉的透气袋作抗氧化剂
D. 为增强治疗缺铁性贫血效果,可在口服硫酸亚铁片时同服维生素C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯化碘(ICl3)在药物合成中用途非常广泛,其熔点:33 ℃,沸点:73 ℃。实验室可用如图装置制取 ICl3。
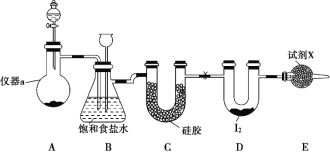
(1)仪器 a 的名称是_____。
(2)制备氯气选用的药品为漂白精固体[ 主要成分为 Ca(ClO)2] 和浓盐酸, 相关反应的化学方程式为______。
(3)装置 B 可用于除杂,也是安全瓶,能监测实验进行时装置 C 中是否发生堵塞,请写出发生堵塞时 B 中的现象是 ____。
(4)试剂 X 为_____。
(5)氯气与单质碘反应温度稍低于 70 ℃,则装置 D 适宜的加热方式为__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com