
下面是有关物质的转化关系图(有些物质已省略)。
若A为单质,E在常温下为液体,C的相对分子质量为78。请回答下列问题:

(1)画出A的原子结构示意图________,F的电子式是________。
(2)下面对C物质结构、性质的推断中,不正确的是________。
A.久置于空气中会变成白色
B.具有强氧化性
C.晶体中存在离子键和共价键
D.遇湿润的紫色石蕊试纸只能使其变蓝色
(3)若C是含氧化合物且氧为18O时,则C与D反应所得产物的摩尔质量分别为__________________。
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案科目:高中化学 来源: 题型:
]硫酸钠过氧化氢加合物(xNa2SO4·yH2O2·zH2O)的组成可通过下列实验测定:
①准确称取1.770 0 g样品,配制成100.00 mL溶液A。
②准确量取25.00 mL溶液A,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体0.582 5 g。
③准确量取25.00 mL溶液A,加适量稀硫酸酸化后,用0.020 00 mol·L-1 KMnO4溶液滴定至终点,消耗KMnO4溶液25.00 mL。H2O2与KMnO4反应的离子方程式如下:
2MnO +5H2O2+6H+===2Mn2++8H2O+5O2↑
+5H2O2+6H+===2Mn2++8H2O+5O2↑
(2)上述滴定若不加稀硫酸酸化,MnO 被还原为MnO2,其离子方程式为________________________________________________________________________。
被还原为MnO2,其离子方程式为________________________________________________________________________。
(3)通过计算确定样品的组成(写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关中和滴定的叙述正确的是( )
A.滴定时,标准液的浓度一定越小越好
B.用盐酸作标准液滴定NaOH溶液时,指示剂加入越多越好
C.滴定管在滴液前和滴液后均有气泡可能会产生误差
D.滴定时眼睛应注视锥形瓶内溶液的颜色变化而不应注视滴定管内的液面变化
查看答案和解析>>
科目:高中化学 来源: 题型:
美国普度大学研究开发出一种利用铝镓合金制备氢气的新工艺(如图所示)。下列有关该工艺的说法错误的是( )。

A.该过程中,能量的转化形式只有两种
B.铝镓合金可以循环使用
C.铝镓合金与水反应的化学方程式为:2Al+3H2O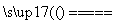 Al2O3+3H2↑
Al2O3+3H2↑
D.总反应式为2H2O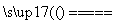 2H2↑+O2↑
2H2↑+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
已知热化学方程式:2SO2(g)+O2(g)2SO3(g) ΔH=-Q kJ·mol-1(Q>0)。下列说法正确的是 ( )。
A.相同条件下,2 mol SO2(g)和1 mol O2(g)所具有的能量小于2 mol SO3(g)
所具有的能量
B.将2 mol SO2(g)和1 mol O2(g)置于一密闭容器中充分反应后,放出热量为
Q kJ
C.增大压强或升高温度,该反应过程放出更多的热量
D.如将一定量SO2(g)和O2(g)置于某密闭容器中充分反应后放热Q kJ,则此
过程中有2 mol SO2(g)被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
当前环境问题是一个全球重视的问题,引起环境问题的气体常见的有温室气体CO2、污染性气体NOx、SOx等。如果对这些气体加以利用就可以成为重要的能源,既解决了对环境的污染,又解决了部分能源危机问题。
(1)二氧化碳是地球温室效应的罪魁祸首,目前人们处理二氧化碳的方法之一是使其与氢气反应合成甲醇,甲醇是汽车燃料电池的重要燃料。CO2与H2反应制备CH3OH和H2O的化学方程式为____________________________________________________
_____________________________________________________________________
(2)在高温下一氧化碳可将二氧化硫还原为单质硫。
已知:
①C(s)+O2(g)===CO2(g)ΔH1=-393.5 kJ·mol-1
②CO2(g)+C(s)===2CO(g)ΔH2=+172.5 kJ·mol-1
③S(s)+O2(g)===SO2(g)ΔH3=-296.0 kJ·mol-1
请写出CO与SO2反应的热化学方程式________________________________________
______________________________________________________________________。
(3)硝酸厂常用催化还原方法处理尾气。CH4在催化条件下可以将NO2还原为N2。
已知:CH4(g)+2O2(g)===CO2(g)+2H2O(g)ΔH=-889.6 kJ·mol-1①
N2(g)+2O2(g)===2NO2(g)ΔH=+67.7 kJ·mol-1②
则CH4还原NO2生成水蒸气和氮气的热化学方程式是__________________________
_________________________________________________________________ ______。
查看答案和解析>>
科目:高中化学 来源: 题型:
向分别盛有100 mL水、100 mL 0.1 mol·L-1盐酸、100 mL 0.01 mol·L-1硫酸铜溶液的X、Y、Z三个烧杯中各投入0.05 mol Na。下列有关说法正确的是( )
A.三个烧杯中均会发生的离子反应为2Na+2H2O===2Na++2OH-+H2↑
B.三个烧杯中钠均在液面上剧烈反应,且X烧杯中反应最剧烈
C三个烧杯反应后,生成的溶质的物质的量浓度相同
D.三个烧杯反应后,生成的气体的质量一定相同
查看答案和解析>>
科目:高中化学 来源: 题型:
有3份等质量的小苏打,第1份直接与盐酸恰好完全反应;第2份首先加热,使其部分分解后,再与盐酸恰好完全反应;第3份首先加热,使其完全分解后,再与盐酸恰好完全反应。假若盐酸的物质的量浓度相同,消耗盐酸的体积分别为V1、V2和V3,则V1、V2和V3的大小关系正确的是( )
A.V1>V2>V3 B.V1>V3>V2
C.V2>V3>V1 D.V1=V2=V3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com