
【题目】如图所示甲是某学生验证铜和浓硝酸反应的装置,乙、丙是另外两位同学对甲装置改进后的装置:
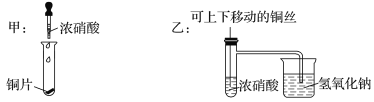
(1)甲、乙、丙三个装置中共同发生的反应的化学方程式是__________________________________。
(2)和甲装置相比,乙装置的优点是①______________________;②________________。
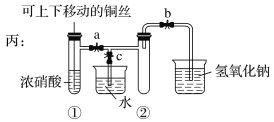
(3)为了进一步验证NO2和水的反应,某学生设计了丙装置。实验时先关闭活塞________,再打开活塞________,才能使NO2气体充满②试管;当气体充满②试管后,将铜丝提起与溶液脱离。欲使烧杯中的水进入②试管,应该_______________________。
【答案】Cu+4HNO3(浓)===Cu(NO3)2+2NO2↑+2H2O 可以控制反应的发生和停止 吸收NO2气体,防止污染环境 c ab 先关闭b,再关闭a,然后打开c,用手捂住试管②
【解析】
铜和浓硝酸反应的化学方程式是Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,根据题目给定的装置图可知乙装置有尾气处理装置,同时可以通过移动铜丝来控制反应的发生与停止。实验丙中,实验时先关闭活塞c,再打开活塞a,b,才能使NO2气体充满②试管,当气体充满②试管后,将铜丝提起与溶液脱离停止反应。欲使烧杯中的水进入②试管应该先关闭b,再关闭a,然后打开c,用手捂住试管②。
(1)三个装置中共同发生的反应的化学方程式是:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O。
故答案为:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O。
(2) 和甲装置相比,乙装置的优点是:乙装置有尾气处理装置,同时可以通过移动铜丝来控制反应的发生与停止,故答案为:可以控制反应的发生和停止;吸收NO2气体,防止污染环境。
(3)实验丙中,实验时先关闭活塞c,再打开活塞a,b,才能使NO2气体充满②试管,当气体充满②试管后,将铜丝提起与溶液脱离,停止反应。欲使烧杯中的水进入②试管,应该先关闭b,再关闭a,然后打开c,用手捂住试管②,气体膨胀,当二氧化氮与水接触后发生反应,气压减小,可以把水吸入试管②,故答案为:c ;ab ;先关闭b,再关闭a,然后打开c,用手捂住试管②。


 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案科目:高中化学 来源: 题型:
【题目】乙烯分子中C—C之间形成一个σ键和一个π键;乙炔分子C—C之间形成一个σ键和2个π键。根据所学理论,写出:
(1)在乙烯和乙炔分子与溴发生加成反应中,断裂何种类型键?____________
(2)写出加成反应方程式。__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】24Cr原子处于基态时,价电子排布可用电子排布图表示成![]() ,而不是
,而不是![]() 。下列说法中,正确的是()
。下列说法中,正确的是()
A. 这两种排布方式都符合能量最低原理
B. 这两种排布方式都符合泡利原理
C. 这两种排布方式都符合洪特规则
D. 这个实例说明洪特规则有时候和能量最低原理是矛盾的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国研究锂硫电池获得突破,电池的总反应是16Li+S8 ![]() 8Li2S ,充放电曲线如图所示,下列说法不正确的是( )
8Li2S ,充放电曲线如图所示,下列说法不正确的是( )
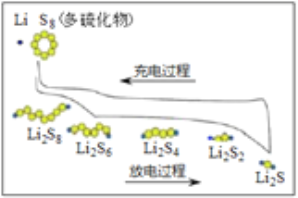
A. 充电时,电能转化为化学能
B. 放电时,锂离子向正极移动
C. 放电时,1mol Li2S6转化为Li2S4得到2mole-
D. 充电时,阳极总电极反应式是8S2- -16e- = S8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在如图装置中,烧瓶中充满干燥气体a。将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满整个烧瓶。a和b可能是

a(干燥气体) | b(液体) | |
① | NH3 | 水 |
② | CO2 | 饱和NaOH溶液 |
③ | Cl2 | 饱和食盐水 |
④ | NO2 | 水 |
⑤ | HCl | 0.1 mol·L1AgNO3溶液 |
A. ①②③ B. ①②⑤ C. ②④⑤ D. ①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以有机物A合成聚酯类高分子化合物F的路线如下图所示:

已知:①RCH=CH2 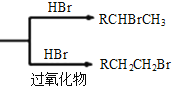 ②丙酮能被KMnO4(H+)氧化,使之褪色
②丙酮能被KMnO4(H+)氧化,使之褪色
(1)A生成B的反应类型为_______,C中含氧官能团的名称为_______。
(2)G是与CH3OH相对分子质量相差56的同系物,且不能使KMnO4(H+)褪色,G的名称为__________________
(3)检验A分子碳碳双键的方法_______________________________________________。
(4)D与NaOH水溶液反应的化学方程式为_____________________________________。
(5)E在一定条件下还可以合成含有六元环结构的H,则H的结构简式为____________。
(6)若F的平均相对分子质量为25200,则其平均聚合度为_______________
(7)满足下列条件的C的同分异构体有____________种(不考虑立体异构)。
①含有1个六元碳环,且环上相邻4个碳原子上各连有一个取代基
②1mol该物质与新制氢氧化铜悬浊液反应产生2mol砖红色沉淀
(8)写出以![]() 为原料(其他试剂任选)制备化合物
为原料(其他试剂任选)制备化合物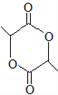 的合成路线,请用以下方式表示:
的合成路线,请用以下方式表示:![]() 目标产物。__________________
目标产物。__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食盐晶体是由钠离子和氯离子组成的,且均为等距离的交错排列,如图所示。已知食盐的密度是2.2 g/cm3,阿伏加德罗常数为6.02×1023/mol。在食盐晶体中两个距离最近的钠离子间的距离最接近于 厘米(保留整数)。
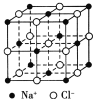
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A. 0.1molSiO2晶体中含有Si-O键的数目为0.2NA
B. 56g铁粉与高温水蒸气反应,生成H2数目为1.5NA
C. 标准状况下,22.4 LCl2溶于水,转移电子数为NA
D. 18gH218O和D2O的混合物中,所含中子数为9NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com