
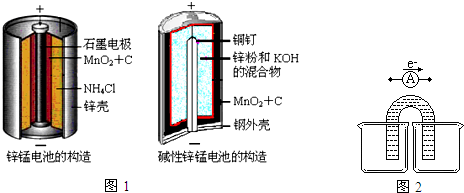
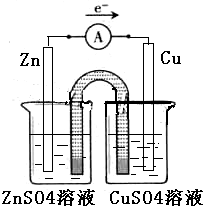
 ,故答案为:
,故答案为: ;
;

科目:高中化学 来源: 题型:
| A、①②⑤ | B、①③⑥ |
| C、②④⑤ | D、①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、NaAlH4中含有离子键和非极性共价键 |
| B、每生成11.2 L(标准状况下)H2,转移NA个电子 |
| C、NaAlH4中氢元素为+1价,在反应中有50%的氢被还原 |
| D、反应中氧化产物与还原产物的物质的量之比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、所得分散系极不稳定 |
| B、具有丁达尔效应 |
| C、不能透过滤纸 |
| D、以上性质都不具有 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、磁铁矿--Fe2O3--炼铁 |
| B、胆矾--CuSO4?5H2O--波尔多液 |
| C、蓝宝石--SiO2--饰品 |
| D、纯碱--NaHCO3--焙制糕点 |
查看答案和解析>>
科目:高中化学 来源: 题型:
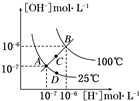
| A、图中四点KW间的关系:A=D<C<B |
| B、若从A点到C点,可采用温度不变在水中加少量CH3COONa固体 |
| C、若从A点到D点,可采用温度不变在水中加少量酸 |
| D、若处在B点所在的温度,将pH=2的硫酸与pH=10的NaOH的两种溶液等体积混合后,溶液显中性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
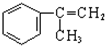 丙:分子式C9H8O,(部分性质,能使Br2/CCl4褪色 )由甲出发合成丙的路线之一如下:
丙:分子式C9H8O,(部分性质,能使Br2/CCl4褪色 )由甲出发合成丙的路线之一如下: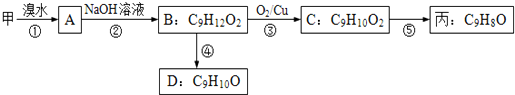
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com