
| A. | 0.1mol•L-1的FeCl3溶液中:HCO3-、K+、SO42-、Br- | |
| B. | 滴入酚酞试液显红色的溶液中:NH4+、SO42-、Fe2+、Cl- | |
| C. | 通入大量SO2的溶液中:Na+、Cl-、S2-、SO42- | |
| D. | pH=1的溶液中:Mg2+、Ca2+、NO3-、Ag+ |
分析 A.Fe3+、HCO3-发生双水解反应;
B.滴入酚酞试液显红色的溶液呈碱性,离子之间不反应且和OH-不反应的离子能大量共存;
C.SO2具有氧化性和还原性,能和强还原性、强氧化性物质发生氧化还原反应;
D.pH=1的溶液呈酸性,离子之间不反应且和H+不反应的离子能大量共存.
解答 解:A.Fe3+、HCO3-发生双水解反应生成Fe(OH)3和CO2而不能大量共存,故A错误;
B.滴入酚酞试液显红色的溶液呈碱性,NH4+、Fe2+和OH-反应生成弱电解质NH3.H2O、沉淀Fe(OH)2而不能大量共存,故B错误;
C.SO2具有氧化性和还原性,能和S2-发生氧化还原反应而不能大量共存,故C错误;
D.pH=1的溶液呈酸性,这几种离子之间不反应且和H+不反应,所以能大量共存,故D正确;
故选D.
点评 本题考查离子共存,为高频考点,侧重考查复分解反应、氧化还原反应、双水解反应,明确离子性质及离子共存条件是解本题关键,注意限制性条件、隐含条件离子共存的判断,题目难度不大.


科目:高中化学 来源: 题型:填空题
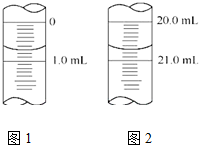 维生素C是一种水溶性维生素(其水溶液呈酸性),它的分子式是C6H8O6.人体缺乏这种维生素易得坏血症,所以维生素C又称抗坏血酸.维生素C易被空气中的氧气氧化.在新鲜水果、蔬菜、乳制品中都含维生素C,如新鲜橙汁中维生素C的含量在500mg•L-1左右.某校课外活动小组测定了某品牌的软包装橙汁中维生素C的含量.下面是测定实验分析报告,请填写有关空白.
维生素C是一种水溶性维生素(其水溶液呈酸性),它的分子式是C6H8O6.人体缺乏这种维生素易得坏血症,所以维生素C又称抗坏血酸.维生素C易被空气中的氧气氧化.在新鲜水果、蔬菜、乳制品中都含维生素C,如新鲜橙汁中维生素C的含量在500mg•L-1左右.某校课外活动小组测定了某品牌的软包装橙汁中维生素C的含量.下面是测定实验分析报告,请填写有关空白.| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗NaOH溶液的体积(mL) | 20.05 | 20.00 | 18.80 | 19.95 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性:HNO3>H2CO3>H2SiO3 | B. | 稳定性;H2S>H2O>HF | ||
| C. | 还原性:Cl->Br->I- | D. | 碱性:NaOH>Mg(OH)2>Ca(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
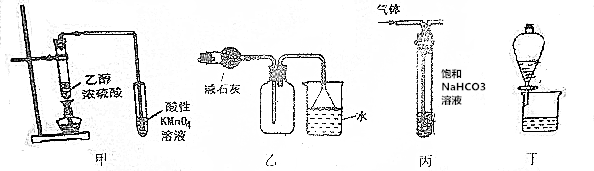
| A. | 装置甲可用于检验乙烯生成 | |
| B. | 装置乙可用于收集和吸收氨气 | |
| C. | 装置丙可用于出去CO2中混有的SO2气体 | |
| D. | 装置丁可分离碘的CCl4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两种粒子,若核外电子排布完全相同,则其化学性质一定相同 | |
| B. | 离子化合物中,一定存在金属元素和非金属元素 | |
| C. | 同时含有离子键和共价键的化合物,一定是离子化合物,不可能是共价化合物 | |
| D. | 难失电子的原子,获得电子的能力一定强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
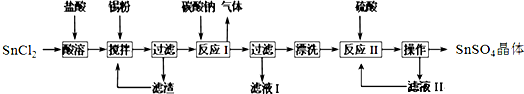
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中和相同体积的两种酸溶液所需NaOH的物质的量相同 | |
| B. | 醋酸溶液的浓度小于盐酸 | |
| C. | 两种溶液中由水电离出来的c(H+)不相同 | |
| D. | 分别用蒸馏水稀释相同倍数后,盐酸的pH大于醋酸的pH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com