
A、 如图是为了标志不同类的危险品,装运浓硫酸的包装箱应贴的标志 |
| B、闻化学药品的气味时都不能将鼻子凑近药品 |
| C、配制一定物质的量浓度的溶液过程中,用玻璃棒引流时,玻璃棒下端与容量瓶刻度线下方内壁相接触 |
| D、点燃可燃性气体之前,要先检验气体的纯度 |


科目:高中化学 来源: 题型:
| A、Cl2,饱和食盐水 |
| B、SO2 氨水 |
| C、NH3,稀盐酸 |
| D、NO2水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D | |
| X | FeCl2溶液 | FeCl3溶液 | Fe | Na2SO4溶液 |
| Y | FeCl3 | CuCl2 | Al | Na2CO3 |
| Z | Fe | Fe | NaOH溶液 | BaCl2溶液 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 起始物质的量 | 甲 | 乙 | 丙 |
| n(H2O)/mol | 0.10 | 0.20 | 0.20 |
| n(CO)/mol | 0.10 | 0.10 | 0.20 |
| A、甲容器中平均反应速率v(CO)与乙容器中平均反应速率v(CO)相同 |
| B、该反应的平衡常数表达式为K=c(CO) c(H2O)/c(CO2) c(H2) |
| C、平衡时,甲容器中CO的转化率与丙容器中CO的转化率相同 |
| D、平衡时,乙中c(H2O)是甲中的2倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:
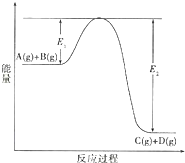 反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题.
反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com