
下列化合物中含有共价键的是()
A. MgCl2 B. HCl C. NaCl D. KCl
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:
下列叙述正确的是()
A. 交叉分类法和树状分类法是化学上仅有的两种分类方法
B. 化合物中某元素处于最高价只能被还原
C. H2SO4在电流作用下在水中电离出H+和SO42﹣
D. 偏二甲肼(分子式:C2H8N2)是一种有机高能燃料,它的摩尔质量为60g
查看答案和解析>>
科目:高中化学 来源: 题型:
若NA表示阿伏加德罗常数,下列说法正确的是()
A. 1mol Na2O2与水反应时,转移电子的数目为2NA
B. 标准状况下,22.4L水中含有水分子的数目为NA
C. 14g N2中含有电子的数目为7NA
D. 数目为NA的一氧化碳分子和0.5mol甲烷的质量比为7:4
查看答案和解析>>
科目:高中化学 来源: 题型:
某盐的混合物中含有0.2mol/L Na+、0.4mol/L Mg2+、0.4mol/L Cl﹣,则SO42﹣为()
A. 0.1 mol/L B. 0.2 mol/L C. 0.3 mol/L D. 0.4 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
已知A为淡黄色固体,T、R为两种常见的用途很广的金属单质,D是具有磁性的黑色晶体,C是无色无味的气体,H是白色沉淀,W溶液中加入KSCN出现血红色.
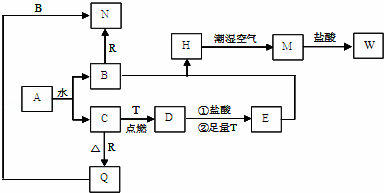
(1)写出下列物质的化学式:D: E: N: .
(2)B与E混和得到H并在潮湿空气中变成M的过程中,可能观察到的现象: ;
(3)按要求写方程式:
B和R反应生成N的离子方程式: ;
M→W的离子方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
肼(N2H4)﹣空气燃料电池是一种环保碱性燃料电池,其电解质溶液是20%﹣30%的KOH溶液.电池总反应为:N2H4+O2=N2↑+2H2O.下列关于该燃料电池工作时的说法正确的是()
A. 电池工作时,负极附近溶液的碱性增强
B. 正极的电极反应式是:O2+4H++4e﹣=2H2O
C. 负极的电极反应式是:N2H4+4OH﹣﹣4e﹣=4H2O+N2↑
D. 溶液中阴离子向正极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
化学反应A2+B2═2AB的能量变化如图所示,则下列说法正确的是()
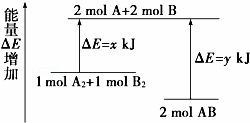
A. 该反应是吸热反应
B. 断裂1 mol A﹣A键和1 mol B﹣B键能放出x kJ能量
C. 形成2 mol A﹣B键需要放出y kJ的能量
D. 2 mol AB的总能量高于1 mol A2和1 mol B2的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组原子中,彼此化学性质一定相似的是( )
|
| A. | 原子核外电子排布式为1s2的X原子与原子核外电子排布式为1s22s2的Y原子 |
|
| B. | 原子核外M层上仅有两个电子的X原子与原子核外N层上仅有两个电子的Y原子 |
|
| C. | 2p轨道上有三个未成对的电子的X原子与3p轨道上有三个未成对的电子的Y原子 |
|
| D. | 最外层都只有一个电子的X、Y原子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com