
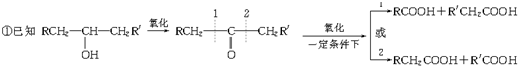
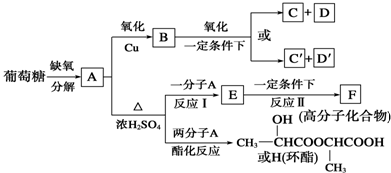
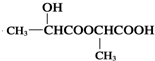 ��֪��AΪCH3CH��OH��COOH��һ����A������E��E�����ɸ߷��ӻ�����F������֪EΪCH2=CHCOOH��FΪ
��֪��AΪCH3CH��OH��COOH��һ����A������E��E�����ɸ߷��ӻ�����F������֪EΪCH2=CHCOOH��FΪ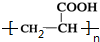 ����Ӧ��Ϊ��ȥ��Ӧ����Ӧ��Ϊ�Ӿ۷�Ӧ��A������BΪCH3COCOOH��������Ϣ�٣�B��һ��������������C���D�䣬C���Ǽ��ᣨHCOOH������D��ΪHOOCCOOH��C��C����ͬϵ�����CΪCH3COOH��DΪH2CO3���ݴ˴��⣮
����Ӧ��Ϊ��ȥ��Ӧ����Ӧ��Ϊ�Ӿ۷�Ӧ��A������BΪCH3COCOOH��������Ϣ�٣�B��һ��������������C���D�䣬C���Ǽ��ᣨHCOOH������D��ΪHOOCCOOH��C��C����ͬϵ�����CΪCH3COOH��DΪH2CO3���ݴ˴��⣮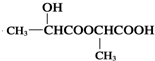 ��֪��AΪCH3CH��OH��COOH��һ����A������E��E�����ɸ߷��ӻ�����F������֪EΪCH2=CHCOOH��FΪ
��֪��AΪCH3CH��OH��COOH��һ����A������E��E�����ɸ߷��ӻ�����F������֪EΪCH2=CHCOOH��FΪ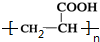 ����Ӧ��Ϊ��ȥ��Ӧ����Ӧ��Ϊ�Ӿ۷�Ӧ��A������BΪCH3COCOOH��������Ϣ�٣�B��һ��������������C���D�䣬C���Ǽ��ᣨHCOOH������D��ΪHOOCCOOH��C��C����ͬϵ�����CΪCH3COOH��DΪH2CO3��
����Ӧ��Ϊ��ȥ��Ӧ����Ӧ��Ϊ�Ӿ۷�Ӧ��A������BΪCH3COCOOH��������Ϣ�٣�B��һ��������������C���D�䣬C���Ǽ��ᣨHCOOH������D��ΪHOOCCOOH��C��C����ͬϵ�����CΪCH3COOH��DΪH2CO3��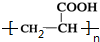 ��
��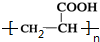 ��
�� | Ũ���� |
| �� |
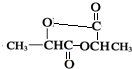 +2H2O��A��HBr��Ӧ�ķ���ΪCH3CH��OH��COOH+HBr��CH3CH��Br��COOH+H2O��C����������Һ��Ӧ�ķ���ʽΪHCOOH+2Ag��NH3��2OH
+2H2O��A��HBr��Ӧ�ķ���ΪCH3CH��OH��COOH+HBr��CH3CH��Br��COOH+H2O��C����������Һ��Ӧ�ķ���ʽΪHCOOH+2Ag��NH3��2OH | �� |
| Ũ���� |
| �� |
 +2H2O��CH3CH��OH��COOH+HBr��CH3CH��Br��COOH+H2O��HCOOH+2Ag��NH3��2OH
+2H2O��CH3CH��OH��COOH+HBr��CH3CH��Br��COOH+H2O��HCOOH+2Ag��NH3��2OH | �� |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������£�Ũ�Ⱦ�Ϊ0.05mol/L��NaOH��Һ��HCl��Һ����3��2��������ϣ�������Һ��pH����12 |
| B�������£���ϡ��ˮ��μ���ϡ�����У�����Һ��pH=7ʱ��2c��SO42-����c��NH4+�� |
| C�������£�0.1mol/L�������0.1mol/L�����������������ϣ���Ϻ���ҺpH=7 |
| D�������£�pH=4�Ĵ�����Һ��pH=10������������Һ�������Ϻ����ҺpH��7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ü�ȩ���ݺ��� |
| B������ľ�ĺ�ֲ��ոѵ���Ҫ�ɷֶ�����ά�� |
| C�����ع��͡���ֹʳ�ã������������Ʒ��� |
| D�����ݹ����������Һ�Ĺ���������������ϩ�����Կ��ô��ﱣ��ˮ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
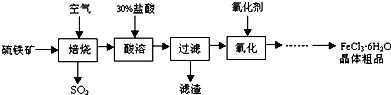
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� |
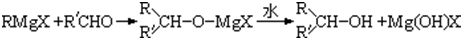 ��R��R���������ͬ��������Ҳ�����Dz�ͬ��������
��R��R���������ͬ��������Ҳ�����Dz�ͬ��������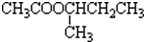 �Ĺ������£���Ӧ�����Ͳ��ֲ���û���г�����
�Ĺ������£���Ӧ�����Ͳ��ֲ���û���г�����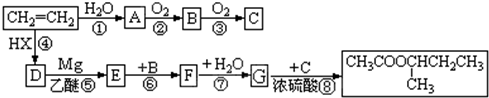
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| A����װ����ͭΪ���� |
| B����ͭƬ�������仯��12.8 gʱ��a�������ĵ�O2�ڱ�״���µ����Ϊ2.24 L |
| C����װ����b���ĵ缫��Ӧʽ�ǣ�H2+2OH--2e-�T2H2O |
| D����װ����a��Ϊ����������������Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
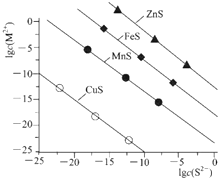 25��ʱ����Na2S����Cu2+��Mn2+��Fe2+��Zn2+���ֽ������ӣ�M2+��������S2-���Ũ�ȵĶ���ֵlgc��S2-����lgc��M2+����ϵ��ͼ��ʾ������˵����ȷ���ǣ�������
25��ʱ����Na2S����Cu2+��Mn2+��Fe2+��Zn2+���ֽ������ӣ�M2+��������S2-���Ũ�ȵĶ���ֵlgc��S2-����lgc��M2+����ϵ��ͼ��ʾ������˵����ȷ���ǣ�������| A��Ksp��CuS��ԼΪl��10-20 |
| B����Cu2+Ũ��Ϊ10-5mol?L-1��ˮ�м���ZnS��ĩ������CuS�������� |
| C����l00mLŨ�Ⱦ�Ϊ10-5mol?L-1 Zn2+��Fe2+��Mn2+�Ļ����Һ����μ���10-4mol?L-1 Na2S��Һ��Zn2+�ȳ��� |
| D��Na2S��Һ�У�2c��S2-��+2c��HS-��+2c��H2S��=c��Na+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��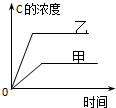 �о������¶ȶԷ�Ӧ��Ӱ�죬���ҵ��¶Ƚϸ� |
B��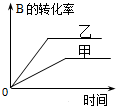 �о�����ѹǿ�Է�Ӧ��Ӱ�죬�Ҽ�ѹǿ�ϸ� |
C��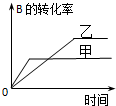 �о������¶ȶԷ�Ӧ��Ӱ�죬���ҵ��¶Ƚϵ� |
D��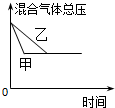 �о����Dz�ͬ�����Է�Ӧ��Ӱ�죬�Ҽ�ʹ�õĴ���Ч�ʽϸ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����Ƭ����NaOH��Һ�У�2Al+2OH-+6H2O=2[Al��OH��4]-+3H2�� |
| B��NaHCO3���룺NaHCO3?Na++H++CO32- |
| C��������̼���Ʒ�Ӧ��2H++CO32-=CO2��+H2O |
| D��ͭ���Ȼ�����Һ��Ӧ��Fe3++Cu=Cu2++Fe2+�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com