
| A. | 0.01 mol/L | B. | 0.015 mol/L | C. | 0.017 mol/L | D. | 0.05 mol/L |
分析 酸碱混合后,溶液中的c(OH-)=0.01mol/L,可知碱过量,根据c(OH-)=0.01mol/L=$\frac{n(O{H}^{-})-n({H}^{+})}{V混}$来计算.
解答 解:设NaOH和HCl的物质的量浓度均为x,NaOH和HCl溶液以3:2体积比相混合,体积分别为3V、2V,
酸碱混合后,溶液中的c(OH-)=0.01mol/L,
则根据c(OH-)=$\frac{n(O{H}^{-})-n({H}^{+})}{V混}$=$\frac{3Vx-2Vx}{5V}$=0.01mol/L,
解得x=0.05mol/L,
故选:D.
点评 本题考查酸碱混合的计算,明确混合后c(OH-)=0.01mol/L为碱过量是解答本题的关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| 纯净物 | 混合物 | 强电解质 | 弱电解质 | 非电解质 | |
| A | 盐酸 | 漂白粉 | 硫酸 | 醋酸 | 干冰 |
| B | 氢氧化钡 | 蔗糖溶液 | 硫酸钡 | 溴水 | 二氧化硫 |
| C | 胆矾 | 石灰水 | 氧化铝 | 水 | 氯气 |
| D | 小苏打 | 氢氧化铁胶体 | 氯化银 | 次氯酸 | 酒精 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
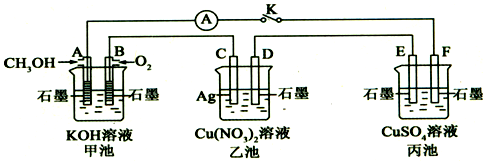
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 A、B、C是中学化学中常见的三种物质,它们之间的相互转化关系如图(部分反应条件及产物略去):
A、B、C是中学化学中常见的三种物质,它们之间的相互转化关系如图(部分反应条件及产物略去):查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 出现环境 | 实验事实 | |
| A | 以稀H2SO4为电解质的Cu-Zn原电池 | Cu为正极,正极上发生还原反应 |
| B | 电解CuCl2溶液 | 电子经过负极→阴极$\stackrel{通过电解液}{→}$阳极→正极 |
| C | 弱酸性环境下钢铁腐蚀 | 负极处产生H2,正极处吸收O2 |
| D | 将钢闸门与外加电源负极相连 | 牺牲阳极阴极保护法,可防止钢闸门腐蚀 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2SO2(g)+O2(g)?2SO3(g)△H=-196kJ/mol(反应热) | |
| B. | CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3kJ/mol(燃烧热) | |
| C. | NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=+57.3kJ/mol(中和热) | |
| D. | 2NO2=O2+2NO△H=-116.2kJ/mol(反应热) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{1}{22.4}$mol/L | B. | $\frac{1}{36.5}$mol/L | C. | $\frac{4}{5}$×$\frac{1}{22.4}$mol/L | D. | 无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AlCl3溶液和Al2(SO4)3溶液加热、蒸发、浓缩、结晶、灼烧,所得固体的成分相同 | |
| B. | 配制FeCl3溶液时,将FeCl3固体溶解在硫酸中,然后再用水稀释到所需的浓度 | |
| C. | 用加热的方法可除去KNO3溶液中混有的Fe3+ | |
| D. | Na2CO3溶液加水稀释后,恢复至室温,pH和KW均减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com