
下列说法错误的是
A.常温下,若醋酸钠与醋酸的混合溶液pH=7,则c(Na+)=c(CH3COO-)
B.某温度下,pH=6的NaCl溶液中离子浓度的大小关系:c(Na+)= c(Cl-)>c(H+)>c(OH-)
C.若2a mol·L-1HCN与a mol·L-1 NaOH溶液等体积混合后所得溶液中c(Na+)>c(CN-),则pH>7
D.含0.1 mol NaHCO3和0.2molNa2CO3的混合液中:c(Na+)+c(H+)=c(OH-)+c(HCO3—)+2c(CO32—)
B
【解析】
试题分析:根据电荷守恒,c(Na+)+ c(H+)=c(CH3COO-)+ c(OH-),pH=7,故c(Na+)=c(CH3COO-),A正确;NaCl溶液呈中性,c(H+)= c(OH-),故B错误;2a mol·L-1HCN与a mol·L-1 NaOH溶液等体积混合后,得到等物质的量浓度的NaCN和HCN,根据电荷守恒,c(Na+)+ c(H+)= c(OH-)+c(CN-),c(Na+)>c(CN-),所以c(H+)<c(OH-),故C错误;NaHCO3和Na2CO3的混合液中,c(Na+)+c(H+)=c(OH-)+c(HCO3—)+2c(CO32—),符合电荷守恒,故D正确。
考点:本题考查盐的水解、弱电解质电离。


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源:2014-2015山东省淄博市高二12月月考化学试卷(解析版) 题型:选择题
关于氯化铁水解的错误说法是
A.水解达到平衡(不饱和)时,无论加氯化铁饱和溶液还是加水稀释,平衡均向正方向移动
B.浓度为5mol/L和0.5mol/L的两种FeCl3溶液,其它条件相同时,Fe3+的水解程度前者比后者低
C.有50℃和20℃的相同浓度氯化铁溶液,其他条件相同时,Fe3+的水解程度前者比后者小
D.为抑制Fe3+水解,较好地保存FeCl3溶液,应加少量盐酸
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省高二上学期期中考试化学试卷(解析版) 题型:填空题
(10分)I、常温下在20mL0.1mol/L Na2CO3溶液中逐滴加入0.1mol/L HCl溶液40mL,溶液中含碳元素的各种微粒(CO2因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如图所示。

回答下列问题:
(1)在同一溶液中,H2CO3、HCO3-、CO32-(填:“能”或“不能”) 大量共存。
(2)已知在25℃时,CO32-水解反应的平衡常数(即水解常数用Kh表示)
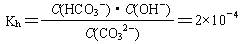
当溶液中c(HCO3-)︰c(CO32-)=2︰1时,溶液的pH= 。
(3)当混合液的pH=________时,开始放出CO2气体。
II、(1)常温下向25mL含HCl 0.01mol的溶液中滴加氨水至过量,该过程中水的电离平衡____________________(填写电离平衡移动情况)。当滴加氨水到25mL时,测得溶液中水的电离度最大,则氨水的浓度为______________。
(2)已知NH4A溶液为中性,又知HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH________7(填“>”、“<”或“=”)。
(3)25 ℃时,将a mol NH4NO3溶于水,向所得溶液中滴加b L氨水后溶液呈中性,则所滴加氨水的浓度是________mol·L-1。(用含a 、b 的式子表示)(NH3·H2O的电离平衡常数取Kb=2×10-5 mol·L-1)
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省高二上学期期中考试化学试卷(解析版) 题型:选择题
下列事实一定能说明HNO2为弱电解质的句数是
①常温时NaNO2溶液的pH大于7;
②用HNO2溶液做导电实验,灯泡很暗;
③HNO2与NaCl不能反应;
④常温下0.1 mol·L-1的HNO2溶液pH=2;
⑤1 L pH=1的HNO2溶液加水稀释至100 L后溶液的pH=2.2;
⑥1 L pH=1的HNO2溶液和1 L pH=1的盐酸分别与足量的NaOH溶液完全反应,最终HNO2消耗的NaOH多;
⑦HNO2溶液中加入一定量的NaNO2晶体,溶液中c(OH-)增大;
⑧HNO2溶液中加水稀释,溶液中c(OH-)增大。
A.4句 B.5句 C.6句 D.7句
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省赣州市北校区高二1月月考化学试卷(解析版) 题型:填空题
(5分)在一定温度下,将2 mol A和1 mol B两种气体相混合于体积为2 L的某密闭容器中(容积不变),发生如下反应:3A(g)+B(g) 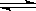 xC(g)+2D(g)ΔH<0,2 min末反应达到平衡状态(温度不变),生成了1mol D,并测得C的浓度为0.5 mol·L-1,请填写下列空白:
xC(g)+2D(g)ΔH<0,2 min末反应达到平衡状态(温度不变),生成了1mol D,并测得C的浓度为0.5 mol·L-1,请填写下列空白:
(1)x的值等于________________。
(2)该反应的化学平衡常数K=________,(填数值)升高温度时K值将________(选填“增大”、“减小”或“不变”)。
(3)A物质的转化率为__________________。
(4)若维持温度不变,在原平衡混合物的容器中再充入2mol C和2mol D,欲使达到新的平衡时,各物质的物质的量分数与原平衡相同,则至少应再充入A的物质的量为________mol。
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省赣州市北校区高二1月月考化学试卷(解析版) 题型:选择题
在一定温度下,反应AB(g)  1/2 A2(g)+1/2 B2(g)的平衡常数为0.1。若将1.0 mol的AB(g)通入体积为1.0 L的密闭容器中,在该温度时AB(g)的最大分解率接近于
1/2 A2(g)+1/2 B2(g)的平衡常数为0.1。若将1.0 mol的AB(g)通入体积为1.0 L的密闭容器中,在该温度时AB(g)的最大分解率接近于
A.5% B.17% C.25% D.33%
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏省高一12月月考化学试卷(解析版) 题型:计算题
把一小块镁铝合金溶于100mL盐酸中,然后向其中滴入1 mol·L-1 NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积如下图所示。

①写出OA段的离子反应方程式
②写出BC段的化学方程式
③合金中镁的质量 g。
④盐酸的物质的量浓度 mol·L-1。
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏省高一12月月考化学试卷(解析版) 题型:选择题
除去SO2中混有的HC1气体,可选用的试剂是
A.石灰水 B.浓硫酸
C.饱和NaHSO3溶液 D.饱和Na2SO3溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏省高二12月月考化学(必修)试卷(解析版) 题型:选择题
下列氯化物中,不能直接利用单质与氯气反应的得到是
A.AlCl3 B.NaCl C.MgCl2 D.FeCl2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com