
����Ŀ��2017��5��18���й����ʵ�����������ҹ����Ϻ����еĿ�ȼ���Բɻ�óɹ�����Ϊȫ���һ����ÿ�ȼ�������ȶ������Ĺ��ҡ���ȼ������Ȼ����ˮ������γɵľ������ʣ���Ҫ�����ڶ�����ͺ��״�½���С�����˵����ȷ����( )

�ټ����������ࣻ����ͬ�����£�������ܶȴ��ڿ������ܶȣ��ۼ���������ˮ���ܿ�ȼ����һ�ּ���DZ������Դ������ظ�ԭ���ܴ��ھ����������ȼ����
A.�٢ۢܢ�B.�ڢۢܢ�C.�٢ڢۢ�D.�٢ڢܢ�

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��ȷ���� ( )
A.Si��NaOH��Һ��Ӧ��Si��2OH����H2O===![]() ��H2��
��H2��
B.��Ca(HCO3)2��Һ�м���������NaOH��Һ��Ca2����![]() ��OH��===CaCO3��H2O
��OH��===CaCO3��H2O
C.���MgCl2��Һ��2H2O��2Cl��![]() 2OH����H2����Cl2��
2OH����H2����Cl2��
D.��0.2 mol FeI2����Һ�еμӺ�0.25 mol Cl2����ˮ��2Fe2����8I����5Cl2===2Fe3����4I2��10Cl��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ����С���о���������������ʱ���ı�ijһ�����Ի�ѧƽ���Ӱ�죬�õ����±仯����(ͼ��p��ʾѹǿ��T��ʾ�¶ȣ�n��ʾ���ʵ���)��

�������Ϲ����жϣ����н�����ȷ���ǣ� ��
A.��Ӧ����H��0��p2��p1B.��Ӧ����H��0��T1��T2
C.��Ӧ����H��0��T2��T1����H��0��T2��T1D.��Ӧ������H��0��T2��T1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������(ClNO)���л��ϳ��е���Ҫ�Լ�������NO��Cl2��ͨ�������·�Ӧ�õ�����ѧ����ʽΪ2NO(g)��Cl2(g)![]() 2ClNO(g)��
2ClNO(g)��
(1)���������������ڴ����еĺ������������ʱ�������������ȣ��漰���·�Ӧ���� 2NO2(g)��NaCl(s)![]() NaNO3(s)��ClNO(g) K1����4NO2(g)��2NaCl(s)
NaNO3(s)��ClNO(g) K1����4NO2(g)��2NaCl(s)![]() 2NaNO3(s)��2NO(g)��Cl2(g) K2����2NO(g)��Cl2(g)
2NaNO3(s)��2NO(g)��Cl2(g) K2����2NO(g)��Cl2(g)![]() 2ClNO(g) K3,��K1��K2��K3֮��Ĺ�ϵΪK3=_______________����K1��K2��ʾ����
2ClNO(g) K3,��K1��K2��K3֮��Ĺ�ϵΪK3=_______________����K1��K2��ʾ����
(2)��֪���ֻ�ѧ���ļ����������±������������ȵĽṹΪCl��N==O��
��ѧ�� | N��O | Cl��Cl | Cl��N | N==O |
����/(kJ��mol��1) | 630 | 243 | a | 607 |
��2NO(g)��Cl2(g)![]() 2ClNO(g)�ķ�Ӧ�� ��H��a�Ĺ�ϵΪ ��H = ___kJ��mol��1��
2ClNO(g)�ķ�Ӧ�� ��H��a�Ĺ�ϵΪ ��H = ___kJ��mol��1��
(3)300��ʱ��2NO(g)��Cl2 (g)![]() 2ClNO(g)������Ӧ���ʱ���ʽΪv�� = k��cn (ClNO)��������ʺ�Ũ�ȵĹ�ϵ���±���
2ClNO(g)������Ӧ���ʱ���ʽΪv�� = k��cn (ClNO)��������ʺ�Ũ�ȵĹ�ϵ���±���
��� | c(ClNO)/(mol��L��1) | v/(mol��L��1��s��l) |
�� | 0. 30 | 3. 60��10��9 |
�� | 0. 60 | 1. 44��10��8 |
�� | 0. 90 | 3. 24��10��8 |
n = ___��k = ____��
(4)������Ⱥ����ܱ������г������ʵ���֮��Ϊ2 : 1��NO��Cl2���з�Ӧ2NO(g)��Cl2(g)![]() 2ClNO(g)�����жϷ�Ӧ�Ѵﵽ��ѧƽ��״̬����__�����ţ���
2ClNO(g)�����жϷ�Ӧ�Ѵﵽ��ѧƽ��״̬����__�����ţ���
a�������е�ѹǿ���� b��2v��(NO) = v��(Cl2)c�������ƽ����Է����������ֲ��� d���÷�Ӧƽ�ⳣ�����ֲ���e��NO��Cl2������ȱ��ֲ���
(5)25��ʱ�������Ϊ2 L�Ҵ���ѹ�Ƶĺ����ܱ�������ͨ��0.08 mol NO��0.04 mol Cl2������Ӧ��2NO(g)��Cl2 (g)![]() 2ClNO(g)��H��
2ClNO(g)��H��
������Ӧ��ʼ��ƽ��ʱ�¶���ͬ����÷�Ӧ������ѹǿ(p)��ʱ��(t)�ı仯��ͼ������a��ʾ���� ��H __���>����<����ȷ������0��������������ͬ�����ı�ijһ����ʱ�������ѹǿ(p)��ʱ��(t)�ı仯��ͼ������b��ʾ����ı��������______��
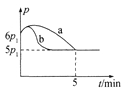
��ͼ�Ǽס���ͬѧ���������Ӧƽ�ⳣ���Ķ���ֵ(lg K)���¶ȵı仯��ϵ��������ȷ��������____����ס����ҡ�����mֵΪ_____��
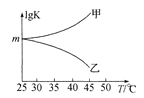
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������������ݻ�ΪVmL�ļ���ƿ���ռ����������ڿ�����δ�ž������ƿ������������������ܶ�Ϊ9.5������ʢ������ļ���ƿ������ˮ�У�ƿ��ˮ��������һ���߶Ⱥ�ֹͣ����������ͬ��ͬѹ�£�ƿ��ʣ����������Ϊ
A.![]() VmLB.
VmLB.![]() mLC.
mLC.![]() mLD.���ж�
mLD.���ж�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�����������᳧��������Ҫ�ɷ�Ϊ���������P����FeS��SiO2�ȣ��Ʊ���������ʽ�������ľۺ�����̷�(FeSO4��7H2O)���������£�
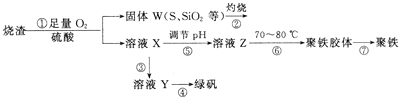
(1)���������в���������ͨ��������Һ�У���Һ������ɫ����_____�����ţ���
A��Ʒ����Һ B����ɫʯ����Һ C������KMnO4��Һ D����ˮ
(2)�������У�FeS��O2��H2SO4��Ӧ�����ӷ���ʽΪ_________��
(3)��������������������__________��
(4)ʵ����Ϊ�������õ��ľ�����Ʒ����Ԫ�ص�������������������ʵ�顣���÷�����ƽ��ȡ2. 800 g��Ʒ���ڽ���Ʒ�����������������������Ȼ�����Һ���۹��ˡ�ϴ�ӡ�����������ù�������Ϊ3. 495 g�����þ�����Ҫ�ɷ�Ϊ[Fe(OH) (SO4)]n����þ�����Ʒ����Ԫ�ص���������Ϊ____________�����������в�����Ԫ�غ���Ԫ�أ���
(5)��ͼ�ǽ�����������������SO2ת��Ϊ��Ҫ�Ļ���ԭ��H2SO4��ԭ��ʾ��ͼ�����õ�������Ũ����Ϊ49%���������ϲμӷ�Ӧ��SO2������H2O��������Ϊ______��
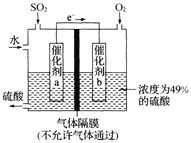
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ߺϽ��׳���֣���һ�������Ͻ�����������ϵ����С���ֳƲ���Ͻ��ʺ�������Ԫ�����ش��������⣺
![]() ��̬��ԭ�ӵļ۵��ӹ������ʽΪ____�����Ļ�̬ԭ�Ӻ���δ�ɶԵ�����Ϊ___����
��̬��ԭ�ӵļ۵��ӹ������ʽΪ____�����Ļ�̬ԭ�Ӻ���δ�ɶԵ�����Ϊ___����
![]() ����ͪ�
����ͪ�![]() ����ʽΪ
����ʽΪ![]() ������̼������������Ԫ���е�һ������������_____
������̼������������Ԫ���е�һ������������_____![]() ��Ԫ�ط���
��Ԫ�ط���![]() ����ϡ��ˮ�����У�
����ϡ��ˮ�����У�![]() �붡��ͪ�
�붡��ͪ�![]() ����ʽΪ
����ʽΪ![]() ��Ӧ�������ʺ�ɫ����������ӽṹ��ͼ��ʾ���ýṹ��̼ԭ�ӵ��ӻ���ʽΪ_______���ýṹ�г������Լ����Ǽ��Լ�����λ���⣬������__________��
��Ӧ�������ʺ�ɫ����������ӽṹ��ͼ��ʾ���ýṹ��̼ԭ�ӵ��ӻ���ʽΪ_______���ýṹ�г������Լ����Ǽ��Լ�����λ���⣬������__________��
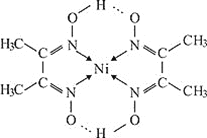
![]() ����������CO�����γ��ʻ������
����������CO�����γ��ʻ������![]() ��
��![]() ��1��
��1��![]() �������
�����к���![]() ����ĿΪ_______����֪
����ĿΪ_______����֪![]() ����Ϊ�������幹�ͣ������ܼ��ܹ��ܽ�
����Ϊ�������幹�ͣ������ܼ��ܹ��ܽ�![]() ����_______
����_______![]() ��д��ĸ
��д��ĸ![]() ��
��
A.���Ȼ�̼ ![]() ��
�� ![]() ˮ
ˮ ![]() Һ��
Һ��
![]() �����Ȼ��������۵�Ϊ
�����Ȼ��������۵�Ϊ![]() ���е�Ϊ
���е�Ϊ![]() �����Ȼ������۵�Ϊ
�����Ȼ������۵�Ϊ![]() ���е�Ϊ
���е�Ϊ![]() �������۷е����ϴ��ԭ����___________��
�������۷е����ϴ��ԭ����___________��
![]() ������
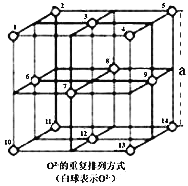
�����У�![]() ���ظ����з�ʽ��ͼ��ʾ�������з�ʽ�д���������1��3��6��7��
���ظ����з�ʽ��ͼ��ʾ�������з�ʽ�д���������1��3��6��7��![]() Χ�ɵ����������϶��3��6��7��8��9��12��
Χ�ɵ����������϶��3��6��7��8��9��12��![]() Χ�ɵ����������϶��
Χ�ɵ����������϶��![]() ����һ���
����һ���![]() ��������������϶�У���һ��
��������������϶�У���һ��![]() ��
��![]() ��������������϶�С���
��������������϶�С���![]() �����У����������϶����
�����У����������϶����![]() ��֮��Ϊ_______��
��֮��Ϊ_______��![]() �����ܶ�Ϊ
�����ܶ�Ϊ![]() �������
�������![]() _______
_______![]() д���������ʽ����
д���������ʽ����![]() ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C�����ձ��зֱ�ʢ����ͬ���ʵ���Ũ�ȵ�ϡ���ᡣ
A.  B.
B.  C.
C. 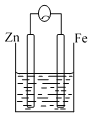
(1)A�з�Ӧ�����ӷ���ʽΪ_____��B��Cu���缫��ӦʽΪ______��
(2)C�б���ʴ�Ľ�����____________���ܷ�Ӧ����ʽΪ____________��
(3)A��B��C��������ʴ�����ʣ��ɴ�С��˳����__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1�������Ȼ�����Һ�ش��������⣺
����FeCl3��Һ�м�������NaHCO3������������Ϊ___�������ӷ���ʽ��ʾ��ԭ��___��
�ڲ��ϼ���FeCl3��Һ������ˮ�ֲ����գ��õ��Ĺ�����___��
��������FeCl3��Һʱ��Ϊ��ֹ��Һ����ǣ�Ӧ����___��
��2�����÷�ӦCu+H2O2+H2SO4=CuSO4+2H2O���һ��ԭ��أ��ش��������⣺
�ٸ�������Ϊ___��������ӦʽΪ___��
�ڷ�Ӧ������SO![]() ��____���ƶ���
��____���ƶ���
�۵���·��ת��0.1mol����ʱ�����Һ����(�����缫)������___�ˡ�
��3����֪25��ʱ����������ʵĵ���ƽ�ⳣ�����������ʾ���ش��������⣺
��ѧʽ | CH3COOH | H2CO3 | HClO |
����ƽ�ⳣ�� | Ka=1.8��10-5 | Ka1=4.3��10-7 Ka2=5.6��10-11 | Ka=3.0��10-8 |
�����ʵ���Ũ�Ⱦ�Ϊ0.1molL-1��������Һ��pH��С�������е�˳����__���ñ����д��
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
�ڳ����£�0.1molL-1CH3COOH��Һ��ˮϡ�����У����б���ʽ�����ݱ�����___������ĸ��
A.c��H+�� B.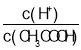 C.c��H+��c��OH-�� D.
C.c��H+��c��OH-�� D.![]() E.
E.![]()
��д�������������Һ��ͨ������������̼�����ӷ���ʽ��____��
��25��ʱ��CH3COOH��CH3COONa�Ļ����Һ������û��ҺpH=6������Һ��c��CH3COO-��-c��Na+��=____����ȷ��ֵ����
�ݱ�״���£���1.12LCO2ͨ��100mL1molL-1��NaOH��Һ�У�����Һ������Ũ�ȷ���������е�ʽ��c��OH-��=2c��H2CO3��+____��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com