
【题目】通常条件下,下列物质能用化合反应制得的是
A.![]() B.
B.![]() C.
C.![]() D.CuS
D.CuS
【答案】B
【解析】
两种或两种以上的物质反应生成一种物质的反应为化合反应。
A.可通过可溶性的铝盐和碱发生复分解反应生成氢氧化铝;
B.氢氧化亚铁和氧气、水反应生成氢氧化铁;
C.利用强酸制取弱酸的原理制备硅酸;
D.硫和铜反应生成硫化亚铜。
![]() 制备氢氧化铝,可用铝盐和氨水反应,离子反应为:
制备氢氧化铝,可用铝盐和氨水反应,离子反应为:![]() ,属于复分解反应,无法以化合反应制取,故A错误;
,属于复分解反应,无法以化合反应制取,故A错误;
B.反应方程式为:![]() ,B可以实现,故B正确;
,B可以实现,故B正确;
C.制备硅酸的反应为:![]() ,是两种化合物相互交换成分生成另外两种化合物的反应,故为复分解反应,故C错误;
,是两种化合物相互交换成分生成另外两种化合物的反应,故为复分解反应,故C错误;
D.硫为弱氧化剂,则铜粉和硫粉混合加热制备硫化亚铜,无法通过化合反应制取硫化铜,故D错误;
故选:B。


科目:高中化学 来源: 题型:
【题目】硫、氯的单质和化合物应用广泛。
(1)将硫铁矿和焦炭按物质的量之比为3∶2混合放在炼硫炉中,通入适量空气,发生下列燃烧反应:
FeS2+C+O2→Fe3O4+CO+S。
配平上述化学反应方程式:______________________________。生成3 mol硫,被氧化物质的物质的量为__________________。
(2)盐酸是应用广泛的酸之一,它具有
a.酸性;b.氧化性;c.还原性;d.挥发性。
请回答下列问题:
①浓盐酸长时间露置在空气中,溶液的质量减轻,盐酸表现了________(填序号)。
②实验室用稀盐酸和锌粒反应制取氢气,盐酸表现了________(填序号),反应的离子方程式为_____________________________________________________________________。
③用盐酸除去铁表面的铁锈,盐酸表现了______(填序号),反应的离子方程式为__________________________________________________________________。
④实验室常用KMnO4和浓盐酸反应制取Cl2,反应的化学方程式为2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。被还原的元素是______,还原剂是______,氧化产物是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)硅和氯两元素的单质反应生成1 mol Si的最高价化合物,恢复至室温,放热687 kJ,已知该化合物的熔、沸点分别为-69 ℃和58 ℃,写出该反应的热化学方程式___________________________________。
(2)肼(N2H4)可作为火箭发动机的燃料,与氧化剂 N2O4反应生成 N2 和水蒸气。
已知:①N2(g)+2O2(g)=N2O4(l) ΔH1=-19.5 kJ·mol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH2=-534.2 kJ·mol-1
写出肼和 N2O4反应的热化学方程式___________________。
(3)饮用水中的 NO3-主要来自 NH4+。已知在微生物的作用下,NH 4+经过两步反应被氧化成 NO3-。两步反应的能量变化示意图如图:
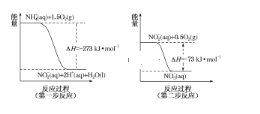
1mol NH 4+全部被氧化成 NO3-的热化学方程式为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语的相关表述中正确的是
A. 因H+(aq) +OH- (aq)==H2O(l) △H=-akJ·mol-1,故1molNaOH固体与足量的稀盐酸反应,放出的热量为akJ
B. 因CuSO4·5H2O(s)==CuSO4(s)+5H2O(1)△H=+bkJ·mol-1,故1molCuSO4(s)溶于水时,放出的热量为bkJ
C. 因氢气的燃烧热为c kJ·mol-1,故水电解的热化学方程式为2H2O (l)==2H2(g)+O2(g) △H=+c kJ·mol-1
D. 因N2(g)+3H2(g)![]() 2NH3(g) △H=-d kJ·mol-1,故在某容器中通入1molN2与3molH2充分反应后,放出的热量小于dkJ
2NH3(g) △H=-d kJ·mol-1,故在某容器中通入1molN2与3molH2充分反应后,放出的热量小于dkJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积固定的2L的密闭容器中,一定量的SO2与1mol O2在催化剂作用下加热到600℃发生反应:2SO2+O2![]() 2SO3;△H<0。当气体的物质的量减少0.2mol时反应达到平衡,在相同的温度下测得气体压强为反应前的8/9。下列有关叙述正确的是( )
2SO3;△H<0。当气体的物质的量减少0.2mol时反应达到平衡,在相同的温度下测得气体压强为反应前的8/9。下列有关叙述正确的是( )
A. 当SO3的生成速率与SO2的消耗速率相等时反应达到平衡
B. 降低温度,正反应速率减小程度比逆反应速率减小程度大
C. 将生成物SO3通入过量BaCl2溶液中,得到沉淀的质量为233g
D. 达到平衡时,平衡常数为2.5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烧碱样品中含有少量不与酸作用的可溶性杂质,为了测定烧碱的纯度,进行以下滴定操作:
A.在250mL容量瓶中定容成250mL烧碱溶液
B.用移液管移取25mL烧碱溶液于锥形瓶中并滴加几滴酚酞指示剂
C.在天平上准确称取烧碱样品W g,在烧杯中加蒸馏水溶解
D.将物质的量浓度为M mol·L-1的标准HCl溶液装入酸式滴定管,调整液面,记下开始刻度数为V1mL
E.在锥形瓶下垫一张白纸,滴定到终点,记录终点酸的体积V2mL
回答下列问题:
(1)正确的操作步骤的顺序是(用字母填写)________→________→________→D→________
(2)使用滴定管之前应进行的操作是________
(3)操作E中的锥形瓶下垫一张白纸的作用是________
(4)若酸式滴定管未用盐酸标准溶液润洗,会对测定结果有何影响________(填“偏高”、“偏低”或“无影响”)
(5)该烧碱样品的纯度计算式________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】平板电视显示屏生产过程中会产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2)。利用废玻璃粉末可以制取多种化工产品。设计流程如下:
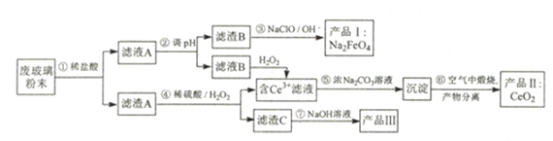
查阅资料可知:
①CeO2性质:淡黄或黄褐色粉末,不溶于水和碱,微溶于酸;有强氧化性。
②Ce3+在碱金属碳酸盐溶液中生成难溶的碳酸复盐Ce2(CO3):Na2CO3·2H2O。
③常温时两种沉淀物的溶度积见表:
沉淀物 | Fe(OH)3 | Ce(OH)3 |
Ksp | 4.0×10-38 | 1.5×10-20 |
回答下列问题:
(1)过程①分离操作中用到的玻璃仪器有_______________________________。
(2)过程④中发生反应的离子方程式为_________________________________,过程⑥中发生的化学反应方程式为__________________________________。
(3)产品I是一种新型、绿色的多功能净水剂,集氧化、灭菌、消毒、吸附、絮凝、沉淀等性能为一体。净水过程中,Na2FeO4 起到吸附、絮凝作用的原理是_________________。
(4)工业上也可用电解浓NaOH溶液制备产品I。用铁做电极,写出电解时阳极发生的电极反应方程式_________________。
(5)沉淀过程中,当某种离子浓度降至10—5 mol·L-1时,可认为此离子完全沉淀。过程②中Fe3+沉淀完全时溶液的pH=_____ (已知 lg2=0.3)。
(6)写出产品III的一种用途______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置图及实验用品均正确的是![]() 部分夹持仪器未画出)( )
部分夹持仪器未画出)( )
A. 实验室制硝基苯
实验室制硝基苯
B. 石油分馏
石油分馏
C. 实验使用经酒精制取乙烯
实验使用经酒精制取乙烯
D. 实验室制乙酸乙酯
实验室制乙酸乙酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溶液 A中可能含有如下离子:Na+、NH4+、Ba2+、Mg2+、SO42-、SO32-、Cl-、OH-。某同学设计并完成了如下的实验:
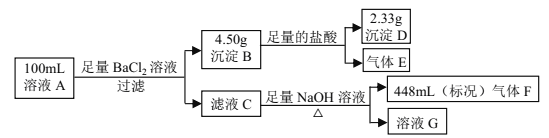
下列说法正确的是
A. 溶液 A 中一定存在 NH4+、 SO42-、 SO32-,可能存在 Na+
B. 溶液 A 中一定存在 NH4+、 Mg2+、 SO42-、 SO32-,可能存在 Cl-
C. 溶液 A 中可能存在 Cl-,且 c(Na+) ≥ 0.20 mol·L-1
D. 如果气体 F 能使湿润的蓝色石蕊试纸变红,说明溶液中一定含有 NH4+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com